阿尔茨海默病(俗称老年痴呆),一种离我们有点远,但却是许多老年人绕不过去的顽疾,我们该如何应对它?这可能是无论普通人还是学术界一直关注的问题,今天我们就系统聊一聊这个问题。
01,阿尔茨海默病:当我们开始遗忘
记性不好是很多时候我们喜欢给自己找的借口,然而如果这种记性不好变成一种真正的疾病,那么可能就不大妙了。
而这,正是阿尔茨海默病的一个重要表现。作为一种神经退行性疾病,阿尔茨海默病的典型表现就是记忆力衰退,想象一下,你将逐步遗忘许多事情,先是短期记忆变差了,接下来是开始遗忘最近发生的事情,然后是更遥远的事情也遗忘了,直到你记不起你的同事,朋友,甚至是子女,这是一种多么可怕的事情。而且,阿尔茨海默病还会伴随着诸如言语能力、行动能力下降,认知受损等诸多问题,直到彻底离开这个世界。

(图源网络)
作为一种很早就被人记录的疾病,直到1901年,德国精神病学家阿尔茨海默第一次用自己名字命名了这个疾病,随后的几年里,他发现这种疾病并不罕见,而是广泛存在于人群中。
根据研究,阿尔茨海默病是一种典型的随着年龄不断增加的疾病,比如在美国,60-74岁年龄组的阿尔茨海默病发病率是5.3%,而到了74-84岁,在这个比例就上升到了13.8%,而85岁以上的人群,阿尔茨海默病的比例将高达34.6%【1】
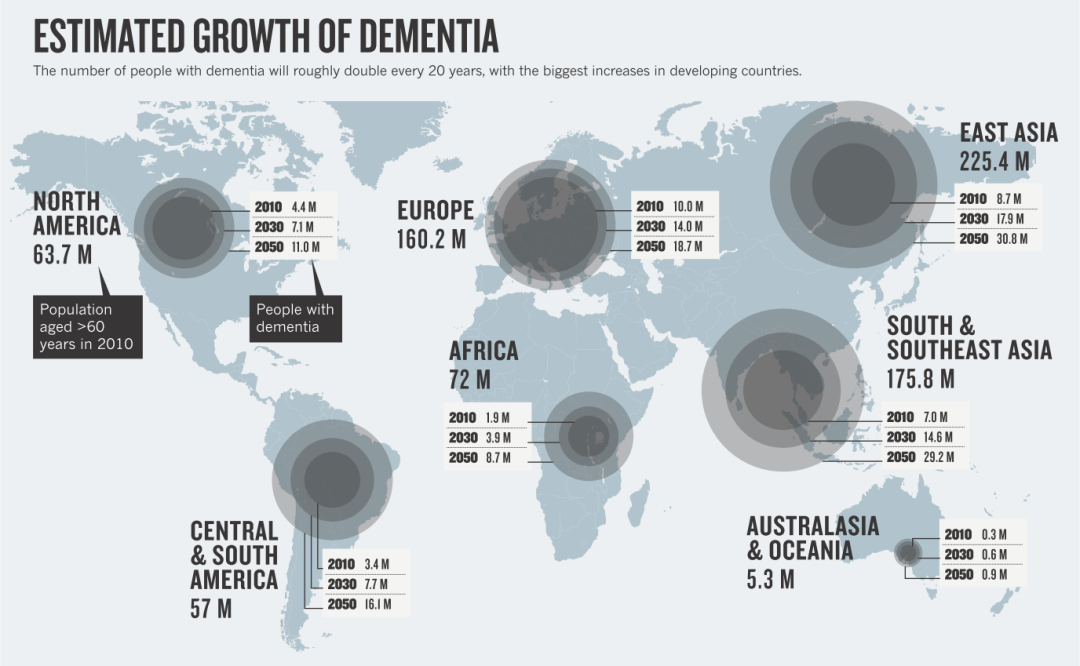
(图源【2】)
今天,无论是医生,还是科学家,都会告诉你,对于阿尔茨海默病,一定要早发现早治疗。
这个经验道理的背后,却是阿尔茨海默病研究及药物研发的一个痛楚:治不好的阿尔茨海默病。
02,治不好的阿尔茨海默病
近百年来,我们的科技和医学取得了长足的进步,哪怕是让人为之色变的癌症我们也取得了相当的进展,手术、化疗、放疗、免疫疗法等一系列策略都在进步,甚至出现了彻底治愈特殊血液瘤的免疫疗法。
然而,阿尔茨海默病,作为一种发现了上百年的疾病,我们的手段竟然十分的有限,甚至可以说是“束手无策”,这一切,都在于我们对于阿尔茨海默病的研究坎坷不断。
03,人为什么会得埃尔茨海默病呢?
人为什么会得阿尔茨海默病呢?最早对于阿尔茨海默病患者的脑切片观察,为我们提供了深刻的认知。
和正常人相比,阿尔茨海默病的人大脑呈现了明显的萎缩,而从病理学角度,阿尔茨海默病的最显著病理特征就是其大脑存在大量的由淀粉样蛋白(Aβ)组成的老年斑,而这也引发了阿尔茨海默病机制研究的最主要领域:β淀粉样蛋白假说。即大脑中产生的Aβ淀粉样蛋白是有毒性的,能够不断地损害大脑,最后造成大脑退行性变化【4】。

(图源【3】)
这一点事实上在试验中也得到了证实。
Aβ是来源于β淀粉样前体蛋白(amyloid precursor protein,APP)基因编码。正常情况下,APP会由α分泌酶和β分泌酶剪切形成可溶性的s-αAPP肽,随后被进一步裂解成为p3肽。然而在极少数情况下,APP蛋白会由β分泌酶和γ分泌酶裂解形成Aβ【5】。
根据γ分泌酶剪切位置的差异,会形成由40和42个氨基酸组成的Aβ蛋白(Aβ40,Aβ42),这两种蛋白是引发AD的重要蛋白,尤其是Aβ42容易聚集,具有较强的细胞毒性,最后形成AD患者脑中淀粉样斑块。
而反过来,如果减少Aβ的生成,则可以降低阿尔茨海默病的发病率,比如Aβ基因上发现了稀有突变A673T可以降低Aβ生成,从而降低了人群的AD发病率,并对老年人认知能力具有保护作用【6】。
这一切似乎都很完美,然而当科学家们试着去清除大脑的Aβ,无论是通过直接清除Aβ的药物,还是间接的通过影响β分泌酶和γ分泌酶来减少Aβ生成,结果却都无法解决阿尔茨海默病。
当然,可能有不少人会想到最近发生的Aβ56造假事件,甚至有人认为这摧毁了阿尔茨海默病的基本假说,其实想多了。Aβ56最多只是阿尔茨海默病中的Aβ假说的一个小分支,真正的Aβ假说本身,依然是经得住考验的最基础假说。
当然,也有科学家去寻找阿尔茨海默病的其他机制,比如针对神经纤维缠结(neurofibrillary tangle,NFT),这是一种由tau蛋白引发的神经变化【7】,甚至还开发出了相应的药物,但是结果依然一样,失败。
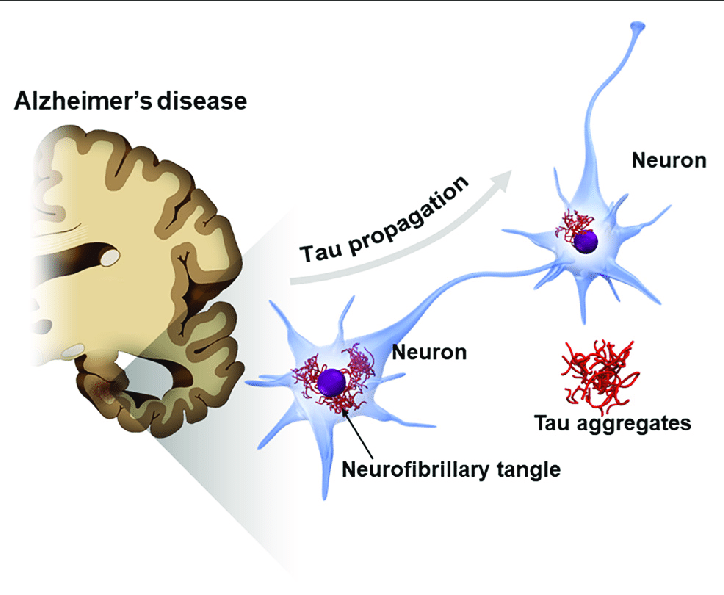
(图源【8】)
除此以外,还有科学家提出了微生物感染假说,这是依据对Aβ蛋白结构的进化来源判断,以及口腔疾病发病率和阿尔茨海默病发病率的相关性得出的,但是我们目前无法找到解决办法。
可以说,这些年,对于阿尔茨海默病的机制以及治疗探索一直在进行,然而一直是屡败屡战。
当然,这并未阻止人们对阿尔茨海默病药物的研发,比如CDE(国家食品药品监督管理局药品审评中心)的网站上依然能够看到目前在进行的阿尔茨海默病药物研究,也许未来会找到真正的治疗阿尔茨海默病的药物,如果大家感兴趣的话,可以直接到CDE的官网上去做相关的查询。
而对于当前的阿尔茨海默病,反倒是最早提出的胆碱假说,即阿尔茨海默病是由于神经神经递质乙酰胆碱减少而造成的这种被认为是错误的理论,却成为了治疗阿尔茨海默病的唯一稻草,目前有关阿尔茨海默病的药物,基本上是针对胆碱的。
但是,这种药物,只对于早期有一定缓解作用,对于中晚期,无效。
因此,对于阿尔茨海默病来说,早发现、早治疗可能是唯一的选择。
04,早发现,早治疗可能是当下唯一的路
如今,针对阿尔茨海默病,早发现、早治疗基本上是业内的共识,那么阿尔茨海默病早期有哪些迹象呢?
一般认为,阿尔茨海默病早期的表现相对难以判断,但是我们还是可以寻找到一些迹象。典型的就是记忆力下降。尽管随着年龄增加,记忆力下降是普遍现象,但是如果一个人的记忆力下降较为明显,那么就得重点关注了。
除此以外,性格的改变也可能是阿尔茨海默病的重要标志之一,所以如果老人性情忽然变化,那么就要留意了。
而临床上,经过多年的总结,也有一套相对可靠地判断标准,比如典型的是1984年建立的NINCDS-ADRDA标准,通过这套检测标准,可以很大程度上分辨出阿尔茨海默病。
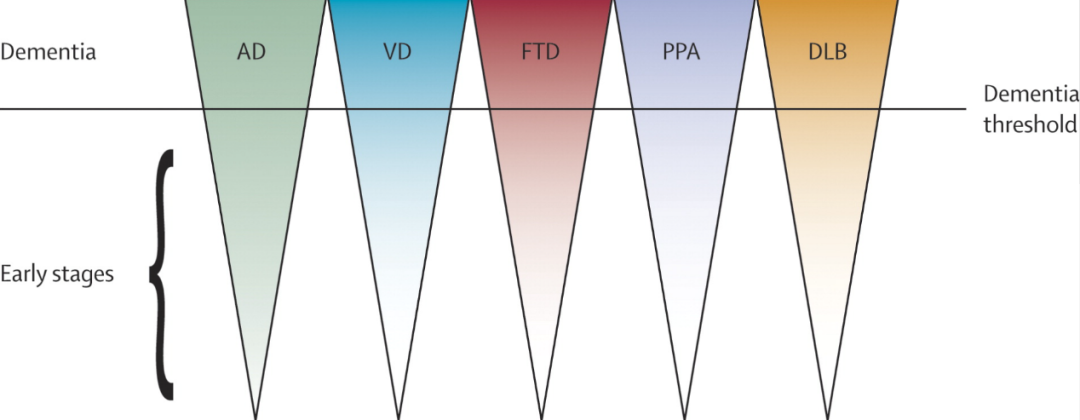
早期的治疗,目前主要是采取针对胆碱类的药物,比如AchE抑制剂、烟碱受体调节剂以及谷氨酸受体拮抗剂等药物能够显著的改善阿尔茨海默早期的表现。甚至对于正常群体来说,也可以通过该药物来降低阿尔茨海默病的发病风险。除此以外,抗抑郁类药物也被认为是对于阿尔茨海默病早期有一定的治疗效果,具体以医生建议为准。
当然,除了药物治疗,现实中还有一系列措施可以降低阿尔茨海默病的发病率。
比如体育锻炼,研究发现体育锻炼,尤其是有氧运动能够显著改善阿尔茨海默病的记忆和认知功能。
再比如一些益智类锻炼,如阅读,填字游戏,以及国际象棋等活动也能够改善阿尔茨海默病的症状。
这些策略,可以配合早期的治疗,让早期症状得到缓解并降低正常人的阿尔茨海默病发病率。
除此以外,预防也是一些好的思路。
05,如何预防呢?
那如何预防老年痴呆呢?一方面,努力降低风险因素,并对有可能性风险的群体重点关注。比如,对于某些基因型,要重点关注。
典型的是APOE 4基因型的个体,要重点关注,因为这种基因型比APOE2的阿尔茨海默病发病率高出十几倍【9】。TREM2基因也是近些年发现的一个和阿尔茨海默病发病风险相关的基因【10】。

再比如,一些疾病要重点关注,就像心脑血管疾病,中风,以及高胆固醇血症、高血压、糖尿病和吸烟等因素,都是阿尔茨海默病的高风险因素,因此也要重点关注这些疾病群体。
而在此基础之上,研究发现,许多小细节其实也是关系到了阿尔茨海默病的发病。
比如健康的生活方式、良好的饮食习惯、较低的心理压力,都是能够降低阿尔茨海默病的发病。
可以说,阿尔茨海默病作为一种影响非常严重的疾病,现实中对其的关注是远远不足的。而且由于相关药物和治疗措施的缺乏,使得阿尔茨海默病的应对必须是早发现早治疗,越早的介入,越有可能减轻阿尔茨海默病的发病情况。
此文章将被收录于「困在时间里的人——阿尔茨海默病专题」。
[1] Rajan K B , Weuve J , Barnes L L , et al. Population estimate of people with clinical Alzheimer's disease and mild cognitive impairment in the United States (2020–2060)[J]. Alzheimer's & Dementia, 2021.
[2]Abbott, Alison. "Dementia: a problem for our age." Nature 475.7355 (2011): S2-S4.
[3]Zolezzi, Juan M., and Nibaldo C. Inestrosa. "Comprehensive Overview of Alzheimer’s Disease Neurodegeneration, from Amyloid-β to Neuroinflammatory Modulation." Mechanisms of Neuroinflammation (2017).
[4] Tanzi R E . The synaptic Aβ hypothesis of Alzheimer disease[J]. Nature Neuroscience, 2005.
[5] Nunan J , Small D H . Regulation of APP cleavage by alpha-, beta- and gamma-secretases.[J]. Febs Letters, 2000, 483(1):6-10.
[6] Jonsson T, Atwal J K, Steinberg S, et al. A mutation in APP protects against Alzheimer’s disease and age-related cognitive decline[J]. Nature, 2012, 488(7409): 96.
[7]Takeda, Shuko. "Tau propagation as a diagnostic and therapeutic target for dementia: potentials and unanswered questions." Frontiers in neuroscience 13 (2019): 1274.
[8] Takeda S . Tau Propagation as a Diagnostic and Therapeutic Target for Dementia: Potentials and Unanswered Questions[J]. Frontiers in Neuroscience, 2019, 13:1274.
[9] Blennow K, de Leon MJ, Zetterberg H (July 2006). "Alzheimer's disease". Lancet. 368 (9533): 387–403.
[10]Guerreiro, Rita, et al. "TREM2 variants in Alzheimer's disease." New England Journal of Medicine 368.2 (2013): 117-127.







 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国