“疫苗”这个词,近日无疑成为了人们交相谈论的热门话题,而在此前,大多数人对疫苗并不陌生,毕竟,我们从出生开始就受着疫苗的保护。
过去注射的疫苗,往往是利用灭活或减毒的抗原来激发机体的免疫反应,我国目前在用的新冠疫苗,也主要属于这一类型。而美国辉瑞与德国BioNTech研发出来、欧美多国在用的,却是一种新型的mRNA疫苗。
mRNA我们都知道,但mRNA疫苗又是什么?它与我们现在注射的新冠灭活疫苗,又有何区别呢?酝酿多年的它,有着瞩目的优点,也有着需要攻关的技术难题。
 在高强度研发之下,mRNA疫苗已面世 | Pixabay, spencerbdavis1
在高强度研发之下,mRNA疫苗已面世 | Pixabay, spencerbdavis1
30年前发现的mRNA妙用
在许多人的印象中,mRNA作为一种新型的治疗药物或疫苗似乎是近几年的事,但其实这个概念出现于1989年。
细胞内的mRNA(Messenger RNA/信使RNA)携带着DNA的遗传信息,与核糖体相结合,翻译出指定的蛋白质——这好比是我们选好了糕点模具,拿着它,在面团上印出好吃的糕点。
 选好一个模子,印出许多个曲奇饼 | Unsplash, Jamie Daykin
选好一个模子,印出许多个曲奇饼 | Unsplash, Jamie Daykin
反过来,如果我们想要合成指定的蛋白质,是不是可以在外部刻好模具,把mRNA设计好了再往细胞中注入, 让细胞生产出指定的蛋白质来呢?
这一主意,确实可行。
一家位于加利福尼亚洲的生物制药公司伟科(Vical Incorporated)证明了,被脂质体包裹的mRNA可以顺利进入细胞内部——脂质体接触到人体细胞膜的时候,会因为成分相似而发生融合,顺利将脂质体中的mRNA送入细胞内。
之后,美国威斯康星大学的沃尔夫(Wolff)在《Science》发表的实验结果也证明,外部注射进小鼠肌肉细胞的mRNA可以正常发挥作用,并翻译出预期的蛋白质。
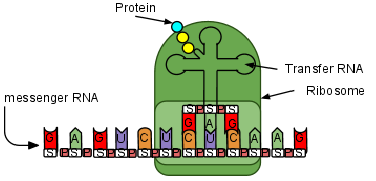 mRNA与核糖体结合,翻译出蛋白质 | Wikimedia Commons, pluma / CC BY-SA 3.0(https://creativecommons.org/licenses/by-sa/3.0)
mRNA与核糖体结合,翻译出蛋白质 | Wikimedia Commons, pluma / CC BY-SA 3.0(https://creativecommons.org/licenses/by-sa/3.0)
有了这成功的两步,于是科学家便广泛研究起mRNA在各方面的应用,比如做成疫苗。
以往的传统疫苗,采用的是灭活/减活的病原体,或者人工合成的病原体蛋白质外壳。将它们注射到体内时,这些外来物会被机体的免疫系统所识别,从而生产针对它们的抗体,还有记忆B细胞。
这些记忆B细胞会在免疫反应后以非常低的数量留存于血液中,当病原体再次感染人体时,它们便会被激活并在短时间内增殖,生产大量抗体来抵御外敌。
mRNA疫苗的原理,则是 直接往细胞里输送能够合成病原体蛋白质外壳的mRNA ,细胞就可以照着制作出同样的蛋白质外壳,作为抗原,来激发机体产生对应的免疫反应,产生抗体。
 传统疫苗,就好像商店里制作做好的小饼干;mRNA疫苗,则相当于买了模具,可以回家自制糕点 | Unsplash, Sigmund
传统疫苗,就好像商店里制作做好的小饼干;mRNA疫苗,则相当于买了模具,可以回家自制糕点 | Unsplash, Sigmund
抵御艾滋病?mRNA疫苗在准备
很多人不知道的是,mRNA疫苗曾经在艾滋病领域被深度研究过,且被认为是最有希望获得成功的一个选项。
HIV是一种攻击免疫细胞并造成其功能丧失的病毒,它会使人体易于感染各种疾病与肿瘤,且死亡率较高。治疗艾滋病的主要方法,是使用多种能够抵抗HIV、抑制病毒复制传播的药物复合制剂,来减缓病情的发展。
然而,这些药治标不治本。患者需要终生服用这些药物,一旦停止,那些被药物抑制而潜伏在身体里的HIV病毒便会伺机而动,重新活跃起来。这些药物除了会带来呕吐、晕眩、疼痛等副作用,它们的价格也非常昂贵。
 治疗艾滋病的药物,给人们带来了沉重负担 | Unsplash, Myriam Zilles
治疗艾滋病的药物,给人们带来了沉重负担 | Unsplash, Myriam Zilles
目前艾滋病在非洲、拉丁美洲等发展中国家仍然流行,有着大量病例。由于社会经济落后、医疗设施匮乏等原因,当地对艾滋病的防控做得并不好,而染病的人们,很多都无法承担昂贵的治疗费用。研究出价格便宜且更有效的防治手段,对于他们来说可谓迫在眉睫。
mRNA疫苗的出现,给他们带来了新的曙光。
以往直接注射的灭活/减毒抗原,通常会被细胞很快降解,而mRNA疫苗可以停留在细胞内 更长效地产生抗原 ,从而激起更有效的免疫反应,应对潜伏的病毒。
mRNA疫苗还可以引起 更加激烈的免疫反应 :在生产抗原的同时,mRNA本身也会被细胞内的模式识别受体(Pattern Recognition Receptor)所识别,两者一起激活免疫系统。
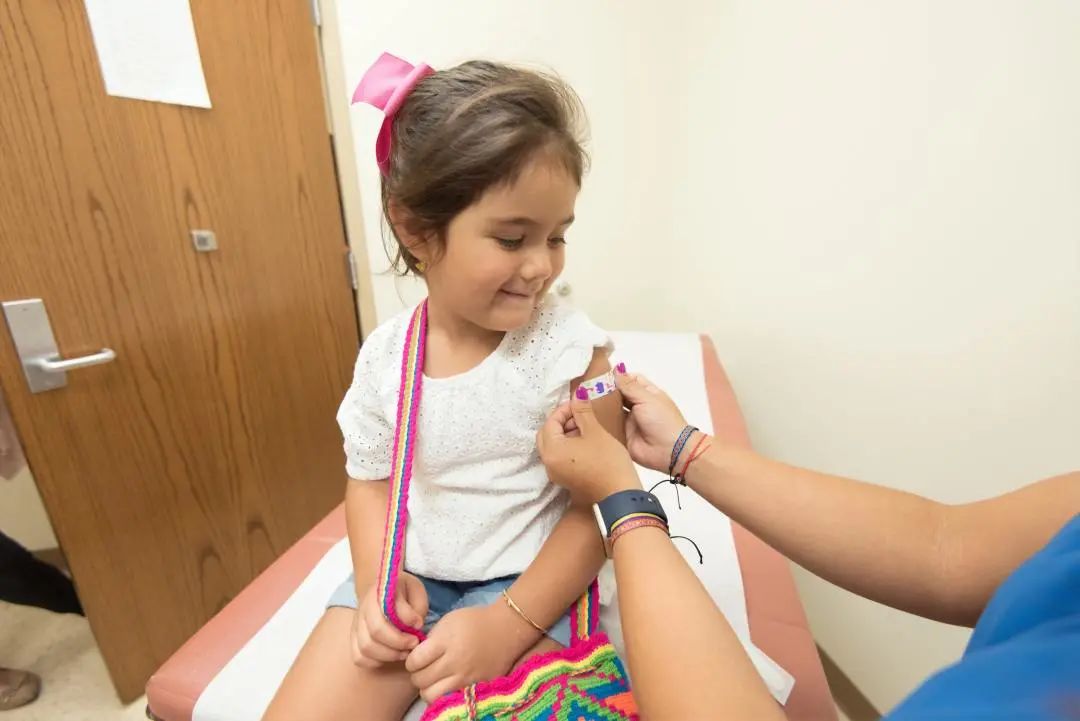 图 | Unsplash, CDC
图 | Unsplash, CDC
与传统疫苗相比,mRNA疫苗的 研发周期要短许多 ,因为无需筛选培养菌株、多次纯化蛋白质,目前向遗传基因中插入人工合成片段,这一技术已经相对成熟。兵贵神速,mRNA疫苗在面对突如其来的流行病时更显优势。
同时,HIV作为RNA病毒,变异速度非常快,而mRNA疫苗的灵活性,是应对这一问题的优秀种子选手。它可以 针对不同的靶点做出改变 ,甚至可以在面对不同免疫反应时,为不同的人特制疫苗。
 就好比不同模具,做出了不同小饼干 | Unsplash, Pille R. Priske
就好比不同模具,做出了不同小饼干 | Unsplash, Pille R. Priske
缓慢发展的研发进程
然而,伴随着诸多好处的mRNA疫苗,还有一些问题需要解决,比如mRNA的不稳定性、对冷链运输的要求、大批量生产的难度等等。与之相关的研究,一做就是二十年。
首先,虽然mRNA疫苗相比于DNA疫苗来说更安全,没有整合进宿主基因的风险(因为mRNA并不会进入细胞核,仅停留在细胞质内),但是它相对DNA疫苗及灭活疫苗来说 稳定性稍差 。
因此,科学家们对mRNA做出各种修饰,比如在mRNA前端加上帽子结构,尾部加上多聚腺苷酸尾巴,用甲基化后的伪尿嘧啶等方法来提高它的稳定性。
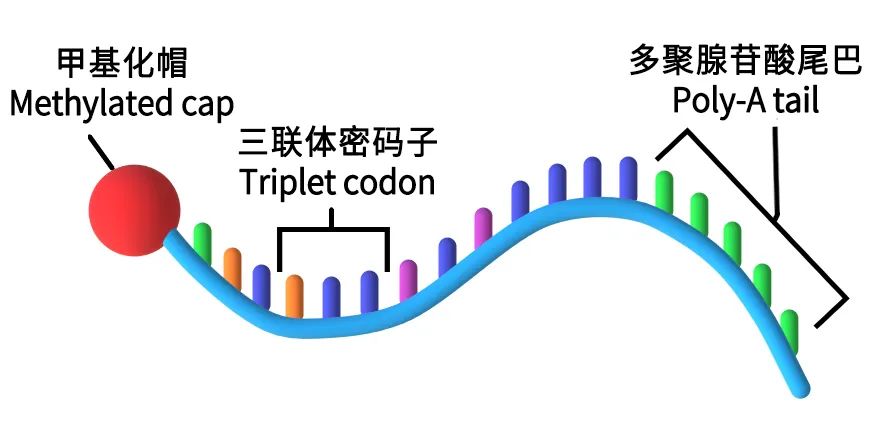 mRNA结构示意图 | Wikimedia Commons, Christinelmiller / CC BY-SA 4.0(https://creativecommons.org/licenses/by-sa/4.0)汉化:咻咻
mRNA结构示意图 | Wikimedia Commons, Christinelmiller / CC BY-SA 4.0(https://creativecommons.org/licenses/by-sa/4.0)汉化:咻咻
除此之外,不同的投递载体、双链DNA的污染,对于mRNA的 表达效率 也有影响,这将会使机体免疫应答的数量及质量发生变化。
然而,人体的免疫机制非常复杂,我们需要探索这些不同的因素是否具有不同的免疫特性。
在过去的二十年,科学家们尝试各种方法去攻克这些与mRNA疫苗相关的问题,虽然至今还未研发出艾滋病疫苗,但相关的研究成果已经惠及到了各个领域的疫苗研发和疾病治疗。
不少基础医学与临床医学都针对着疟疾、埃博拉、流感、寨卡、基孔肯雅热等等仍在肆虐的病原体,试图做出mRNA疫苗。而如今,这些实验结果与数据被应用到了新冠疫苗的制作上。
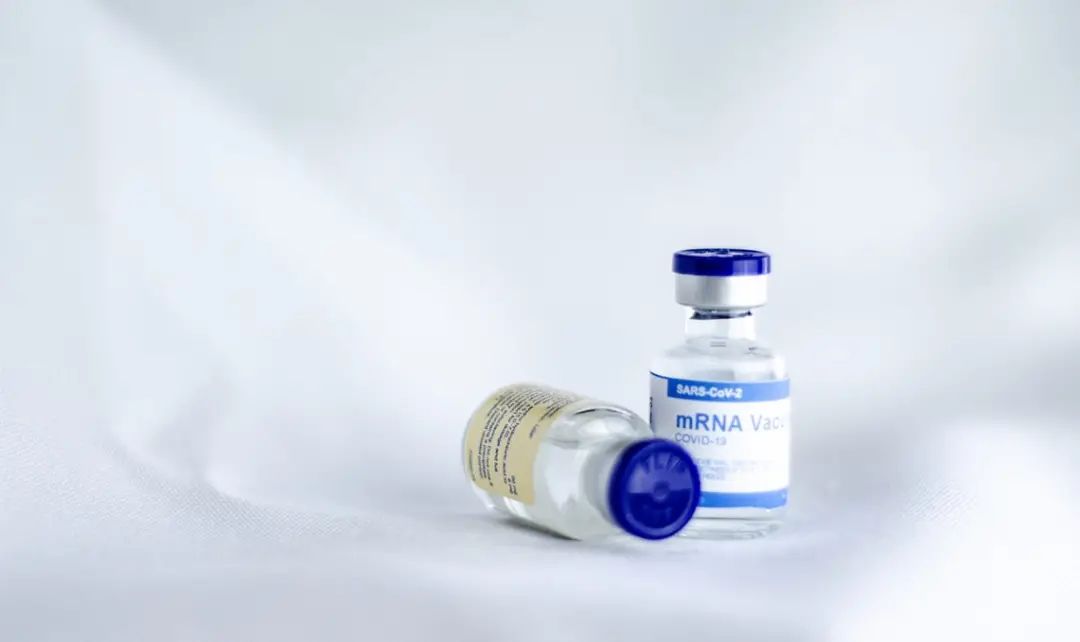 才有了新冠疫苗的快速研发 | Unsplash, Spencer Davis
才有了新冠疫苗的快速研发 | Unsplash, Spencer Davis
为新冠mRNA疫苗研发而铺垫
新冠疫情发生后,我国迅速制定了多种不同疫苗的研发技术路线,mRNA疫苗就是其中之一,预计5月可以开启海外多地临床实验。
美国、加拿大等等重仓购入的辉瑞和Moderna的新冠mRNA疫苗,也采用了往期mRNA疫苗的研究成果,利用 纳米脂质体粒(LNP) 进行运输,而这一技术曾在mRNA流感疫苗做过临床一期试验。
中东呼吸综合征冠状病毒(MERS-CoV)的mRNA疫苗相关研究,也被用作原型来优化新冠疫苗设计,来分析其引发的免疫反应。
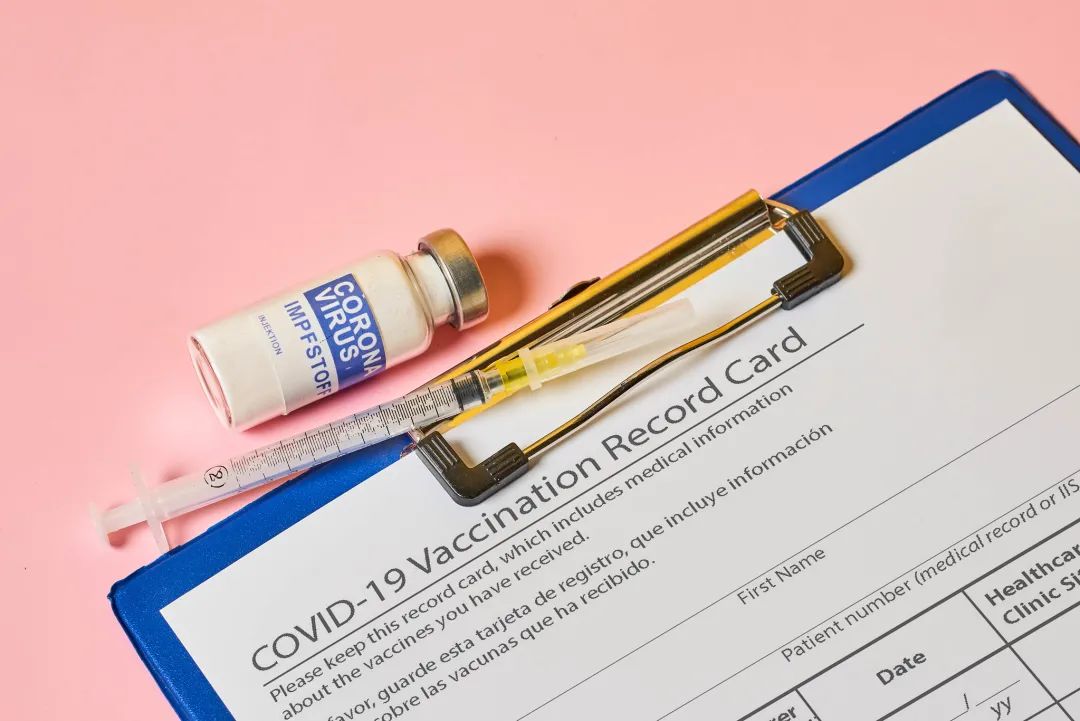 新冠疫苗,高速研发 | Flickr, Marco Verch Professional Photographer
新冠疫苗,高速研发 | Flickr, Marco Verch Professional Photographer
/ CC BY 2.0 (https://creativecommons.org/licenses/by/2.0/)
毫无疑问,新冠mRNA疫苗的迅速发展拯救了很多人的生命,而这一切都建立在前人无数研究的基础上。mRNA疫苗在安全、高效的同时,设计生产的速度也非常快,有潜力灵活应对各种流行病,甚至给艾滋病防控开启了新的大门。
这次的新冠mRNA疫苗作为首个通过临床试验、正式进入市场的疫苗,可以说是给整个mRNA制药领域打了一个强心剂。
 通过疫苗的保护,加强新冠疫情的防控 | Pixabay, Tumisu
通过疫苗的保护,加强新冠疫情的防控 | Pixabay, Tumisu
回顾历史,人们为应对贫困地区的流行病如艾滋病、登革热、埃博拉等等投入了不少的科研力量,攻克难关,而每一份努力也都有所回报。
我们在改善贫困地区卫生环境、扭转疫情局势的同时也为医疗新科技的发展奠基,这才有了当下新冠疫苗的高速研发。
全球健康与发展守卫计划
我们关心科学家的每一次灵光一现,关心在未知领域的每一步开拓和探索。但这次,我们想把目光投向全球贫困人群。
他们生活窘迫,面对伤害也更加脆弱:气候变化、传染病、饥饿、贫困、新生儿死亡、性别歧视……科学和创新,能为他们带来什么?
全球健康与发展守卫计划通过招募并培养创作者、传播者,促进各类优质内容产生,鼓励传播和发声,从而将关注全球健康与全球发展的理念传播给大众,让贫困人群获得更多关注,并期待让这种关注实实在在改善他们的境遇。
参考文献
[1] Crick F. Central dogma of molecular biology. Nature. 1970; 227 (5258): 561-563.
[2] Verbeke R, Lentacker I, De Smedt SC, Dewitte H. Three decades of messenger RNA vaccine development. Nano Today. 2019; 28 100766.
[3] Le Pag M. The Promice of mRNA extends far beyond the current pandemic. New Scientist (1971). 2020; 248 (3309): 14.
[4] Yoshimura K. Current status of HIV/AIDS in the ART era. Journal of Infection and Chemotherapy. 2017; 23 (1): 12-16.
[5] Mu Z, Haynes BF, Cain DW. HIV mRNA Vaccines—Progress and Future Paths. Vaccines. 2021; 9 (2): 134.
[6] Corbett KS, Edwards DK, Leist SR, Abiona OM, Boyoglu-Barnum S, Gillespie RA, et al. SARS-CoV-2 mRNA vaccine design enabled by prototype pathogen preparedness. Nature. 2020; 586 (7830): 567-571.
[7] Feldman RA, Fuhr R, Smolenov I, Ribeiro AM, Panther L, Watson M, et al. mRNA vaccines against H10N8 and H7N9 influenza viruses of pandemic potential are immunogenic and well tolerated in healthy adults in phase 1 randomized clinical trials. Vaccine. 2019; 37 (25): 3326-3334.
[8] Pardi N, Hogan MJ, Weissman D. Recent advances in mRNA vaccine technology. Current opinion in immunology. 2020; 65 14-20.
[9] Yi C, Yi Y, Li J. mRNA vaccines: possible tools to combat SARS-CoV-2. Virologica Sinica. 2020; 35 (3): 259-262.
[10] Wolff JA, Malone RW, Williams P, Chong W, Acsadi G, Jani A, et al. Direct gene transfer into mouse muscle in vivo. Science. 1990; 247 (4949): 1465-1468.
作者:陈语文
编辑、排版:咻咻






 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国