长期以来,金刚石在人们心中占据着重要地位。金刚石经过加工形成钻石,因其精美华丽的外表深受人们的喜爱。
在晶体学中,金刚石结构又称为金刚石立方晶体结构(diamond cubic lattice structure),原型是金刚石。在金刚石晶体中,每个碳原子都以sp3杂化轨道与另外4个碳原子形成共价键,构成正四面体。金刚石立方晶体结构中最小的碳环是六元环,最小的闭合碳环是十元环。闭合的十元碳环非常重要,它是构成晶胞的主要碳环,它的6个碳原子位于晶胞的6个面心,其余4个位于晶胞的内部,而另一个碳原子是晶胞的4个顶点。4个顶点的对角点就是四面体的另外4个顶点,十元环的对角线就是晶胞的棱长。
由于金刚石中的C-C键极强,所以金刚石硬度大,熔点极高;又因为所有的价电子均被限制在共价键区域,没有自由电子,所以金刚石不导电。
纯净的金刚石是无色透明、呈正八面体形状的固体,加工琢磨后璀璨夺目,用做装饰品。在自然界中,金刚石硬度最大,可以用来切割玻璃,也用做钻探机的钻头。
世界各地的钻石矿均具有相同的特征,因此,可以认为钻石是在较古老的地质历史时期形成于地幔深处,在后期火山活动中,被金伯利岩浆或钾镁煌斑岩岩浆带至地表,并赋存在金伯利岩和钾镁煌斑岩中,形成钻石原生矿。原生矿经过风化剥蚀作用,钻石被带至河流或滨海环境沉积下来,则形成钻石的次生砂矿。
自然界中天然钻非常少,大颗粒钻石更是凤毛麟角。一般来说,人们从1吨金刚石砂矿中,只能得到0.5克拉钻石,所以它们远不能满足人们日益增长的需求。因此,人们便开始尝试用人工合成方式来补充天然储量的不足。
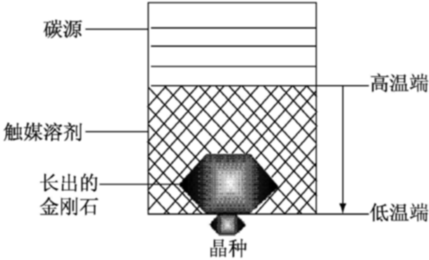
通用电气公司首次用HPHT法合成了小颗粒金刚石晶体。研究人员通过加热的反应室生成金刚石,该反应室由含钴的碳化钨压砧提供压力,将锰、铁、钴、镍等金属与石墨粉配成混合粉末, 作为触媒溶剂放置于反应室中。在压强约为6GPa, 温度为1500℃的条件下,金刚石处于碳的热力学稳定态,而石墨处于亚稳定态。石墨在触媒溶剂中溶解度大于金刚石,而溶解度的差异促使石墨向金刚石晶体转变。最终,金刚石在混合粉末中成核、生长。由于自发成核、生长条件不易控制等原因,很难利用这种方法获得大体积、高质量的金刚石晶体。
人类对事物的认识是一个循序渐进的过程,就像对金刚石的研究一样,通过它的性质研究它的组成,利用各种物理化学方法对其组成结构进行研究,知道其组成结构后,又探索各种制取金刚石的方法,以使金刚石广泛地被运用于生产生活中。

本作品为“科普中国-科学原理一点通”原创,转载时务请注明出处。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国