四氢呋喃,英文缩写为THF(Tetrahydrofuran),是一个杂环有机化合物。属于醚类,是芳香族化合物呋喃的完全氢化产物,是一种无色、可与水混溶、在常温常压下有较小粘稠度的有机液体。这种环状醚的化学式可写作(CH2)4O。由于它的液态范围很长,所以是一种常用的中等极性非质子性溶剂。它的主要用途是作高分子聚合物的前体。尽管THF的气味和化学性质与乙醚很相似,但是麻醉效果却很差。1
在世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考中,四氢呋喃在2B类致癌物清单中。2
命名和编号命名中文系统命名法:四氢呋喃1
中文同义词:1.4-环氧丁烷;四甲撑氧;氧杂环戊烷;一氧五环;四氢化氧杂茂;聚四甲基醚二醇1
英文名称:Tetrahydrofuran3
IUPAC命名法:oxolane3
国际化合物标识:InChI=1S/C4H8O/c1-2-4-5-3-1/h1-4H23
编号信息CAS编号:109-99-93
PubChem编号:80283
欧盟(EC)编号:203-726-83
NSC编号:578583
ICSC编号:05783
RTECS编号:LU59500003
UN编号:20563
UNII编号:3N8FZZ6PY43
DSSTox substance编号:DTXSID10213283
物化性质1.性状:无色易挥发液体,有类似乙醚的气味4
2.pH值:5(20%水溶液)4
3.熔点(℃):-108.54
4.沸点(℃):664
5.相对密度(水=1):0.894
6.相对蒸气密度(空气=1):2.54
7.饱和蒸气压(kPa):19.3(20℃)4
8.燃烧热(kJ/mol):-2515.24
9.临界温度(℃):2684
10.临界压力(MPa):5.194
11.辛醇/水分配系数:0.464
12.闪点(℃):-14℃3
13.自燃点(℃):3214
14.爆炸上限(%):11.84
15.爆炸下限(%):1.84
16.溶解性:溶于水、乙醇、乙醚、丙酮、苯等多数有机溶剂。4
17.折射率(n20ºC):1.40504
18.折射率(n25ºC):1.40404
19.黏度(mPa·s,0ºC):0.664
20.黏度(mPa·s,20ºC):0.554
21.黏度(mPa·s,30ºC):0.474
22.黏度(mPa·s,40ºC):0.424
23.蒸发热(KJ/kg,66ºC):4104
24.比热容(KJ/(kg·K),20ºC,定压,液体):1.964
25.比热容(KJ/(kg·K),60ºC,定压,气体):1.554
26.临界密度(g·cm-3):0.3224
27.临界体积(cm3·mol-1):2244
28.临界压缩因子:0.2594
29.偏心因子:0.2264
30.溶度参数(J·cm-3)0.5:19.1294
31.van der Waals面积(cm2·mol-1):6.000×1094
32.van der Waals体积(cm3·mol-1):44.6204
33.气相标准燃烧热(焓)(kJ·mol-1):-2533.164
34.气相标准生成热(焓)( kJ·mol-1) :-184.184
35.气相标准熵(J·mol-1·K-1) :302.414
36.气相标准生成自由能( kJ·mol-1):-81.14
37.气相标准热熔(J·mol-1·K-1):76.254
38.液相标准燃烧热(焓)(kJ·mol-1):-2501.074
39.液相标准生成热(焓)( kJ·mol-1):-216.274
40.液相标准熵(J·mol-1·K-1) :203.94
41.液相标准生成自由能( kJ·mol-1):-83.934
42.液相标准热熔(J·mol-1·K-1):123.94
结构二维结构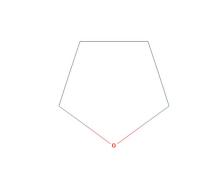
三维结构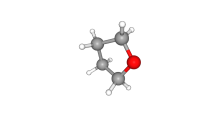
分子结构数据1、摩尔折射率:20.053
2、摩尔体积(cm3/mol):79.73
3、等张比容(90.2K):184.73
4、表面张力(dyne/cm):28.83
5、极化率(10-24cm3):7.943
计算化学数据1.疏水参数计算参考值(XlogP):无3
2.氢键供体数量:03
3.氢键受体数量:13
4.可旋转化学键数量:03
5.互变异构体数量:无3
6.拓扑分子极性表面积9.23
7.重原子数量:53
8.表面电荷:03
9.复杂度:22.83
10.同位素原子数量:03
11.确定原子立构中心数量:03
12.不确定原子立构中心数量:03
13.确定化学键立构中心数量:03
14.不确定化学键立构中心数量:03
15.共价键单元数量:13
作用与用途1、用作溶剂、有机合成的原料。1
2、用作色谱分析试剂、有机溶剂及尼龙66中间体。四氢呋喃又名一氧五环、氧杂环戊烷、四亚甲基氧,是合成农药苯丁锡的中间体,另外,可直接用于制合成纤维、合成树脂、合成橡胶,也是许多聚合材料、精密磁带和电镀工业的溶剂,还用于制己二腈、己二酸、己二胺、丁二酸、丁二醇、γ-丁内酯等,在医药工业上,可用于生产咳必清、黄体酮、利复霉素和用作制药溶剂等。1
3、四氢呋喃是一种重要的有机合成原料且是性能优良的溶剂,特别适用于溶解PVC、聚偏氯乙烯和丁苯胺,广泛用作表面涂料、防腐涂料、印刷油墨、磁带和薄膜涂料的溶剂,并用作反应溶剂,用于电镀铝液时可任意控制铝层厚度且光亮。四氢呋喃自身可缩聚(经阳离子引发开环再聚合)成聚四亚甲基醚二醇(PTMEG),也称四氢呋喃均聚醚。PTMEG与甲苯二异氰酸酯(TDI)制成耐磨、耐油、低温性能好、强度高的特种橡胶;与对苯二甲酸二甲酯和1,4-丁二醇制成嵌段聚醚聚酯弹性材料。相对分子质量为2000的PTMEG与对亚甲基双(4-苯基)二异氰酸酯(MDI)制成聚氨酯弹性纤维(氨纶,即SPANDEX纤维)、特种橡胶和一些特殊用途涂料的原料。在有机合成方面,用于生产四氢噻吩、1.2-二氯乙烷、2.3-二氯四氢呋喃、戊内酯、丁内酯和吡咯烷酮等。在医药工业方面,THF用于合成咳必清、利复霉素、黄体酮和一些激素药。THF经硫化氢处理生成四氢硫酚,可作燃料气中的臭味剂(识别添加剂)。THF还可用做合成革的表面处理剂。1
生产方法工业生产最早以糖醛为原料,将糖醛与蒸气的混合物通入填充锌-铬-锰金属氧化物(或钯)催化剂的反应器,于400-420℃脱去羰基而成呋喃;然后以骨架镍为催化剂,于80-120℃呋喃加氢制得四氢呋喃。该法生产1吨四氢呋喃,约需消耗3吨多糖醛。后来发展的生产方法有许多种,工业化的方法有1,4-丁二醇催化脱水环合法,因为丁二醇是由乙炔和甲醛制得的,此法称雷由法(Reppe法);利用氯丁橡胶单体氯丁二烯的副产物1,4-二氯丁烯生产四氢呋喃,称为二氯丁烯法;发展了以顺酐为原料的催化加氢法。四氢呋喃的生产工艺有以下5种:1
糠醛法:由糠醛脱羰基生成呋喃,再加氢而得。 这是工业上最早生产四氢呋喃的方法之一。糠醛主要由玉米芯等农副产品水解制造。该法污染严重,不利于大规模生产,已逐步被淘汰。1
顺酐催化加氢法:顺酐和氢气从底部进入内装镍催化剂的反应器,产物中四氢呋喃与γ-丁内酯比例可通过调整操作参数加以控制。反应产物与原料氢气冷却至50℃左右进入洗涤塔底部,使未反应的氢气及气态与液态产物分离,未反应的氢气及气态产物经洗涤后循环到反应器,液态产物经蒸馏而得四氢呋喃产品。该工艺可在0~(5∶1)范围内任意调整γ-丁内酯与四氢呋喃的比例,顺酐的单程转化率达100%,四氢呋喃选择性为85%~95%,产品含量达99.97%。该工艺具有催化剂性能好、流程简单、投资少等特点。1
1,4-丁二醇脱水环化法:其工艺过程为:向反应器中加入1087kg 22%的硫酸水溶液,在100℃以110kg/h的速度加入1,4-丁二醇,塔顶温度维持在80℃,以大约110kg/h的速度从塔顶得到含有80%四氢呋喃的水溶液。加入50t 1,4-丁二醇后,从反应器中排除约70kg焦质。将焦质进行过滤,得到的硫酸水溶液可以重新使用,这一过程的四氢呋喃收率可以达到99%以上。硫酸是四氢呋喃工业生产中使用最早的催化剂,也是现今生产中应用较多的催化剂。此工艺技术成熟,工艺比较简单,反应温度较低,四氢呋喃收率较高,但硫酸易腐蚀设备,污染环境。1
二氯丁烯法以1,4-二氯丁烯为原料,经水解生成丁烯二醇,再经催化加氢而得。1,4-二氯丁烯在氢氧化钠溶液中水解,110℃下生成丁烯二醇,离心分离去掉氯化钠,滤液在蒸发结晶器中浓缩,分离出碱金属羧酸盐,再在蒸馏塔中除去高沸物。将精制后的丁烯二醇送入反应器,以镍为催化剂,在80~120℃及一定压力下,丁烯二醇加氢生成丁二醇,蒸馏后进人环合反应器,在常压及120~140℃下于酸性介质中生成粗四氢呋喃,蒸馏脱水和脱高沸物,最后蒸馏得高纯四氢呋喃。此法操作简便,条件温和,收率高,催化剂用量少,可连续使用。1
丁二烯氧化法:以丁二烯为原料,经氧化得呋喃,再加氢而得。此法在国外已工业化。1
安全资料毒理学概述大鼠经口LD50:1650mg/kg;吸入LC50:21000ppm /3H.小鼠吸入LCLO:24000mg/m3/2H.低毒。该品对皮肤和粘膜有刺激作用。高浓度有麻醉作用,麻醉浓度与致死浓度相差不多。高剂量时尚有肝脏毒性。大鼠吸入590mg/m3,历3小时,眼睑及鼻粘膜发红,吸入>147750/m3,出现角膜水肿和混浊、溜延、流涕和鼻出血。大鼠、豚鼠、兔及猫在50mg/L浓度下3小时,部分动物侧倒;100mg/L下出现深度麻醉,部分动物在暴露1~4.5小时后死亡;200mg/L下1小时即出现麻醉,如长时间作用,可引起死亡。大鼠吸入浓度>14000mg/m3,出现睡眠,强直,进入深昏迷,抽搐,并有癫痫样脑电波。对麻醉作用,动物反复吸入后可出现耐受性。动物一次接触高剂量或反复接触,可出现肝脂肪浸润及细胞溶解。经口染毒,可引起胃出血和溃疡。20%水溶液直接涂于兔皮肤可引起中度皮肤刺激。50%水溶液可引起严重的腐蚀性损害,20%水溶液用于兔眼可引起严重的角膜炎。THF接触空气时形成爆炸过氧化物,可增加THF的刺激作用。国外报道引起人麻醉的浓度为73800mg/m3,人的嗅觉阈为88.5mg/m3。1
健康危害高浓度吸入后可出现头晕、头痛、胸闷、胸痛、咳嗽、乏力、胃痛、口干、恶心、呕吐等症状,可伴有眼刺激症状。部分患者可发生肝功能障碍。尿中THF浓度与环境中的THF浓度相关,还会流鼻血,可引起胃出血和溃疡;高剂量或反复接触,可出现肝脂肪浸润及细胞溶解。 20%水溶液直接涂于人皮肤可引起中度皮肤刺激,50% 水溶液可引起严重的腐蚀性损害。 20%水溶液用于人眼可引起严重的眼角膜损坏:长期接触会导致失去性功能、生育能力,或肾疾病!3
燃爆危险该品极度易燃,具刺激性。3
危险特性:其蒸气与空气可形成爆炸性混合物。遇高热、明火及强氧化剂易引起燃烧。接触空气或在光照条件下可生成具有潜在爆炸危险性的过氧化物。与酸类接触能发生反应。其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。3
有害燃烧产物:一氧化碳3
风险术语R11 高度易燃。3
R22吞食有害。3
R23/24/25吸入、皮肤接触及吞食有毒。3
R52/53对水生生物有害,可能对水体环境产生长期不良影响。3
R36/37/38刺激眼睛、呼吸系统和皮肤。3
使用注意事项呼吸系统防护:可能接触其蒸气时,应该佩戴过滤式防毒面具(半面罩)。必要时,建议佩戴自给式呼吸器。1
眼睛防护:一般不需要特殊防护,高浓度接触时可戴安全防护眼镜。1
身体防护:穿防静电工作服。v
手防护:戴防苯耐油手套。1
其它:工作现场严禁吸烟。工作毕,淋浴更衣。注意个人清洁卫生。1
应急处置皮肤接触:脱去被污染的衣着,用肥皂水和清水彻底冲洗皮肤。1
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。1
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。1
食入:饮足量温水,催吐,就医。1
灭火方法:喷水冷却容器,可能的话将容器从火场移至空旷处。处在火场中的容器若已变色或从安全泄压装置中产生声音,必须马上撤离。1
灭火剂:泡沫、干粉、二氧化碳、砂土。用水灭火无效。1
小量泄漏:用砂土或其它不燃材料吸附或吸收。也可以用大量水冲洗,洗水稀释后放入废水系统。1
大量泄漏:构筑围堤或挖坑收容。用泡沫覆盖,降低蒸气灾害。喷雾状水冷却和稀释蒸汽、保护现场人员、把泄漏物稀释成不燃物。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。1
注意事项操作注意事项:密闭操作,全面通风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴过滤式防毒面具(半面罩),戴安全防护眼镜,穿防静电工作服,戴橡胶耐油手套。远离火种、热源,工作场所严禁吸烟。使用防爆型的通风系统和设备。防止蒸气泄漏到工作场所空气中。避免与氧化剂、酸类、碱类接触。灌装时应控制流速,且有接地装置,防止静电积聚。搬运时要轻装轻卸,防止包装及容器损坏。配备相应品种和数量的消防器材及泄漏应急处理设备。倒空的容器可能残留有害物。1
储存注意事项:通常商品加有阻聚剂。储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。包装要求密封,不可与空气接触。应与氧化剂、酸类、碱类等分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。1
法规信息职业标准:TWA 590 毫克/立方米; STEL 640 毫克/立方米。4
化学危险物品安全管理条例 (1987年2月17日国务院发布),化学危险物品安全管理条例实施细则 (化劳发[1992] 677号),工作场所安全使用化学品规定 ([1996]劳部发423号)等法规,针对化学危险品的安全使用、生产、储存、运输、装卸等方面均作了相应规定;常用危险化学品的分类及标志 (GB 13690-92)将该物质划为第3.1 类低闪点易燃液体;车间空气中四氢呋南卫生标准 (GB 16231-1996),规定了车间空气中该物质的最高容许浓度及检测方法,但是国家标准委于2017年3月下文将这项强制性国家标准转化为推荐性国家标准。5
本词条内容贡献者为:
包申旭 - 教授 - 武汉理工大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国