游离脂肪酸,简称:FFA,存在于人体内的脂质,大致可以分为胆固醇、中性脂肪(三酸甘油脂)、磷脂质等3种。游离脂肪酸是中性脂肪分解成的物质。当肌肉活动所需能源--肝糖耗尽时,脂肪组织会分解中性脂肪成为游离脂肪酸来充当能源使用。所以,游离脂肪酸可说是进行持久活动所需的物质。
介绍简称:FFA,NEFA
英文名:nonestesterified fatty acid;free fatty acid
游离脂肪酸又称非酯化脂肪酸(nonestesterified fatty acid NEFA),血清中含量很少,如用小量血清标本测定必须采用灵敏的方法,并要避免脂肪水解产生的脂肪酸的干扰。
NEFA是由油酸,软脂酸,亚油酸等组成,大部分游离脂肪酸与白蛋白结合,存在于血液中。
血清中游离脂肪酸的浓度与脂类代谢、糖代谢、内分泌功能有关,游离脂肪酸的浓度会因为糖尿病、重症肝障碍、甲状腺功能亢进等疾病而上升。
正常值:0.3~0.9mmol/L
功能¤ 热量的直接来源:游离脂肪酸是中性脂肪分解成的物质。当肌肉活动所需能源--肝醣耗尽时,脂肪组织会分解中性脂肪成为游离脂肪酸来充当能源使用。所以,游离脂肪酸可说是进行持久活动所需的物质。例如:马拉松赛跑。
是导致氧化应激的物质之一:
高游离脂肪酸(FFA)刺激的后果是高活性反应分子性氧簇(ROS)和活性氮簇 (RNS)生成增多,从而启动了氧化应激机制(高活性反应分子产生和抗氧化作用之间长期失衡而引起组织损伤)。这些活性分子可直接氧化和损伤DNA、蛋白质、脂类,还可作为功能性分子信号,激活细胞内多种应激敏感信号通路,这些信号通路与胰岛素抵抗和β细胞功能受损密切相关。
胰岛素抵抗可以先于糖尿病发生,在其作用下,疾病早期胰岛素代偿性分泌增加以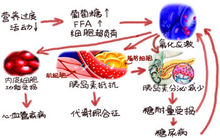 保持正常糖耐量。当胰岛素抵抗增强、胰岛素代偿性分泌减少或二者共同出现时,疾病逐渐向糖耐量减退和糖尿病进展,血糖开始升高。高血糖和高FFA共同导致ROS大量生成和氧化应激,也激活应激敏感信号途径,从而又加重胰岛素抵抗,临床上表现为糖尿病持续进展与恶化。体外研究显示,ROS和氧化应激可引起多种丝氨酸激酶激活的级联反应。最近的抗氧化剂改善血糖控制试验也证实,ROS和氧化应激会引起胰岛素抵抗
保持正常糖耐量。当胰岛素抵抗增强、胰岛素代偿性分泌减少或二者共同出现时,疾病逐渐向糖耐量减退和糖尿病进展,血糖开始升高。高血糖和高FFA共同导致ROS大量生成和氧化应激,也激活应激敏感信号途径,从而又加重胰岛素抵抗,临床上表现为糖尿病持续进展与恶化。体外研究显示,ROS和氧化应激可引起多种丝氨酸激酶激活的级联反应。最近的抗氧化剂改善血糖控制试验也证实,ROS和氧化应激会引起胰岛素抵抗
脂质的成份¤ 存在于人体内的脂质(lipid),大致可以分为胆固醇、中性脂肪(三酸甘油脂)、磷脂质、游离脂肪酸等4种。
胆固醇的功能:
¤ 胆固醇是肝脏代谢脂肪时的合成物质。
¤ 构成细胞膜的原料:胆固醇、磷脂质及蛋白质是构成细胞膜的主要原料。
¤ 构成各种荷尔蒙的原料:肾上腺荷尔蒙、性荷尔蒙等。
¤ 构成胆汁酸的原料。
¤ 胆汁酸在食物进入人体后,能够乳化脂肪,让食物变得容易分解。
中性脂肪(三酸甘油脂)的功能:
¤ 由食物摄取而来的中性脂肪,会先被分解成脂肪酸和甘油,再由小肠吸收,之后,又被合成为中性脂肪,然后经由淋巴管,储存在脂肪细胞中。
¤ 热量的来源:中性脂肪是一种甘油物质,是与3个脂肪酸相连的构造。中性脂肪被酵素分解成脂肪酸(游离脂肪酸),就可以成为热量的来源。
¤ 保温及缓冲的作用:中性脂肪常屯积在皮下、肌肉组织间及脏器的周围,可以让身体保持一定的温度,也可以保护内脏,减少外来压力的伤害。
磷脂质的功能:
¤ 构成细胞膜的原料:磷脂质是磷与脂肪酸的化合物,它和胆固醇、蛋白质都是构成细胞膜的主要原料。尤其在脑和神经细胞含量特别多。
¤ 帮助物质进出细胞:可以将难溶於水的物质变成易溶於水的物质,例如:电解质、葡萄糖。
医学检查化验取材血液
化验方法脂类测定
化验类别血液生化检查 > 脂类测定
试剂以Boehringer mannheim游离脂肪酸测定试剂盒为例:
(1)缓冲液Ⅰ:0.2mol/L pH7.5 KH2PO4(用5mol/L KOH调pH)。
(2)81mol/L ATP溶液:125mg ATP溶于2.5ml缓冲液Ⅰ中。
(3)10mmol/L MgCl2溶液。
(4)10mmol/L pH6.5辅酶A溶液。
(5)50g/L Triton X-100溶液。
(6)酰基辅酶A合成酶 8.4ku/L(用缓冲液Ⅰ配制)。
(7)2-(N-吗啉代)乙烷磺酸(2-morpholi-noethanesulphonic acid,MES)缓冲液:0.2mol/L,pH7.5(用KOH调pH)。
(8)N-乙基顺丁烯二酰亚胺(N-ethylmaleimide,NEM),20mmol/L(用MES缓冲液配制)。
(9)4-氨基安替比林溶液,15mmol/L(用MES缓冲液配制)。
(10)2,4,6-三溴-3-羟基苯甲酸(TBHB)溶液60mmol/L(用MES缓冲液配制)。
(11)过氧化物酶溶液,2000u/ml。
(12)1g/L NaN3溶液
(13)酰基辅酶A氧化酶溶液:约120u/ml(用缓冲液Ⅰ配制)。
操作方法(1)混合试剂:
①试剂Ⅰ:含缓冲液Ⅰ 4.0ml、ATP 2.0ml、MgCl2 2.0ml、辅酶A 2.0ml、TritonX-100 4.0ml、酰基辅酶A合成酶2.0ml,加双蒸水4.5ml(共20.5ml)。
②试剂Ⅱ:含MES缓冲液10.0ml、4-氨基安替比林6.0ml、TBHB 8.0ml、NaN3溶液2.0ml、TritonX-100 4.0ml、过氧化物酶溶液0.4ml,双蒸水10.0ml(共40.4ml)。
③试剂Ⅲ:NEM缓冲液2.1ml、酰基辅酶A氧化酶2.0ml(共4.1ml)。
上述三种混合试剂4℃避光保存可稳定3天。
(2)各管内加入试剂Ⅰ1ml与试剂Ⅱ2ml,混合,37℃10min。
(3)加入空白与血清标本各50μl,混合后37℃5min,在546nm测定吸光度为A1。
(4)加入试剂Ⅲ 0.20ml,混合,待20~25min反应停止后在546nm测定吸光度为A2。
正常值酶法(37℃):400~900μmol/L。
临床意义(1)升高:糖尿病、糖原累积病、甲状腺功能亢进症、褐色细胞瘤、肢端肥大症、巨人症、库欣综合征、重症肝损害、心肌梗死、妊娠后期、阻塞性黄疸、肝炎、肝硬化、血色病等。1
(2)降低:甲状腺功能减低症、艾迪生病、胰岛细胞瘤、脑垂体功能减退症、降糖药或胰岛素使用过量等。
附注若血清游离脂肪酸浓度大于2mmol/L可适当稀释后再测。
相关疾病
艾迪生病、肝硬化、黄疸、甲状腺功能亢进症、巨人症、库欣综合征、糖尿病、糖原累积病、血色病、肢端肥大症
临床意义NEFA与氧化应激
氧化应激:氧化应激是指机体在遭受各种有害刺激时,自由基的产生和抗氧化防御之间严重失衡,从而导致组织损伤
氧化应激与糖尿病
氧化应激与糖尿病:糖尿病是以胰岛素分泌缺陷和(或)胰岛素抵抗导致的一组以慢性高血糖为特征的代谢性疾病。氧化应激可通过损伤胰岛! 细胞和降低外周组织对胰岛素的敏感性,导致糖尿病的发生。
游离脂肪酸与心血管疾病游离脂肪酸(free fatty acids, FFA)是指非酯化的脂肪酸。血中的 FFA 主要是脂肪代谢的中间产物,是机体细胞能量代谢的重要代谢底物,为心脏、肝脏、骨骼肌等器官代谢提供能量。有大量研究显示,过高的游离脂肪酸导致的高游离脂肪酸血症与代谢综合征、动脉粥样硬化、急性冠脉综合征、心力衰竭等疾病的发生发展相关。
游离脂肪酸与动脉粥样硬化动脉粥样硬化的发病机制有多种学说,现大多数学者支持" 内皮损伤反应学说 ",认为各种危险因素都是最终作用于损伤的内皮细胞,动脉硬化病变的形成是动脉对损伤内膜形成炎症 - 纤维反应增生的结果。游离脂肪酸参与了动脉粥样硬化形成过程中的炎症反应及内皮功能的损伤。
游离脂肪酸与高血压高血压是常见病、多发病也是心脑血管疾病的危险因素。虽然原发性高血压的病因尚不十分清楚,但其中可能存在的机制及相关危险因素已有了长足的研究进展。现多个试验及研究显示,游离脂肪酸升高与高血压发病有明显相关性:有国外临床实验研究显示,血浆游离脂肪酸浓度升高与高血压发病有明显相关性,并且,可通过检测血浆空腹游离脂肪酸浓度和餐后两小时游离脂肪酸浓度,作为预测高血压发病的危险因素,对高血压发病有提示及预警意义。还有研究显示,在去除体重指数等全身营养状态相关影响后,高血压患者与健康对照组相比,前者血浆游离脂肪酸浓度明显升高。还有国内研究显示,新发高血压者基础空腹血清 FFA 组成显著改变,表现为饱和脂肪酸水平显著增高。2
有研究显示,高游离脂肪酸血症可能通过以下机制引起肥胖个体血压升高: (1) 削弱内皮依赖性血管舒张;血 FFA 浓度增高引起血管内皮细胞功能障碍可能机制有:①引起胰岛素刺激的内皮依赖性血管扩张(IMV)削弱;②通过改变影响血流剪切力大小及神经递质如乙酰胆碱等释放从而导致血管舒缩功能;③氧化应激反应(2)影响植物神经系统功能,现研究表明,游离脂肪酸通过α 受体增强交感神经敏感性,最终导致高血压发病率增高(3)影响血流动力学稳定性(4)影响平滑肌细胞功能,国内外大量基础研究表明,游离脂肪酸可诱导平滑肌细胞膜钙离子通道数量上调,增加血钙敏感度,管壁张力增高;蛋白激酶 C(PKC)信号转导通路在血管平滑细胞增殖、迁移中发挥枢纽作用,游离脂肪酸也可(5)引起高胰岛素血症。可见,高游离脂肪酸血症与高血压的发生发展密切相关,现正尝试通过改善脂肪酸代谢的途径干预高血压的发生发展。
游离脂肪酸与冠心病冠状动脉粥样硬化性心脏病 (coronary atherosclerotic heartdisease CHD)是指冠状动脉粥样硬化使血管狭窄或阻塞,或(和)因血管功能性改变(痉挛)导致心肌细胞缺血缺氧或坏死而引起的心脏病。动脉粥样硬化(atherosclerosis,AS)是冠心病的发病基础。高游离脂肪酸血症可通过破坏内皮细胞、参与血状态下的心肌损伤。是需要干预的冠心病独立危险因素。
游离脂肪酸与心力衰竭心力衰竭是各种心脏疾病终末期后出现的以心脏射血不足为主要表现的一组临床综合征。随着心血管疾病发病率的逐年增高及急性心梗等血管再通治疗的有效性,心力衰竭的发病率正逐渐增加。游离脂肪酸为心肌的能量底物,与心衰患者心肌能量代谢的改变密切相关。2
国内外专家针对调节脂肪酸代谢从而改变心肌能量代谢的治疗已做了不少尝试。其中包括;
①降低血中游离脂肪酸浓度。但就目前的研究显示,单纯降低血浆游离脂肪酸浓度,对于心衰患者心肌能量代谢改善的作用不确切。其中代表药物为阿昔莫司。阿昔莫司是一种抗酯化的调脂药。其可以抑制脂肪组织释放游离脂肪酸。有国外研究,分别给予缺血性心衰患者及扩张性心肌病心衰患者阿昔莫司口服治疗,虽然可显著降低血浆游离脂肪酸水平,但在患者胰岛素抵抗、心肌收缩功能或运动耐量、血管舒张功能、心脏指数等方面均未见明显改善。
②抑制脂肪酸进入心肌线粒体。调节 FFA 进入线粒体的过程的关键酶是:肉碱脂酰转移酶 -1。现针对抑制肉碱脂酰转移酶-1,从而抑制 FFA 进入心肌线粒体的药物试验取得了一定进展。其中哌克西林能特异地抑制心脏的肉碱脂酰转移酶 -1 活性。有研究显示:给予非梗阻性肥厚型心肌病患者哌克昔林治疗,发现哌克昔林能够显著提高心衰患者的运动耐量,减少心衰症状的发作,通过改善心脏的舒张功能,,改善心衰相关临床症状。此外,另一种可以抑制肉碱脂酰转移酶 -1 药物乙莫克舍能显著改善心衰患者临床症状,使左室射血分数增加。然而,可惜的是,随后的大型随机双盲临床试验因为它的肝毒性而提前终止。
本词条内容贡献者为:
张磊 - 副教授 - 重庆师范大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国