神经干细胞(neural stem cell)是指存在于神经系统中,具有分化为神经神经元、星形胶质细胞和少突胶质细胞的潜能,从而能够产生大量脑细胞组织,并能进行自我更新,并足以提供大量脑组织细胞的细胞群。1
是一类具有分裂潜能和自更新能力的母细胞,它可以通过不对等的分裂方式产生神经组织的各类细胞。需要强调的是,在脑脊髓等所有神经组织中,不同的神经干细胞类型产生的子代细胞种类不同,分布也不同。
细胞分类根据分化潜能及产生子细胞种类不同分类
1)神经管上皮细胞
分裂能力最强,只存在胚胎时期,可以产生放射状胶质神经元和神经母细胞。
2)放射状胶质神经元
可以分裂产生本身并同时产生神经元前体细胞或是胶质细胞,主要作用是幼年时期神经发育过程中产生投射神经元完成大脑中皮质及神经核等的基本神经组织细胞。
3)神经母细胞
成年人体中主要存在的神经干细胞,分裂能力可以产生神经前体细胞和神经元和各类神经胶质细胞。
4)神经前体细胞
各类神经细胞的前体细胞,比如小胶质细胞是由神经胶质细胞前体产生的。
根据部位分类
神经嵴干细胞(neural crest stemcell,NC-SC)和中枢神经干细胞(CNS-SC)。
外周神经干细胞(PNS-SC),既可发育为外周神经细胞、神经内分泌细胞和Schwann氏细胞,也能分化为色素细胞(pigmented cell)和平滑肌细胞等。NSC一般是指存在于脑部的中枢神经干细胞(CNS-SC),其子代细胞能分化成为神经系统的大部分细胞。
以往认为,中枢神经系统的神经元在出生前或出生后不久,就失去再生能力。但近年的一些研究表明,成年哺乳动物的脑组织仍可不断产生新的神经元,成人脑组织中同样存在NSC,主要是在侧脑室下层(SVZ)和海马齿状回两处。
目前多使用基因转移的方法,建立神经干细胞系,即诱导NSC的细胞周期不断循环往复,从而阻止其分化过程。永生化的NSC具有较好的生物学特性,它们能自我复制并在体外大量增殖,在移植人体内后仍具有多向分化潜能,同时可被转染并稳定地表达外源基因。
长期以来,人们一直认为成年哺乳动物脑内神经细胞不具备更新能力,一旦受损乃至死亡不能再生。这种观点使人们对中枢神经系统疾病的治疗受到了很大限制。虽然传统的药物、手术及康复治疗取得了一定的进展,但是仍不能达到满意的效果。
1992年,Reynolds等2从成年小鼠脑纹状体中分离出能在体外不断分裂增殖,且具有多种分化潜能的细胞群,并正式提出了神经干细胞的概念,从而打破了认为神经细胞不能再生的传统理论。Mckay于1997年在《Science》杂志上将神经干细胞的概念总结为:具有分化为神经元、星形胶质细胞及少突胶质细胞的能力,能自我更新并足以提供大量脑组织细胞的细胞。
细胞特点自我更新 神经干细胞具有对称分裂及不对称分裂两种分裂方式,从而保持干细胞库稳定。
神经干细胞具有对称分裂及不对称分裂两种分裂方式,从而保持干细胞库稳定。
多向分化神经干细胞可以向神经元、星形胶质细胞和少突胶质细胞分化。
免疫源神经干细胞是未分化的原始细胞,不表达成熟的细胞抗原,不被免疫系统识别。
组织融合性可以与宿主的神经组织良好融合,并在宿主体内长期存活。
治疗机理1、患病部位组织损伤后释放各种趋化因子,可以吸引神经干细胞聚集到损伤部位,并在局部微环境的作用下分化为不同种类的细胞,修复及补充损伤的神经细胞。由于缺血、缺氧导致的血管内皮细胞、胶质细胞的损伤,使局部通透性增加,另外在多种黏附分子的作用下,神经干细胞可以透过血脑屏障,高浓度的聚集在损伤部位;
2、神经干细胞可以分泌多种神经营养因子,促进损伤细胞的修复。
3、神经干细胞可以增强神经突触之间的联系,建立新的神经环路。
细胞移植传统的药物治疗效果不令人满意,吃药只可暂时性的控制疾病,一旦停药,病症复现甚至更严重。常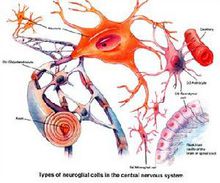 年服药不仅让患者痛苦不已,而且对身体造成极大的危害,导致 其他严重疾病的并发。药物不具备激活脑神经细胞的功能是根本原因,所以要想从根本上治疗脑病等神经系统疾病,借助外界移植神经干细胞是唯一有效的方法。
年服药不仅让患者痛苦不已,而且对身体造成极大的危害,导致 其他严重疾病的并发。药物不具备激活脑神经细胞的功能是根本原因,所以要想从根本上治疗脑病等神经系统疾病,借助外界移植神经干细胞是唯一有效的方法。
科学研究证明了神经干细胞的定向分化性,使修复和替代死亡的神经细胞成为现实。为了减少神经损伤的后遗症,延缓或抑止疾病的进一步发展,取得更好的恢复效果,从根本上修复和激活死亡神经细胞是十分必要的。
NSC是一群能自我更新并具有多种分化潜能的细胞,它来源于神经组织并可生成神经组织,在适当条件下可分化成神经元、少突胶质细胞和星形细胞。以往的观点认为,成年哺乳动物CNS(中枢)的神经再生非常有限,而且随着年龄的增长,神经元数量会逐渐减少。然而近20年的研究表明,成年哺乳动物CNS(中枢神经系统)内仍然存在神经发生。目前已明确的部位有海马齿状回、室管膜下区 [2,3] 。已有研究发现,在缺血缺氧条件下位于室管膜下区、海马和脉络膜丛等部位的内源性NSC可发生增殖、迁移并分化为神经元和神经胶质细胞,因而提示中枢神经系统可通过自身内源性干细胞来修复,只是由于条件不足而没有足够的新生细胞。最近的研究证实,这些原始NSC数量稀少,且处于静止状态,缺乏特异性形态、表面标志和分化抗原,至今也不能高度纯化分离,很难克隆化4]。因此,外源性NSC移植提供给我们一个大胆的新思路。许多研究表明,NSC移植物在宿主CNS内具有明显的生存、迁移和分化能力,由人胎脑分离的NSC在植入胚胎或新生鼠脑内后,表现为在宿主脑内迁移并进行区域特异性分化,若将相同的人胎脑NSC植入成年大鼠室管膜下区,它们沿吻侧迁移流迁移入嗅球,分化为双极神经元,其分化命运与存留于室管膜下区的内源性NSC相同 [5]。从成年哺乳动物CNS分离的NSC也具有较强的分化潜能,而决定NSC分化命运的主要因素除局部微环境外,还包括NSC的内在特性。如成年动物脊髓NSC植入海马齿状回,能分化为神经元;若植入成年大鼠脊髓则不分化为神经元 [6] ;将从成年动物海马齿状回获得的NSC 植入成年大鼠室管膜下区或迁移流后,能分化为嗅球神经元;若植入成年大鼠海马,则产生新的海马神经元 [7,8] 。无论胚胎或成人NSC,在移植入成人CNS非神经发生区后大部分都分化成神经胶质细胞。外源性CSN移植取得了令人鼓舞的成果。Modo等 [9] 给局灶性缺血大鼠移植MHP36鼠干细胞,结果表明,移植的干细胞可增殖分化成神经元细胞,并能显著促进神经功能恢复;Zhang等 [10] 的研究发现,静脉注射骨髓间质细胞可进入脑梗死后的脑实质,并促进新生血管形成。进一步的研究表明,移植的干细胞和骨髓间质细胞可通过分泌生长因子促进内源性神经元再生,促使神经功能恢复。于炳新等 [11] 给局灶性脑缺血大鼠注射重组人粒细胞集落刺激因子,动员自体骨髓造血干细胞。结果表明,脑实质内表达SYN和MAP-2蛋白的增殖细胞显著增加,神经功能缺损明显改善。因此认为,除通过骨髓间质细胞机制外,同时也可能存在骨髓干细胞脑实质内转移,但尚待进一步的研究。
植入成年大鼠室管膜下区或迁移流后,能分化为嗅球神经元;若植入成年大鼠海马,则产生新的海马神经元 [7,8] 。无论胚胎或成人NSC,在移植入成人CNS非神经发生区后大部分都分化成神经胶质细胞。外源性CSN移植取得了令人鼓舞的成果。Modo等 [9] 给局灶性缺血大鼠移植MHP36鼠干细胞,结果表明,移植的干细胞可增殖分化成神经元细胞,并能显著促进神经功能恢复;Zhang等 [10] 的研究发现,静脉注射骨髓间质细胞可进入脑梗死后的脑实质,并促进新生血管形成。进一步的研究表明,移植的干细胞和骨髓间质细胞可通过分泌生长因子促进内源性神经元再生,促使神经功能恢复。于炳新等 [11] 给局灶性脑缺血大鼠注射重组人粒细胞集落刺激因子,动员自体骨髓造血干细胞。结果表明,脑实质内表达SYN和MAP-2蛋白的增殖细胞显著增加,神经功能缺损明显改善。因此认为,除通过骨髓间质细胞机制外,同时也可能存在骨髓干细胞脑实质内转移,但尚待进一步的研究。
细胞应用细胞因子与神经干细胞的增殖、分化密切相关。不同的细胞因子在神经干细胞的诱导分化中起重要作用,但尚没有一种细胞因子能在体外将神经干细胞全部诱导分化为所需的功能神经细胞,参与神经干细胞诱导分化的细胞因子有白细胞介素类,如IL-1、IL-7、IL-9及IL-11等。神经营养因子对神经干细胞分化到终末细胞的整个过程均有影响,如果将培养的神经干细胞置于脑源性神经营养因子作用下,大量的神经干细胞可 以表现出分化神经元的特性。生长因子类,如上皮生长因子、神经生长因子及碱性成纤维细胞生长因子等也影响神经干细胞的分化。神经干细胞对不同种类、不同浓度的因子,以及多种因子联合应用作用各不相同,在神经干细胞发育分化的不同阶段,相同因子的作用也不同。如在表皮生长因子及碱性成纤维细胞生长因子存在的条件下,胚胎神经干细胞主要向神经元、星形胶质细胞和少突胶质细胞分化,而出生后及成年的脑神经干细胞,则无论是否有上皮生长因子及碱性成纤维细胞生长因子,都主要分化为星形胶质细胞。这些研究提示,上皮生长因子及碱性成纤维细胞生长因子对神经干细胞向功能细胞的诱导分化是复杂的。
以表现出分化神经元的特性。生长因子类,如上皮生长因子、神经生长因子及碱性成纤维细胞生长因子等也影响神经干细胞的分化。神经干细胞对不同种类、不同浓度的因子,以及多种因子联合应用作用各不相同,在神经干细胞发育分化的不同阶段,相同因子的作用也不同。如在表皮生长因子及碱性成纤维细胞生长因子存在的条件下,胚胎神经干细胞主要向神经元、星形胶质细胞和少突胶质细胞分化,而出生后及成年的脑神经干细胞,则无论是否有上皮生长因子及碱性成纤维细胞生长因子,都主要分化为星形胶质细胞。这些研究提示,上皮生长因子及碱性成纤维细胞生长因子对神经干细胞向功能细胞的诱导分化是复杂的。
信号转导在神经干细胞分化中十分重要。作为一种信号传导途径,Notch信号传导系统尚未完全阐明。认为Notch受体是一种整合型膜蛋白,是一个保守的细胞表面受体,它通过与周围配体接触而被激活,其信号传导途径开始于Notch受体与配体结合后其胞浆区从细胞膜上脱落,并向细胞核转移,将信号传递给下游信号分子。该途径的信号传递主要是通过蛋白质相互作用,引起转录调节因子的改变或将转录调节因子结合到靶基因上,实现对特定基因转录的调控。当激活Notch途径时,干细胞进行增殖,当抑制Notch活性时,干细胞进入分化程序。这些研究结果表明找到调节Notch信号途径的方式,就可能通过改变Notch信号来精确调控神经干细胞向神经功能细胞分化的过程和比例。此外,Janus激酶信号转导递质与转录激活剂(JAK-STAT)信号传导系统也参与干细胞的调控。
神经干细胞的应用:神经干细胞在神经发育和修复受损神经组织中发挥重要作用。神经干细胞移植是修复和代替受损脑组织的有效方法,能重建部分环路和功能。此外神经干细胞可作为基因载体,用于颅内肿瘤和其它神经疾病的基因治疗,利用神经干细胞作为基因治疗载体,弥补了病毒载体的一些不足。Wagner等将神经干细胞移植到帕金森病模型的鼠脑,神经干细胞在其脑组织中迁移并修复损毁的脑组织,且震颤症状明显减轻,可能是神经干细胞分化成为多巴胺能神经元起到治疗作用。Piccini等从流产胎儿脑中分离的神经组织细胞,移植入患者的脑中治疗帕金森病,结果有一半以上的患者症状得到明显改善,而且效果持续存在。多发性硬化是发病率较高的神经系统疾病,在其啮齿类动物模型中发现产生髓鞘的少突胶质细胞被破坏或失去功能,将神经干细胞直接移植到鼠脑中,移植的细胞在脑中发生了大范围的迁移,在分化成的少突胶质细胞中,约40%的细胞形成了髓鞘,其特性非常接近正常状态,一些接受移植的动物其典型的症状也得到了明显的改善。脑胶质瘤是医学治疗的难点之一,手术切除肿瘤困难,且容易复发,放疗和化疗对肿瘤有一定的作用。由于神经干细胞具有迁移的功能,利用这种特性可以向脑部释放药物。对鼠神经干细胞进行转基因处理,使之分泌IL-4,这种物质能够激活免疫系统,对肿瘤细胞发生抗瘤攻击,患有脑胶质瘤的实验鼠接受这种细胞注射之后,寿命比未治疗的实验鼠大大延长,核磁共振成像表明,实验鼠脑部的大块肿瘤有缩小的迹象,有趣的是,即使注射的神经干细胞不分泌IL-4,实验鼠的寿命也会延长。Ling等认为这是由于神经干细胞还能分泌一种能够减缓肿瘤细胞分裂的未知物质的缘故。此外,神经干细胞对于判断药效及药物毒性等也有一定实用价值,如可以利用神经干细胞培养技术观察某些天然化合物和合成化合物的神经活性,为发展小分子治疗药物提供理论基础。
神经干细胞应用中存在的问题:建立的神经干细胞系绝大多数来源于鼠,而鼠与人之间存在着明显的种属 差异;神经干细胞的来源不足;部分移植的神经干细胞发展成脑瘤;神经干细胞转染范围的非选择性表达及转染基因表达的原位调节;利用胚胎干细胞代替神经干细胞存在着社会学及伦理学方面的问题等。(神经干细胞系的建立可以无限地提供神经元和胶质细胞,解决了胎脑移植数量不足的问题,同时避免了伦理学方面的争论,为损伤后进行代替治疗提供了充足的种子细胞)。
差异;神经干细胞的来源不足;部分移植的神经干细胞发展成脑瘤;神经干细胞转染范围的非选择性表达及转染基因表达的原位调节;利用胚胎干细胞代替神经干细胞存在着社会学及伦理学方面的问题等。(神经干细胞系的建立可以无限地提供神经元和胶质细胞,解决了胎脑移植数量不足的问题,同时避免了伦理学方面的争论,为损伤后进行代替治疗提供了充足的种子细胞)。
神经干细胞的来源、分离、培养及鉴定还有许多工作要做,神经干细胞诱导、分化及迁移机制有待进一步研究。通过细胞培养技术及基因组的研究,如DNA微列阵技术,进一步明确成体神经干细胞的确切位置,可以设计药物特异性地激活这些细胞。进一步认识神经干细胞的本质和控制分化基因,通过调控靶基因,可以从神经干细胞诱导产生特定的分化细胞来满足各种需要。横向分化的发现对神经干细胞的研究和应用具有重要意义,人们可望从自体中分离诱导出神经干细胞,有可能解决神经干细胞的来源问题,神经干细胞的应用将有广阔的前景。
本词条内容贡献者为:
李少斌 - 副教授 - 长江大学生命科学学院




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国