分离压是薄液膜中由于分子作用力产生的额外的压力。分离压的物理定义为是单位面积吉布斯能关于距离的导数。分离压的概念最早由Derjaguin引入。在薄膜蒸发中,分离压的概念得到广泛应用。
简介分离压是薄液膜中由于分子作用力产生的额外的压力。分离压的物理定义为是单位面积吉布斯能关于距离的导数。分离压的概念最早由Derjaguin引入。在薄膜蒸发中,分离压的概念得到广泛应用。1
吉布斯能在热力学里,吉布斯能(Gibbs能),又称吉布斯自由能、吉布斯函数、自由焓,常用英文字母“G”标记。吉布斯能是国际化学联会建议采用的名称。吉布斯能是描述系统的热力性质的一种热力势,定义为
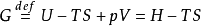 其中,U是系统的内能,T是绝对温度,S是熵,p是压强,V是体积,H是焓。
其中,U是系统的内能,T是绝对温度,S是熵,p是压强,V是体积,H是焓。
假设在等温等压状况下,一个热力系统从良好定义初态变换到良好定义终态,则其吉布斯能减少量必定大于或等于其所做的非体积功;假若这变换是可逆过程,则其吉布斯能减少量等于其所做的非体积功。所以,这热力系统所能做的最大非体积功是其吉布斯减少量。
在等温等压状况下,一个热力过程具有自发性的必需条件为,吉布斯能随着过程的演化而减小。这意味着,平衡系统的吉布斯能是最小值;在平衡点,吉布斯能对于其它自变量的导数为零。
吉布斯能可以用来评估一个反应是否具有自发性,它可以用来估算一个热力系统可以做出多少非体积功。当应用热力学于化学领域时,吉布斯能是最常用到与最有用的物理量之一。吉布斯能是为纪念美国物理学者约西亚·吉布斯而命名。1
表面张力在物理上,表面张力(英语:Surface Tension),狭义的定义是指液体试图获得最小表面位能的倾向;广义地说,所有两种不同物态的物质之间界面上的张力被称为表面张力。表面张力最常见的例子发生在液体与其他物质的接触面。以水为例,水的表面张力来自于由凡得瓦力所造成的内聚力。当固体,如水黾,跑到水上时,表面张力会尽可能将水面维持平整的状态,以达到最小表面位能。如果水黾的重量维持在限度以内,那么水面将只会有少许凹陷,这就是水黾能够在水面上活动的原理。1
相关表面张力
本词条内容贡献者为:
胡建平 - 副教授 - 西北工业大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国