厌氧氨氧化工艺是1990年荷兰Delft技术大学Kluyver生物技术实验室开发的。该工艺突破了传统生物脱氮工艺中的基本理论概念。在厌氧条件下,以氨为电子供体,以硝酸盐或亚硝酸盐为电子受体,将氨氧化成氮气,这比全程硝化(氨氧化为硝酸盐)节省60%以上的供氧量。以氨为电子供体还可节省传统生物脱氮工艺中所需的碳源。1
简介在传统的生物脱氮工艺中,氮的去除是通过硝化与反硝化两个独立的过程实现的。传统理论认为,进行硝化与反硝化的细菌种类和所需环境条件都不同,硝化细菌主要以自养菌为主,需要环境中有较高的溶解氧;而反硝化细菌与之相反,以异养菌为主,适宜生长于缺氧环境。所以很难设想能在同一反应器中同时实现硝化与反硝化两个过程。然而,有不少研究和实践证明,在各种不同的生物处理系统中存在有氧条件下的反硝化现象。研究还发现一些与传统脱氮理论有悖的现象,如硝化过程可以有异养菌参与、反硝化过程可在好氧条件下进行、NH4可在厌氧条件下转变成N2等。这些研究的结果,导致了不少脱氮新工艺的诞生。厌氧氨氧化工艺是1990年荷兰Delft技术大学Kluyver生物技术实验室开发的。该工艺突破了传统生物脱氮工艺中的基本理论概念。在厌氧条件下,以氨为电子供体,以硝酸盐或亚硝酸盐为电子受体,将氨氧化成氮气,这比全程硝化(氨氧化为硝酸盐)节省60%以上的供氧量。以氨为电子供体还可节省传统生物脱氮工艺中所需的碳源。同时由于厌氧氨氧化菌细胞产率远低于反硝化菌,所以,厌氧氨氧化过程的污泥产量只有传统生物脱氮工艺中污泥产量的15%左右。1
机理Van de Graaf等人通过同位素示踪研究表明,氨被微生物氧化时,羟氨最有可能作为电子受体,而羟基本身又是由NO2分解而来,其反应的可能途径如图1所示。
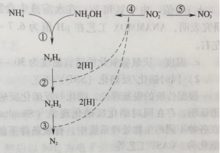
氨厌氧氧化涉及的反应如下:
NH2OH+NH3→N2H4+H2O
N2H4→N2+4[H]
HNO2+4[H]→NH2OH+H2O
NH3+HNO2→N2+2H2O
HNO2+H2O+NAD→HNO3+NADH2
厌氧氨氧化涉及的是自氧菌,反应过程无需添加有机物。Jetten等人从ANAMMOX工艺的反硝化流化床反应器中分离并取得了ANAMMOX菌,经富集培养后获得了一种优势自氧菌,该优势菌种为一种具有不规则球状的革兰氏阴性菌,颜色呈红色。Jetten等人和Van de Graaf等人认为,好氧氨氧化菌在厌氧氨氧化过程中所起的作用不大,在厌氧条件下它们最大的氨氧化速率仅为2mol/(min·mg蛋白质);而厌氧氨氧化菌的最大氨氧化速率可达55nmol/(min·mg蛋白质),但是这种厌氧氨氧化细菌的比生长速率非常低,仅为0.003h-1,即其倍增时间为11d。厌氧氨氧化细菌的产率也很低,为11gVSS/gNH4+—N。因此,一般认为ANAMMOX工艺的污泥龄越长越好。1
Strous等人研究了好氧和微氧条件下厌氧氨氧化污泥的性质,发现在好氧和微氧条件下均没有发生氨氧化反应,这说明即使是微量的氧对厌氧氨氧化细菌也有较强的抑制作用。但是,发现氧气对厌氧氨氧化的抑制是可逆的,即当氧氨氧化细菌从好氧或微氧条件下恢复到厌氧条件时,很快就能恢复活性。自厌氧氨氧化工艺提出以来,人们对这一全新的氨氧化过程进行了大量的研究。结果发现,在自然界的许多缺氧环境中(尤其是在缺氧/有氧界面上),如土壤、湖底沉积物等,均有厌氧氨氧化细菌存在。因此,厌氧氨氧化菌在自然界分布广泛。1
影响因素(1)底物浓度
厌氧氨氧化过程的底物是氨和亚硝酸盐,但如果二者的浓度过高,也会对厌氧氨氧化过程产生抑制作用。有研究表明,氨的抑制浓度为38.0~98.5nmol/L,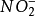 的抑制浓度为5.4~12.0nmol/L。Jetten等人的研究认为,在
的抑制浓度为5.4~12.0nmol/L。Jetten等人的研究认为,在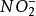 浓度高于20nmol/L时,ANAMMOX工艺受到
浓度高于20nmol/L时,ANAMMOX工艺受到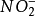 的抑制,长期(2h)处于高
的抑制,长期(2h)处于高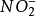 浓度下,ANAMMOX活性会完全消失,但在较低的
浓度下,ANAMMOX活性会完全消失,但在较低的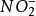 浓度(10nmol/L左右)下,其活性仍会较高。1
浓度(10nmol/L左右)下,其活性仍会较高。1
(2)pH值
由于氨和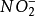 在水溶液中会发生离解,因此pH值对厌氧氨氧化有影响。研究表明,ANANNOX工艺在pH值为6.7~8.3范围内可以运行较好,最适pH值为8左右。
在水溶液中会发生离解,因此pH值对厌氧氨氧化有影响。研究表明,ANANNOX工艺在pH值为6.7~8.3范围内可以运行较好,最适pH值为8左右。
(3)温度
厌氧氨氧化的适宜温度为30~40℃,有研究认为,最适温度在30℃左右。1
本词条内容贡献者为:
郑国忠 - 副教授 - 华北电力大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国