简述
X光若要电离某一壳层(如K层)的电子,其能量E必须大于该壳层的电子结合能Ek,由波长等于hc/E知,波长必须小于hc/Ek,越接近此值,越容易激发电离,吸收系数变大;但一旦波长大于前面所说的极限值,吸收系数会突然下降。因而在极值附近吸收系数有一个突变,这个突变对应的波长是吸收限,这个突变成为吸收边或吸收突跃2。
计算方法与最小激发电压V0(KeV)的关系如下式:
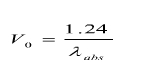
X射线吸收近边结构理论在X射线吸收谱中,吸收边之上60eV以内的低能区的谱出现强的吸收特性,称之为近边吸收结构(XANES)。它是由于激发光电子经受周围原子的多重散射造成的。它不仅反映吸收原子周围环境中原子几何配置,而且反映凝聚态物质费米能级附近低能位的电子态的结构。因此成为研究凝聚态物质的有用工具1。
1913 年英国物理学家H.莫塞莱研究了许多种元素的X射线标识谱(见X射线谱),发现谱线频率的二次方根与该元素在元素周期表中排列的顺序号成线性关系。他认识到这些标识谱是由于原子内层电子跃迁而产生。莫塞莱把各元素的Kα线系和Lβ线系的频率表达为:
vKα=Rc(Z-σK)2(1/12-1/22)
vLβ=Rc(Z-σL)2(1/22-1/32)
式中R是里德伯常数,Z是原子序数,σ是屏蔽因子,c是光速。他发现各元素σK和σL分别都近似等于1和7.4。对于其他线系则不再适用。
莫塞莱利用上述规律,并用实验测出的X射线标识谱线的频率来确定元素在周期表上排列的序号Z,发现只在Co—Ni,Ar—K,Te—I等相邻元素处与原来按原子量大小排列的次序不符。改动后能使周期表上元素的化学、物理性质的周期性规律更符合实际。因此莫塞莱把按X射线谱排列的序号称为原子序数,认为这正是元素原子核所带的正电荷数,也是决定元素化学、物理性质的最主要因素。后来把莫塞莱定律推广到原子光谱中,用来描述光谱项值的二次方根与原子序数的线性关系,由此而画出的图称莫塞莱图。
量子力学证明,描述各元素X射线标识谱规律的莫塞莱定律只是一种近似的规律。但它曾对确定原子序数,预言当时还未发现的元素,研究等电子离子序列光谱和原子结构都有过重要作用。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国