简介
一氧化碳是大气中危害很大的一种污染物。工业上煤不完全燃烧产生的废气,汽车的尾气,以及火山爆发的气体中都含有CO。据估计,全世界CO的年产量可高达(3.1×109)~(14.1×109)t。地球表面土壤的细菌在清除大气中CO的过程中,发挥了非常重要的作用。这是因为这些细菌细胞内存在一大类一氧化碳脱氢酶(carbon monoxide dehydrogenase,CODH)。
一氧化碳脱氢酶是一大类存在于许多需氧和厌氧微生物中的脱氢酶,能够催化一氧化碳氧化为二氧化碳的反应或其逆反应,在这些微生物的代谢途径中起着关键作用。
CO+H2O⇌CO2+2H++2e-
不同来源的一氧化碳脱氢酶具有不同的结构和催化机理。
需氧细菌中的一氧化碳脱氢酶是一类含钼(Mo)金属蛋白,需氧细菌利用它们在呼吸作用中氧化一氧化碳来获得能量。而厌氧微生物(包括厌氧细菌和古菌)中的一氧化碳脱氢酶则属于含镍(Ni)金属蛋白,在不同种属的微生物中发挥不同的作用。特别在厌氧微生物固定一氧化碳和二氧化碳的Wood—Ljungdahl代谢途径中,一氧化碳脱氢酶可以与乙酰辅酶A合成酶(同为镍蛋白)结合形成双功能酶,共同发挥作用,将一氧化碳和二氧化碳转化为重要的代谢中间物乙酰辅酶A。由于一氧化碳脱氢酶能够高效地催化对动物和人体有很高毒性的一氧化碳氧化为二氧化碳,因此对于其催化机理的研究有助于治理环境中的一氧化碳污染。1
类型一氧化碳脱氢酶分为两大类:存在于需氧微生物中的Mo—Fe一黄素酶类和存在于厌氧微生物中的Ni—Fe酶类。由于组成这两类金属酶活性中心、起关键作用的金属分别是钼和镍,因此,这两类酶分别称为含钼一氧化碳脱氢酶——(Mo—CODH)和含镍一氧化碳脱氢酶——(Ni—CODH)。Mo—CODH对CO有很高的亲和力,适合于除去环境中痕量的一氧化碳气体;而就催化活性而言,Ni—CODH则是Mo—CODH的近1 000倍。2
含钼一氧化碳脱氢酶自然界的一氧化碳自养菌(carboxydotrophs)中存在含钼一氧化碳脱氢酶(Mo—CODH),它是一类含钼的铁硫黄素蛋白。
在一氧化碳自养菌中,除少数Mo—CODH定位于细胞质外,大多数Mo—CODH都连接在细胞质膜的内表面上,从而有利于其与同样连接在内膜上的电子受体——细胞色素b561之间进行电子传递。在Mo—CODH中,Mo结合在钼喋呤胞嘧啶二核苷酸(MCD)辅助因子上。
业已发现,在嗜温菌食羧寡氧菌(Oligotropha carboxidovorans)和嗜热菌高温食羧寡氧菌(Oligotropha thermocarboxidovorans)中,Mo—CODH的相对分子质量为230 000~310 000,由相同的亚基组成。下面重点介绍迄今研究最多的食羧寡氧菌的Mo—CODH。2
分子结构天然的Mo—CODH是一个二聚体,每个单体是由L、M和s三个亚基组成的LMS复合物。L、M和S亚基分别由809、288和166个氨基酸组成,其相对分子质量分别为88 700、30 200和17 800。Mo—CODH的整体结构如图1所示。

Mo—CODH的L亚基又称为钼蛋白(molybdoprotein),含有钼和与之结合的MCD,其中钼离子与另一金属离子铜离子形成活性中心的[ CuSMoO2]簇;M亚基为黄素蛋白,其中含有黄素腺嘌呤二核苷酸(FAD);S亚基属于铁硫蛋白,结合了两个[ 2Fe一2S ]簇。s亚基从结构上可以分为N端和C端两个结构域,这两个结构域各结合了一个[2Fe一2S]簇。M亚基由N端、中间和C端三个结构域组成。其FAD分子的结合位点有两段特征性的“双甘氨酸(double—glycine)”序列。
L亚基不仅包含有活性中心,也在LMS复合物形成及Mo—CODH二体化中起主要作用。L亚基含有N端结构域和C端结构域,而钼原子就定位在这两个结构域的结合面上。MCD辅助因子的一端连接Mo的部分与活性中心的[CuSMoO2]簇一起结合在N端结构域的凹槽中;而辅助因子的另一端则插入C端结构域的裂缝中。L亚基的N端结构域与M和s亚基相互作用以形成LMS复合物;而C端结构域则主要参与形成Mo—CODH二聚体结构。 2 ’
活性中心Mo—CODH的活性中心位于L亚基,并被包埋于蛋白质内部。但是,从外部可以通过一个约1.7nm长的通道到达活性中心。这个通道由疏水残基构成,从而允许CO分子进入,而又能阻止极性溶剂分子(如水分子)进入。近期的研究表明,Mo—CODH的活性中心是一个Cu—Mo金属簇,其包含有一个Cu离子和一个[MoO2],Cu离子和Mo离子之间通过一个配位硫原子(μS,又称为硫桥)来连接,结合在Cys388的Sγ原子上,将此金属簇[CuSMoO2]与L亚基共价连接的是Cu而不是Se。而MCD是通过其上的两个S原子与Mo离子形成配位键。这种由Mo和Cu两种金属组成的双核金属簇非常独特,因为所有已知的钼蛋白或MCD的Mo金属蛋白中都是单核的。
Mo—CODH的每个单体都是一个完整的催化单元,可以独立地进行催化反应。2
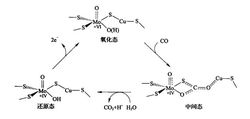
催化机理研究不同状态下活性中心的结构变化,可以推测整个催化过程:处于氧化态的Mo(+VI价)离子与MCD上的两个硫原子以及0a和Ob形成扭曲的金字塔形的四配位结构;当CO结合上后,CO与硫桥、0b以及铜离子连接并处于同一平面上,钼离子被还原为+Ⅳ价,Mo与Oa之间距离缩短,可能形成了三键连接;在H20分子的攻击下,CO2和H+被释放出来,Mo与Oa之间回到双键连接,而Ob变为OH基团与钼离子之间形成单键连接,整个活性中心处于还原态;将两个电子传递给铁硫簇Ⅱ后,活性中心又重新回到氧化态,从而完成一轮催化过程(图2)。2
抑制作用Mo—CODH很容易被氰化物所抑制,这种抑制主要是通过氰化物与[CuSMoO2]簇的硫桥和铜离子反应生成游离的硫氰离子(SCN-)和氰化铜(CuCN)来使活性中心失活。2
含镍一氧化碳脱氢酶含镍一氧化碳脱氢酶(Ni—CODH)广泛存在于以一氧化碳为碳源和能源的厌氧微生物中,如乙酸生成细菌(acetogenic bacteria)、光养细菌(phototrophic bacteria)、氢气生成细菌(hydrogenogenic bacteria)、硫酸还原细菌和古菌(sulfate—reducing bacteria and archaea)以及甲烷生成古菌(methanogenic archaea)等。
Ni—CODH在活性位点处的关键金属为Ni,负责电子传递的铁硫簇为[4Fe一4S]而非[2Fe一2S],而且没有发现有像Mo—CODH中的FAD和MCD辅助因子,整体结构上也没有相似性。不同来源的Ni—CODH差别很大:既有单功能的一氧化碳脱氢酶只负责催化CO的氧化;又有双功能酶,即同时具有一氧化碳脱氢酶和乙酰辅酶A合成酶(ACS)的活性,生理状态下需要Ni—CODH与ACS结合共同发挥功能。因此,又常常以CODH/ACS复合物的名称来代替Ni—CODH。2
分类根据催化活性、代谢功能和蛋白性质和组成的不同,可以将CODH/ACS分为以下四类:
(1)第一类存在于专性化能自养的甲烷生成菌,负责直接利用CO2和氢气(H2)来合成乙酰辅酶A。
(2)第二类酶则负责与第一类相反的反应,即将乙酰辅酶A分解为CO2和CH4,主要存在于利用乙酸的甲烷生成古菌和硫酸还原菌中。
(3)第三类CODH/ACS存在于乙酸生成细菌中,其作用与第一类酶相同,只是以丙酮酸盐作为Co2和H2的来源,并参与Wood—L jungdahl途径。图3显示第三类Ni—CODH/ACS整体结构及各金属簇位置。
(4)第四类酶是一类单功能酶.只负责催化CO的氧化。2

活性中心除第四类CODH/ACS外,其他三类酶都是双功能酶,甚至多功能酶。因此,这三类酶具有两个或多个活性中心。其中,两个核心反应,即CO的氧化和乙酰辅酶A的合成,对应的活性中心金属簇分别为C簇和A簇。其中,C簇位于α亚基(第三类CODH/ACS中为β亚基),其组成为[Ni-4Fe一4S]或[Ni一4Fe一5S];而A簇位于β亚基(第三类CODH/ACS中为α亚基)。A簇和C簇之间通过一个疏水通道相连,从而可以相互传递催化产物。此外,α亚基(第三类CODH/ACS中为β亚基)二聚体中还含有5~7个铁硫簇[4Fe一4S],负责电子传递。
催化机理负责CO的氧化的活性中心C簇的催化机理主要由两步反应组成。第一步,CO被氧化,而C簇被还原;第二步,电子从C簇传递到蛋白外的电子受体,如铁氧化还原蛋白(ferredoxin),C簇回到初始状态。在这一过程,C簇中存在四种氧化还原态:Cox,Cred1,Cint和Cred2。其中,处于氧化状态(Ni2+一Fel 3+)的Cox在获得一个电子之后转化为Cred1。Cred1是与CO和OH基团结合时C簇的状态;而Cred2出现在Credl之后,此时CO可能已被氧化为CO2,并释放出H+离子。这步反应可能是由OH基团攻击连接在Ni上的CO引发,因为在C簇周围有多个碱性残基(包括一个赖氨酸和多个组氨酸),使结合在Fel上的水分子的pKa显著降低,从而使水分子转变为活性的OH基团,对CO进行攻击。此外,在C簇附近还有一个保守的天冬氨酸,可以与组氨酸形成氢键连接,促进此酸碱反应的发生。反应生成的H+通过组氨酸形成的质子通道传递到外部溶剂中。CO被氧化为CO2后,C簇接受两个电子从Cred1转变为Cred2,随后两个电子一个接一个地被传递到B簇。传走第一个电子后,C簇转化为中间态Cint;两个电子都传到B簇后,C簇又重新转化为Cred1,从而完成一次催化循环。2




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国