中国是生猪生产和消费大国,生猪的饲养量约占全球一半。猪肉在居民肉类消费结构中的占比高达62.7%,也是国人肉食蛋白摄入的主要来源。数千年来以猪肉为主的饮食习惯导致其成为国人餐桌上最重要的肉类,煎、炒、烹、炸等丰富的食用方法总让人不禁大快朵颐。
随着生活水平的提升,食品在日常消费中所占比例日渐降低,猪肉逐渐从上世纪的奢侈品变为日常消费品。由于我国居民饮食习惯因素,猪肉是绝大部分居民最主要的肉食来源。猪肉价格水深火热,牵动着全国人民的小心脏。还未实现“车厘子自由”的吃瓜群众,眼看着又失去了“猪肉自由”。继按揭买车买房后,甚至出现了“按揭买猪肉”。
2019本命猪年处于风口浪尖上,“猪”事不顺,猪肉价格飙升,居民消费价格指数(CPI)上涨至2.8%,得到了前所未有的广泛关注,甚至引起国务院就稳定生猪生产和猪肉的保供应稳价格召开了一系列会议,并于9月11日发布《关于稳定生猪生产促进转型升级的意见》。
猪肉价格为何飙升?
2018年8月3日,沈阳首次爆发非洲猪瘟,随后疫情迅速大范围蔓延,对我国生猪养殖业造成重创,给国民经济带来巨大损失。2019年4月19日,海南确认发生首例疫情,至此我国31个省份自治区均被波及。2019年9月17日,韩国发现首例非洲猪瘟疫情。非洲猪瘟传播之快,不仅是中国,非洲猪瘟疫情很可能对整个亚洲的养猪行情产生深远的影响。
实际上,疫病真正感染的猪往往不多。但一旦有流行的征兆,以防感染,各地存栏的猪会提前宰杀上市,导致短时间内猪肉供应量大增,价格下降。等到这一批提前出栏的猪肉卖完,供应短缺,价格便迅速飙升。去年9月14日生猪(外三元)的价格是14.45元/公斤,一年后的今天,价格涨到了27.92元/公斤,创历史新高,相比去年涨幅高达93%。

生猪(外三元)价格一年走势 图片来源:中国养猪网
非洲猪瘟对生猪是一个毁灭性的疾病,感染病毒的生猪死亡率达到百分之百。一旦发现非洲猪瘟感染病例,需要立即扑杀,甚至殃及整个猪场。目前国内大部分猪场损失亏本,甚至清场转行。生猪供应链不足,导致猪肉价格疯涨。
此外,用于非洲猪瘟检测和猪场消毒的投入增加,养猪风险颇高,若非洲猪瘟疫苗仍未上市,未来生猪价格将进一步走高。生猪供应的形势十分严峻,截至2019年8月,生猪存栏较去年同期锐减了近四成。
迫使猪肉价格上涨的非洲猪瘟到底是什么?
1921年,非洲猪瘟首发现于肯尼亚,上世纪五、六十年代在非洲、欧洲、南美洲流行,2018年非洲猪瘟首次传入中国。
非洲猪瘟(African swine fever, ASF)是由非洲猪瘟病毒(African swine fever virus, ASFV)引起的猪的一种急性、热性、高度接触性传染病,发病率和死亡率可达100%。世界动物卫生组织将其列为法定报告动物疫病,我国将其列为一类动物疫病。
非洲猪瘟病毒(ASFV)是一种有囊膜的DNA病毒,是非洲猪瘟病毒科、非洲猪瘟病毒属的唯一成员。ASFV分为24个基因型,首次发现的传入我国的ASFV毒株属于基因II型。

非洲猪瘟病毒,粒子直径约为200纳米,呈正20面体结构,由多层同心圆结构组成 图片来源:中国动物保健
ASFV对热的抵抗力较弱,在60℃温度下暴露20分钟或在56℃温度下暴露70分钟可被灭活,一般的消毒措施均可有效杀灭ASFV。最有效的消毒剂是去污剂、次氯酸盐、碱类及戊二醛。ASF的自然传播速度慢,高度接触传播,直接接触、采食、蜱虫叮咬、注射等可传播疫病。
非洲猪瘟为什么“来势汹汹”?
ASF的传染源为带非洲猪瘟病毒野猪和发病家猪的分泌物及排泄物、含有病死猪组织或非洲猪瘟病毒污染的泔水、含非洲猪瘟病毒的猪肉及其制品,以及钝缘软蜱。

图片来源:泽州新闻非洲猪瘟科普漫画
其传播途径是通过感染猪与健康易感猪的直接接触可传播非洲猪瘟病毒。非洲猪瘟病毒可通过饲喂污染的泔水、污染的饲料、垫草、车辆、设备、衣物等间接传播。消化道和呼吸道是最主要的感染途径。
易感动物为家猪和野猪。幸运的是,非洲猪瘟并非人兽共患,因此其它哺乳动物包括人类均不感染ASFV。目前报道的发病猪群主要是饲喂ASFV污染泔水的猪。
自然感染条件下,ASF的潜伏期为3-19天,感染猪在潜伏期即可排毒,临床症状出现后可通过分泌物和排泄物大量排毒。ASFV对环境的抵抗力很强,在尸体中可存活6个月以上,在低温条件下可存活数年,在腐败的血液中可存活近4个月,在冷鲜肉中存活数周至数月,在腌制和熏制的猪肉产品中可长时间存活,在粪便中可保持感染性数周。
非洲猪瘟病毒疫苗研制,为什么这么难?
由于非洲猪瘟病毒感染机制复杂,目前世界范围内至今尚未生产有效预防用非洲猪瘟疫苗,因此早期发现、精准检测是控制该病传播和发生的关键。采取严格的生物安全措施清除猪场内已存在的非洲猪瘟病毒及阻止病毒与猪的接触是目前唯一有效的途径。

图片来源:sohu.com
非洲猪瘟病毒在上个世纪刚被发现时,研究人员就已开始研制疫苗,但传统疫苗策略如灭活病毒已被证实无效。其困难之处在于,非洲猪瘟病毒基因型众多(根据主要衣壳蛋白p72分为24个基因型),免疫逃逸机制复杂,由多个毒力基因共同发挥作用。多个基因型之间的生物学特性差异大。同时,非洲猪瘟病毒基因组中存在的大量重复元件,有利于基因组重组的发生,进一步导致了病毒基因组及表型的多样性,极大增加了防控难度。
此外,ASFV感染可经由免疫介导而增强,过量产生抗体甚至可加剧疾病进程。目前国内外采用传统研究策略研制出ASFV的灭活疫苗、自然弱毒或传代致弱疫苗、新型佐剂和亚单位疫苗等新型疫苗,均未成功,都存在不同程度的局限性,不能达到完全保护的功效。自1921年非洲猪瘟在肯尼亚首次发现以来,全球已68个国家和地区发生,目前只有13个国家曾经实现根除,根除时间多为5至36年。
中国科学家攻克非洲猪瘟疫苗研发难题
由于我国猪饲养量巨大,需要付出巨大人力、物力和财力。仅靠扑杀防疫手段,成本太高,安全、有效的疫苗是控制我国非洲猪瘟疫情的迫切需求。诱导强烈的细胞免疫,如NK细胞和T细胞反应,是设计安全有效的ASFV疫苗的准则。
今年1月,青岛的中国动物健康与流行病学中心发表了当地毒株的基因组序列。随后2月,中国农业科学院哈尔滨兽医研究所从感染猪的脾脏中成功分离出我国第一株非洲猪瘟病毒Pig/HLJ/18,为检测技术和疫苗研发奠定了重要基础。
我国科学家成功创制非洲猪瘟候选疫苗 图片来源:兽药网
今年4月,我国非洲猪瘟疫苗研制的实验室研究工作首次取得成功。哈兽研采用非洲猪瘟中国流行株Pig/HLJ/18,通过建立非洲猪瘟病毒CRISPR/Cas9基因敲除操作技术平台,经基因工程技术,将非洲猪瘟病毒的毒力基因敲除,获得MGF360-505R缺失和CD2V与MGF360-505R联合缺失的基因缺失弱毒疫苗。随后8月6日,哈兽研将其成果通过《基因缺失的减毒非洲猪瘟病毒及其作为疫苗的应用》专利申请公布。实验室研究结果显示,该疫苗能提供对非洲猪瘟中国流行强毒株的100%免疫保护,可作为安全和有效的防控中国非洲猪瘟疫情的疫苗,具有极大的社会价值。
今年8月疫苗研发工作又取得了新的重要进展。哈兽研在前期基因缺失疫苗自主研发工作的基础上,进一步筛选出一株非洲猪瘟双基因缺失弱毒活疫苗。这就和给人注射的疫苗相似,用毒力减弱但免疫原性强的非洲猪瘟病原微生物及其代谢产物,经培养繁殖后制成。不会引起非洲猪瘟,相应地刺激机体产生免疫反应,使其获得长期或终生保护的作用。
9月10日,中国农业科学院召开非洲猪瘟防控与生猪复养技术推介会。会上发布,该株非洲猪瘟双基因缺失弱毒活疫苗已完成了实验室安全评估与有效试验,突破了以原代骨髓巨噬细胞实现疫苗规模化生产的重大技术瓶颈,近期已向农业农村部提出生物安全评价申请,即将进入临床试验阶段。
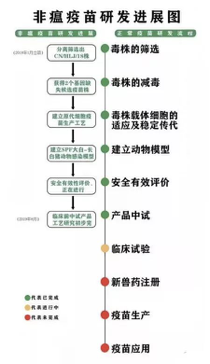
非洲猪瘟疫苗研发进展 图片来源:sohu.com
在当今万物“互联网+”的大趋势下,阿里、京东、网易等互联网巨头们纷纷开启了智能生猪养殖。或许熬过“本命年”这场非洲猪瘟引发的生猪保卫战后,猪场顺利规模化转型升级智能模式,“二师兄”们都可以从一出生就享受着高科技生活了。期盼非洲猪瘟疫苗问世后,在国家的政策调控下,生猪保供稳价复产,百姓们能重新实现“猪肉自由”,随时吃上美味猪肉,“猪”事顺利。
参考文献:
1.Zhao D , Liu R , Zhang X , et al. Replication and virulence in pigs of the first African swine fever virus isolated in China. Emerging Microbes & Infections, 2019, 8(1):438-447.
- Bao J, Wang Q, Lin P, et al. Genome comparison of African swine fever virus China/2018/ AnhuiXCGQ strain and related European p72 Genotype II strains. Transbound Emerg Dis. 2019;66:1167–1176.
3.Mallapaty, S. Spread? of deadly pig virus in China hastens vaccine research. Nature, 2019;569:13-14.
4.Gaudreault, N. N., & Richt, J. A.. Subunit Vaccine Approaches for African Swine Fever Virus. Vaccines, 2019;7(2), 56.
- Zhu, Z., Xiao, C.-T. , et al. Homologous Recombination Shapes the Genetic Diversity of African Swine Fever Viruses. Veterinary Microbiology,2019.
6.中国农业科学院上海兽医研究所.非洲猪瘟检测与诊断技术要点[Z].2019—09




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国