酒石酸伐尼克兰片,适应症为本品适用于成人戒烟。
警示语使用伐尼克兰的患者,有报告出现严重的神经精神症状,包括但不限于抑郁、自杀意念、自杀企图和完成自杀。某些报告可能与停止吸烟的患者的尼古丁戒断症状难以区分。抑郁情绪可能是尼古丁的戒断症状,在进行非药物戒烟的吸烟者中已经有过一些报告,并且偶有自杀想法的报告。不过,服用伐尼克兰且继续吸烟的患者也曾出现上述部分症状。
所有使用本品治疗的患者都应当观察其神经精神症状,包括行为改变、敌意、激越、抑郁情绪和自杀相关事件,包括自杀意念、行为和企图自杀。在上市后经验中,这些症状与原有精神疾病的恶化和自杀,在使用伐尼克兰戒烟的患者中都有报告。这些报告的症状多发生于使用伐尼克兰治疗期间,但部分也出现在停止治疗后。
建议患者及护理人员,当观察到患者出现激越、敌意、抑郁情绪,行为或思维等非自身典型性的改变时,或患者产生自杀意念或自杀行为时,患者应立即停止服用本品,并联系医护人员。在大多数上市后报道病例中,患者停止服用本品后症状消失;不过在某些病例中,这些症状持续存在。因此,应对患者进行持续的监测并提供支持治疗,直到症状完全消除。
成份本品主要成份为酒石酸伐尼克兰
化学名称:7,8,9,10-四氢-6,10-亚甲基-6H-吡嗪酰胺[2,3-h][3]苯并氮杂卓-(2R,3R)-2,3-二羟基丁二酸盐(1:1)
化学结构式:
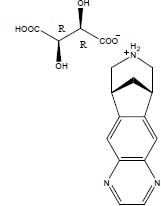
分子式:C13H13N3·C4H6O6
分子量:361.36
性状本品为白色至类白色薄膜衣片(0.5mg 规格)或淡蓝色薄膜衣片(1.0mg 规格),除去包衣后显白色。
适应症本品适用于成人戒烟。
规格0.5mg,1.0mg。
用法用量剂量
本品用于口服。首先按如下方法进行1周的剂量递增,之后推荐剂量为每日2次,每次1mg;患者应设定戒烟日期并在此日期前1~2周开始服用本品。
第1-3日 0.5mg,每日1次(白色片)
第4-7日 0.5mg,每日2次(白色片)
第8日~治疗结束 1mg,每日2次(淡蓝色片)
对无法耐受本品不良反应的患者,可暂时或长期将剂量降至每日2次,每次0.5mg。
患者应服用本品治疗12周。
对于经12周治疗戒烟成功的患者,可考虑续加一个12周疗程,剂量仍为每日2次,每次1mg。
对于初始治疗未成功或治疗后复吸的患者,目前尚无后续12周疗程的疗效资料。
在戒烟治疗中,复吸的风险在紧随治疗结束的期间内升高。在存在复吸高风险的患者中,可以考虑药物逐渐减量。
有戒烟意愿的患者,和获得更多建议和支持的患者,戒烟治疗更易成功。
特殊人群
肾功能损伤患者
轻(估测肌酐清除率]50ml/min且≤80ml/min)至中度(估测肌酐清除率≥30ml/min且≤50ml/min)肾功能损伤患者,不需调整剂量。
中度肾功能损伤且无法耐受不良事件的患者,可将剂量降至每日1次,每次1mg。
重度肾功能损伤患者(估测肌酐清除率[30ml/min),推荐剂量为每日1次,每次1mg。给药剂量应从每日1次,每次0.5mg开始,3天后增加至每日1次,每次1mg。本品对于终末期肾病患者的临床经验有限,因此不推荐在该人群中应用本品(见【药代动力学】)。
肝功能损伤患者
肝功能损伤患者不需调整剂量(见【药代动力学】)。
老年患者
老年患者不需调整剂量(见【药代动力学】)。因老年患者更易发生肾功能减退,处方医生应考虑老年患者的肾功能状况。
儿童患者
本品在儿童或18岁以下青少年人群中的安全性及有效性尚未确定。目前已有数据见【药代动力学】。
尚不推荐本品应用于该人群。
服用方法
本品应用水整片吞服,餐前餐后均可服用。
不良反应无论是否接受戒烟治疗,戒烟本身即伴随多种症状。例如曾有报道试图戒烟的患者出现烦躁不安、抑郁情绪、失眠、易激惹、挫折感、愤怒、焦虑、注意力无法集中、坐立不安、心率下降、食欲增加或体重增加等。本品临床研究的设计及结果分析中未对所出现的不良事件与药物或尼古丁戒断相关性进行区分。
本品的多项临床研究涉及约4,000名患者,治疗时间最长为1年(平均给药84天)。如出现不良反应,通常发生在治疗的第一周,严重程度大多为轻至中度。不同年龄、种族或性别的不良反应发生率无差异。
完成初始剂量递增后,患者服用推荐剂量每日2次,每次1mg。报告最多的不良事件为恶心 (28.6%)。恶心多数发生在治疗的早期,严重程度为轻至中度,很少导致治疗的中断。
因不良事件中断治疗患者的比例,治疗组为11.4%,安慰剂组为9.7%。在这些患者中,治疗组常见不良事件的治疗中断率为:恶心(2.7%,安慰剂组0.6%)、头痛(0.6%,安慰剂组1.0%)、失眠(1.3%,安慰剂组1.2%)及梦境异常 (0.2%,安慰剂组0.2%)。
下表中所列为治疗组发生率高于安慰剂组的不良反应,均按照系统器官种类及发生频率排列:很常见(≥1/10),常见(≥1/100至2000倍)的结合力。此外,伐尼克兰与5-羟色胺(5-HT3)受体具有中等亲和力(Ki=350nM)。
毒理研究
遗传毒性
以下体外和体内试验显示伐尼克兰没有遗传毒性:伐尼克兰Ames试验、哺乳动物CHO/HGPRT试验、体外人淋巴细胞染色体畸变试验、大鼠骨髓微核试验结果均为阴性。
生殖毒性
在 SD 大鼠生育力试验中,雄性大鼠与雌性大鼠经口给予伐尼克兰琥珀酸盐剂量达15mg/kg/天(根据AUC,雄性大鼠与雌性大鼠分别相当于人最大推荐剂量1mg 每天2 次(BID)日暴露量的67 倍与36 倍)时未见生育力损害。但是经口给予伐尼克兰琥珀酸盐剂量达15 mg/kg/天(根据AUC,相当于人最大推荐剂量1mg BID 日暴露量的36 倍)的妊娠大鼠子代可见生育力降低,3 mg/kg/天(根据AUC,相当于人最大推荐剂量1mg BID 日暴露量的9 倍)剂量组妊娠大鼠未见改变。
大鼠与家兔经口给予伐尼克兰琥珀酸盐剂量分别达15 与30 mg/kg/天(根据AUC,分别相当于人最大推荐剂量1mg BID 日暴露量的36 倍与50 倍)未见致畸作用。动物试验结果显示,伐尼克兰琥珀酸盐对胎儿有影响。妊娠家兔经口给予伐尼克兰琥珀酸盐剂量达30 mg/kg/天(根据AUC,相当于人最大推荐剂量1mg BID 日暴露量的50 倍)可见胎仔重量减轻;剂量为10mg/kg/天(根据AUC 相当于人最大推荐剂量1mg BID 日暴露量的23 倍)时未见该现象。此外,妊娠大鼠经口给予伐尼克兰琥珀酸盐剂量达15 mg/kg/天(根据AUC,相当于人最大推荐剂量1mgBID 日暴露量的36 倍)可见子代生育力降低,听觉惊吓反应增强。
致癌性
CD-1 小鼠经口给予伐尼克兰剂量达20 mg/kg/天(根据AUC 约为人最大推荐日暴露量的47 倍)连续2 年,未见肿瘤发生率增加。
SD 大鼠经口给予伐尼克兰剂量为1、5、15 mg/kg/天连续2 年。在雄性大鼠(n = 65 只/性别/剂量组)中,可见中、高剂量组冬眠瘤发生率增加(中剂量5mg/kg/天根据AUC 约为人最大推荐日暴露量的23 倍,1 例;高剂量15 mg/kg/天根据AUC 约为人最大推荐日暴露量的67 倍,2 例)。尚未确立该发现与人体的临床相关性。雌性大鼠未见肿瘤发生率增加。
药代动力学吸收:
伐尼克兰一般在口服给药后3~4小时达到血浆峰浓度。健康志愿者多次口服给药后,血药浓度可在4天内达到稳态。口服给药吸收完全,系统生物利用度高。伐尼克兰口服生物利用度不受食物和给药时间的影响。
分布:
伐尼克兰分布于包括脑组织的各种组织中。稳态表观分布容积平均为415升(%CV=50)。伐尼克兰血浆蛋白结合率低(≤20%),且与年龄及肾功能无关。在啮齿动物,伐尼克兰能通过胎盘并在乳汁中分泌。
生物转化:
伐尼克兰代谢率很低,92%以原形药物经尿排出,不足10%以代谢产物排出。尿中的少量代谢产物包括伐尼克兰-N-氨基甲酰葡萄糖苷酸及羟基伐尼克兰。体循环中与伐尼克兰相关的物质91%为原形药物。体循环中的少量代谢产物包括伐尼克兰-N-氨基甲酰葡萄糖苷酸及N-转葡糖基伐尼克兰。
体外研究显示伐尼克兰不抑制细胞色素P450酶(IC50>6,400ng/ml)。经抑制实验检测的P450酶包括:1A2,2A6,2B6,2C8,2C9,2C19,2D6,2E1及3A4/5。研究亦显示,在人类离体肝细胞中,伐尼克兰未诱导细胞色素P450酶1A2及3A4的活性。因此,对于主要由细胞色素P450酶所代谢的化合物,伐尼克兰改变其药代动力学参数的可能性不大。
排泄:
伐尼克兰的清除半衰期约为24小时,其肾脏排泄主要通过肾小球滤过及肾小管借助于有机阳离子转运蛋白OCT2的主动分泌。
线性/非线性:
单次给药(0.1-3mg)或重复给药(1-3mg/日)时,伐尼克兰具有线性动力学特征。
特殊人群的药代动力学:
特定药代动力学研究及群体药代动力学分析所显示,伐尼克兰的药代动力学参数不因年龄、种族、性别、吸烟状况或合并用药的不同而发生有显著临床意义的变化。
肝功能损伤患者:
因伐尼克兰基本不经肝脏代谢,肝功能损伤患者应用该药时其药代动力学参数不受影响(见【用法用量】)。
肾功能损伤患者:
对于轻度肾功能损伤的受试者(估测肌酐清除率>50ml/min且≤80ml/min),伐尼克兰药代动力学参数无变化。与肾功能正常受试者(估测肌酐清除率




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国