范围
GB 15571—2010 本标1准适用于以淀粉为起始原料,经发酵法制得的葡萄糖与钙源反应制得的食品添加剂葡萄糖酸钙。
规范性引用文件本标准中引用的文件对于本标准的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本标准。凡是不注日期的引用文件,其新版本(包括所有的修改单)适 用于本标准。
化学名称、分子式和相对分子质量化学名称D-葡萄糖酸钙盐一水合物
分子式C12H22CaO14·H2O
相对分子质量448.39(按 2007 年国际相对原子质量)
技术要求感官要求感官要求应符合表 1 的规定。
表 1 感官要求
|| ||
理化指标理化指标应符合表 2 的规定。
表 2 理化指标
|| ||
附录(规范性附录)检验方法
安全提示本标准试验方法中使用的部分试剂具有毒性或腐蚀性,按相关规定操作,使用时需小心谨慎。若溅到皮肤上应立即用水冲洗,严重者应立即治疗。在使用挥发性酸时,要在通风橱 中进行。
一般规定除非另有说明,在分析中仅使用确认为分析纯的试剂和 GB/T6682—2008 中规定的三级 水。 试验方法中所用标准滴定溶液、杂质测定用标准溶液、制剂及制品,在没有注明其他要 求时,均按 GB/T 601、GB/T 602、GB/T 603 之规定制备。
鉴别试验试剂和材料
1 冰乙酸。
2 苯肼:临用时蒸馏。
分析步骤
1 钙盐鉴别
取约 1.0 g 实验室样品,精确至 0.01 g,加 40 mL 水溶解,必要时加热使溶解,取此溶 液按《中华人民共和国药典》2005 年版二部附录 Ⅲ 一般鉴别试验钙盐项下(2),应显钙 盐的鉴别反应。
2 葡萄糖的鉴别
取约 0.5 g 实验室样品,精确至 0.01 g,置 10 mL 试管中,加 5 mL 水,溶解(必要时加 热),加 0.7 mL 冰乙酸和 1 mL 苯肼,在水浴上加热 30min,放至室温,用玻璃棒摩擦试管 内壁,则析出黄色的结晶。
葡萄糖酸钙的测定方法提要
以钙紫红素为指示剂,用乙二胺四乙酸二钠标准滴定液滴定样品水溶液,根据乙二胺四 乙酸二钠标准滴定液的用量,计算以 C12H22CaO14·H2O 计的葡萄糖酸钙的含量。
试剂和材料
1 钙紫红素指示剂。
2 氢氧化钠溶液:40g/L。
3 乙二胺四乙酸二钠标准滴定液:c(EDTA)=0.05mol/L。
分析步骤
取约 0.5g 实验室样品,精确至 0.000 1g,加 100 mL 水,使溶解(必要时加热),放至 室温,加 15mL 氢氧化钠溶液,0.1g 钙紫红素指示剂,用乙二胺四乙酸二钠标准溶液滴定至 溶液由紫色转变为纯蓝色,并将滴定结果用空白试验校正,每 1mL 的乙二胺四乙酸二钠滴 定液相当于 22.42mg 的 C12H22CaO14·H2O 。
结果计算
葡萄糖酸钙(以C12H22CaO14·H2O 计)的质量分数w1,数值以%表示,按公式计算:
式中: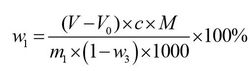
V ——实验室样品消耗乙二胺四乙酸二钠标准滴定液体积的数值,单位为毫升(mL);
V0 ——空白试验消耗乙二胺四乙酸二钠标准滴定液体积的数值,单位为毫升(mL);
c——乙二胺四乙酸二钠标准滴定溶液浓度的准确数值,单位为摩尔每升(mol/L);
m1 ——实验室样品质量的数值,单位为克(g);
w3 ——按A.8下测定的供试品干燥减量质量分数,数值以%表示;
M ——C12H22CaO14·H2O 的摩尔质量的数值,单位为克每摩尔(g/mol)(M=448.39)。
取两次平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.2%。
氯化物的测定试剂和材料
1 硝酸溶液:25→100。
2 硝酸银溶液:17g/L。
3 氯化钠标准溶液:每毫升含0.01mg 的Cl。
分析步骤
称取 1.0g±0.01g 实验室样品,置 100mL 容量瓶中,加 80mL 水使溶解,再用水稀释至 刻度,摇匀,即为实验室样品溶液。分别吸取 10.0 mL 实验室样品溶液与 5mL±0.05mL 氯化钠标准溶液,按 GB/T 9729 测定。
硫酸盐的测定试剂和材料
1 盐酸:20→100。
2 硫酸钾乙醇溶液:0.2g/L。
3 氯化钡溶液:250g/L。
4 硫酸盐标准溶液:每毫升含0.1mg 的SO4。
分析步骤
称取0.5g±0.01g实验室样品,加水微热溶解成约20mL,用此溶液,同时另取 2.5mL±0.05mL硫酸盐标准溶液按 GB/T 9728测定。
还原物质的测定试剂和材料
碱性柠檬酸铜溶液的配制:
溶液A:称取173 g柠檬酸钠(枸橼酸钠)和100g无水碳酸钠,加温水使溶解成700mL(若 溶液显浑浊过滤使澄清) 。
溶液B:称取17.3 g硫酸铜结晶,加水使溶解成100mL。
临用前取100 mL溶液B,在不断振摇下,缓缓加入700mL溶液A,冷却后,加水定容至 1000mL。
2 碘标准液:c(1/2I2)=0.05 mol/L。
3 硫代硫酸钠标准滴定溶液:0.1mol/L。
4 淀粉指示液:10g/L。
5 乙酸溶液:1+27。
6 盐酸溶液:3mol/L。
分析步骤
称取约1.0g 实验室样品,精确至0.001g,置250mL碘瓶中,加20mL水(必要时加热) 使溶解,冷却至室温,精确加入25.0 mL碱性柠檬酸铜溶液,瓶口用小表面皿盖住,准确微 沸5 min后,迅速冷却至室温,加25.0 mL乙酸溶液,摇匀,精确加入10.0 mL碘标准液,密 塞,摇匀,放置10 min,加入10.0mL盐酸溶液,再加3.0mL淀粉指示液,立即用硫代硫酸钠 标准溶液滴定至溶液显亮蓝色,并将滴定结果用空白试验校正。每毫升硫代硫酸钠标准溶液 (0.1mol/L)相当于2.7mg葡萄糖。
结果计算
还原糖(以C6H12O6计) 的质量分数w 2 ,数值以%表示,按公式计算:
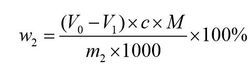 式中:
式中:
0V ——空白试验所消耗的硫代硫酸钠标准滴定溶液的体积的数值,单位为毫升(mL);
1V ——滴定试验溶液所消耗的硫代硫酸钠标准滴定溶液的体积的数值,单位为毫升(mL);
c——硫代硫酸钠标准滴定溶液实际浓度的数值,单位为摩尔每升(mol/L);
2m ——实验室样品质量的数值,单位为克(g); M ——还原糖(3/20C6H12O6)的摩尔质量的数值,单位为克每摩尔(g/mol)(M=27)。
干燥减量的测定仪器和设备
恒温干燥箱。
分析步骤
称取约1.0g 实验室样品细粉,精确至0.000 1g,置于已经在105 ±2 ℃℃干燥至恒重的称 量瓶中,精密称定,再置105 ±2 ℃℃恒温干燥箱内干燥至恒重,从减失的质量和称样量计算 样品的干燥减量。
结果计算
葡萄糖酸钙干燥减量的质量分数w 3 ,数值以%表示,按公式计算:
式中: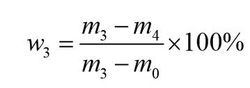
m0——称量瓶的质量的数值,单位为克(g);
m3——称量瓶和干燥前实验室样品质量的数值,单位为克(g);
m4——称量瓶和干燥后实验室样品质量的数值,单位为克(g)。
重金属的测定试剂和材料
1 硝酸。
2 甘油。
3 乙酸铵。
4 硝酸铅。
5 硫代乙酰胺。
6 盐酸溶液:c(HCl)=2 mol/L。
7 氨水溶液:c(NH3·H2O)=5 mol/L。
9 盐酸溶液:c(HCl)=7 mol/L 。
10 乙酸盐缓冲液(pH3.5):称取25 g乙酸铵,精确至0.01 g,加25 mL水溶解后, 加7 mol/L盐酸溶液38 mL,用2 mol/L盐酸溶液或5 mol/L氨水溶液准确调节pH至3.5(pH 计),用水稀释至100 mL。
11 硫代乙酰胺试液:称取4 g硫代乙酰胺,精确至0.01 g,加水使溶解成100 mL, 置冰箱中保存。临用前取5.0 mL混合液(由15 mL 1 mol/L氢氧化钠溶液、5.0 mL水及20 mL甘油组成),加上述1.0 mL硫代乙酰胺溶液,置水浴上加热20s,冷却,立即使用。
12 铅标准溶液:称取0.160 g硝酸铅,精确至0.000 2g,置于1000 mL容量瓶中,加 硝酸5 mL与50 mL水溶解后,用水稀释至刻度,摇匀,作为贮备液。临用前,移取10 mL±0. 02mL贮备液,置于100 mL容量瓶中,加水稀释至刻度,摇匀,即得(每1mL相当于10 µg 的Pb)。配制与贮存用的玻璃仪器均不得含铅。
分析步骤
按《中华人民共和国药典》2005 年版二部附录 Ⅷ H 重金属检查法第一法进行。具体 方法如下: 取 25 mL 纳氏比色管两支,甲管中加入 1 mL±0.01mL(含铅 10.0μg)铅(Pb)标准溶 液与 2 mL 乙酸盐缓冲液后,加水稀释成 25 mL,另称取 1 g 实验室样品,精确至 0.01 g,置 于纳氏比色管乙管中,加 20 mL 水,微热溶解后,放冷,加 2 mL 乙酸盐缓冲液(pH3.5), 用水稀释成 25 mL,若该溶液带颜色,可在甲管中滴加少量的稀焦糖溶液或其他无干扰的有 色溶液,使之与乙管一致;再在甲乙两管中分别加硫代乙酰胺试液各 2 mL,摇匀,放置 2min, 同置白纸上,自上向下透视,乙管中显出的颜色与甲管比较,不得更深。
砷的测定(砷斑法)称取 1g±0.01g 实验室样品,加盐酸试剂 5mL,再加水至 30 mL 溶解后,按 GB/T 5009.76 砷斑法测定,量取 2mL±0.02mL 砷标准溶液(含砷 2.0 μg),制备砷限量标准。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国