扎那米韦(zanamivir)化学名为5-乙酰氨基-4-[(氨基亚氨基甲基)-氨基]-2,6-脱水-3,4,5-三去氧-D-丙三醇基-D-半乳糖-2-烯醇酸,无色结晶固体,分子式为C12H20N4O7,分子量为332.31000,密度为1.75 g/cm,熔点为256ºC (dec.)。
化合物简介基本信息中文名称:扎那米韦
英文名称:zanamivir
英文别名:GG167;ZanamivirHydrate;4-Guanidino-2,4-dideoxy-2,3-dehydro-N-acetylneuraminic acid;4-Guanidino-Neu5Ac2en;Zanamir;Unii-L6o3xi777i;
CAS号:139110-80-8
分子式:C12H20N4O7
分子量:332.31000
结构式: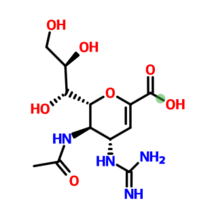
精确质量:332.13300
PSA:198.220001
物化性质外观与性状:无色结晶固体
密度:1.75 g/cm
熔点:256ºC (dec.)1
分子结构数据1、 摩尔折射率:71.55
2、 摩尔体积(cm/mol):189.6
3、 等张比容(90.2K):562.3
4、 表面张力(dyne/cm):77.3
5、 极化率(10-24cm3):28.362
生产方法将5-乙酰氨基-4,7,8,9-四-O-乙酰基-2,3,5-三脱氧-D-甘油基-D-半乳糖壬-2-烯吡喃糖醇溶于苯和甲醇中,在室温和搅拌下,滴加BF3Et2O,加入乙酸乙酯,依次用饱和碳酸氢钠、水洗、浓缩,加入水和乙酸,搅拌。加入乙酸乙酯,用5%碳酸氢钠、水洗、浓缩。得到的物质硅胶柱层析,得4位O-乙酰基水解产物。该化合物溶于无水二氯甲烷和吡啶,滴加含三氟甲磺酸酐的二氯甲烷溶液,搅拌。减压浓缩至干,得到的物质溶于含叠氮钠和四丁基硫酸氢铵的二甲基甲酰胺溶液,在室温搅拌。减压浓缩至干,得到的物质加入乙酸乙酯和水,分出有机层,水洗、干燥、浓缩。得到的物质硅胶柱层析,得4位叠氮化产物。该化合物溶于吡啶,在室温用硫化氢鼓泡,通入氮气。减压蒸出吡啶,得到的物质硅胶柱层析,得4位还原为氨基的产物。在冰浴冷却下,将该化合物加到含犛甲基硫脲的水中,反应后,放入离子交换树脂柱中,先用冷水洗, 再用氨水展开。得到的流出液经减压浓缩至干,得到的物质用硅胶柱层析,得扎那米韦。1
用途用于治疗A型和B型流感。神经氨酸酶抑制剂。该品通过抑制流感病毒的神经氨酸酶,从而改变了流感病毒在感染细胞内的聚集和释放。适用于流感症状出现不到2天的成人或12岁以上青少年的A型或B型流感病毒引起的无并发症的急件感染的治疗。1
化合物相关药品药品名称:【通用名称】 扎那米韦吸入粉雾剂
【商品名称】 依乐韦
【英文名称】 Zanamivir Powder for Inhalation
【汉语拼音】 Zha Na Mi Wei Xi Ru Fen Wu Ji3
成份:本品主要成份为扎那米韦。化学名称:5-乙酰氨基-4-[(氨基亚氨基甲基)-氨基]-2,6-脱水-3,4,5-三去氧-D-丙三醇基-D-半乳糖-2-烯醇酸。分子式:C12H20N4O7,分子量:332.33
所属类别:化药及生物制品 >> 抗微生物药 >> 抗病毒药 >> 其他抗病毒药 3
性状:本品为泡囊型吸入粉雾剂,内容物为白色或类白色粉末。3
适应症:用于成人和7岁及7岁以上儿童的甲型和乙型流感治疗。治疗应尽早开始,且不应晚于感染初始症状出现后48小时(见【注意事项】)。治疗甲型和乙型流感时,抗病毒药物非必需使用的药物,因此使用本品治疗流感时,应慎重考虑其必要性。3
规格:5mg/泡(以扎那米韦计)3
用法用量:每日2次,每次两吸(2×5mg),连续5天,每天的总吸入剂量为20mg。为达到最大治疗效果,症状出现后尽快开始治疗(没有资料支持在流感症状出现48小时候应用本品会有效)。本品在给药方式为经口吸入,使用提供的碟形吸入器--旋达经口吸入肺部给药。如果患者在使用本品同时要应用其他吸入药物,如速效支气管扩张剂,请再使用本品前使用其他药物(见【注意事项】)。3
肾功能不全患者
无需调整剂量(见【药代动力学】)。
肝功能不全患者
扎那米韦在肝脏不被代谢,因此无需调整剂量(见【药代动力学】)。
老年患者
老年患者(≥65岁)使用扎那米韦的经验有限。但是基于扎那米韦的药代动力学特性,无需调整用药剂量(见【药代动力学】)。
儿童
无需调整剂量(见【药代动力学】)。当儿童使用扎那米韦时,应在成年人监护下使用。3
不良反应:虽仅批准本品用于甲型和乙型流感的治疗,但从未临床用药提供更多安全性信息,确保临床用药安全角度考虑,本项内容纳入了本品在国外进行的预防性研究的安全信息。
药物临床试验中不良反应的发生率可能不能反映实际情况下不良反应的发生率。本品临床试验使用的空白对照由吸入乳糖粉末组成,也是活性药物的溶媒;因此在不同治疗组出现的相似的不良反应发生频率可能与乳糖溶媒的吸入相关。
流感治疗
成人和青少年患者临床试验:发生率≥1.5%的不良事件情况详见表1。该表显示12岁及以上人群接受扎那米韦10mg每日两次治疗,接受扎那米韦所有给药方案和空白对照的不良事件发生情况(安慰剂与扎那米韦之际采用相同的乳糖载体)。
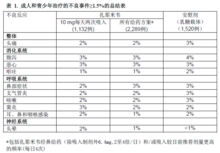
接受扎那米韦给药患者的其他不良反应发生率




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国