简介
在面板数据线性回归模型中,如果对于不同的截面或不同的时间序列,只是模型的截距项是不同的,而模型的斜率系数是相同的,则称此模型为固定效应模型。除了固定效应模型,典型的面板数据分析方法还有随机效应模型和混合效应模型。固定效应模型(FEM)假设所有的纳入研究拥有共同的真实效应量,而随机效应模型(REM)中的真实效应随研究的不同而改变。基于不同模型的运算,所得到的合并后的效应量均数值也不相同。早在1976年,第一篇Meta分析就使用FEM进行了数据合并,基于其统计简洁性及异质性认知,致使FEM广泛使用,直到2006年仍然有四分之三的Meta分析的文章在使用。然而,随着方法学不断更新及异质性理解,方法学家们对于证据合并内在结构理解与剖析,已开始逐渐对“理想”状态的FEM产生疑问。随后,REM逐渐被使用,并替代部分FEM。
分类固定效应模型可分为三类:
(1)个体固定效应模型:个体固定效应模型是对于不同的时间序列(个体)只有截距项不同的模型:

从时问和个体上看,面板数据回归模型的解释变量对被解释变量的边际影响均是相同的,而目除模型的解释变量之外,影响被解释变量的其他所有(未包括在回归模型或不可观测的)确定性变量的效应只是随个体变化而不随时间变化。
(2)时点固定效应模型:时点固定效应模型就是对于不同的截面(时点)有不同截距的模型。如果确知对于不同的截面,模型的截距显著不同,但是对于不同的时间序列(个体)截距是相同的,那么应该建立时点固定效应摸型:
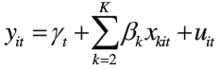
(3)时点个体固定效应模型:时点个体固定效应模型就是对于不同的截面(时点)、不同的时间序列(个体)都有不同截距的模型。如果确知对于不同的截面、不同的时间序列(个体)模型的截距都显著不相同,那么应该建立时点个体固定效应模型:
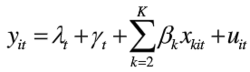
于随机效应模型的比较从定义的角度FEM:假设所有纳入的研究拥有共同的真实效应量,或者除了随机误差外,所观察效应量均为真实效应量。如比较对糖尿病黄斑水肿(DME)的抗血管内皮生长因子(Anti-VEGF)药物中aflibercept与bevacizumab疗效,除了药物自身疗效外,其他患者背景、药物使用情况及测量结局的工具等均“一致”,每个研究的观察效应量差别仅仅是由于抽样误差引起,也就是说,每个研究的观察效应量就“等于”其真实效应量。Cochrane Handbook已明确指出,当异质性小于40%,建议采用FEM进行Meta合并,因此,FEM对各研究背景较为苛刻,仅适用于“理想化”研究背景。
REM:如上所诉,FEM中假设所有研究的真实效应量是相同的,但在大多数的系统评价和Meta分析中这是很难实现的。因为研究的对象很难保存同质性,所以在REM中的真实效应量会随着不同的研究所改变,例如一个研究的效应量可能比拥有不同年龄、教育背景、健康程度等参与者的研究的效应量更高或更低,所以真实效应量的大小不仅取决于样本的抽样误差,还取决于参与者或研究对象以及进行的干预措施等,也可称其为异质性。
基于统计学角度FEM:假设纳入研究拥有共同的真实效应量,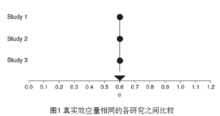 如图1中圆圈所示,各研究合并的真实效应量(θ)用倒三角表示。可以发现,对于FEM,所有研究真实效应量都是相同的。每个研究的样本量并非无限的,所以都会存在抽样误差(ε),从而导致了各研究的观察效应量(Y)不等于真实效应量(如图2中正方形所示),并且随着研究的不同而不同,可以用公式
如图1中圆圈所示,各研究合并的真实效应量(θ)用倒三角表示。可以发现,对于FEM,所有研究真实效应量都是相同的。每个研究的样本量并非无限的,所以都会存在抽样误差(ε),从而导致了各研究的观察效应量(Y)不等于真实效应量(如图2中正方形所示),并且随着研究的不同而不同,可以用公式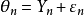 表示。
表示。
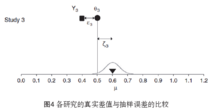
REM:在图3中,由于每个研究人群的背景、年龄、教育程度、地理环境的因素的不同,导致各个真实效应量也完全不同(成正态分布),同时也不同于合并的真实效应量(μ),把两者之间的差值叫做真实差值,并用ζ表 示(如图4)。由于抽样误差的成在,相互之间的观察效应量或多或少于真实效应量,例如图4中的Study3,观察效应量小于真实效应量,而真实效应量又小于合并的真实效应量,所以在REM中,合并后的真实效应量由两种因素决定,即真实差值和抽样误差,可用下列公式表示
示(如图4)。由于抽样误差的成在,相互之间的观察效应量或多或少于真实效应量,例如图4中的Study3,观察效应量小于真实效应量,而真实效应量又小于合并的真实效应量,所以在REM中,合并后的真实效应量由两种因素决定,即真实差值和抽样误差,可用下列公式表示 。
。
基于权重分配的角度在Meta分析中,为了减少误差获得更加准确的结果,每种模型的计算各不相同,主要体现在各个研究权重值的分配上,这也是两种效应模型的根本的区别所在。
FEM:在这种模型中,权重的分配主要依赖其精确度,每个研究的权重等于方差的倒数(W=1/V),样本量越大,效应量的方差就越大,那么相应的权重分配就越多。因此大样本的研究对总合并后效应量的贡献值相对于小样本研究就更大,导致小样本研究更容易被忽略,分配的权重也就更少。
REM:与FEM不同,REM的总效应量是各个研究真实效应量的均数值,并非只注重大样本量的研究,而是为了平衡每个研究的效应量注重所有纳入的研究1。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国