三氟化钴(Cobalt(III) fluoride)是一种化学药品,也称为氟化钴(III),分子式为CoF3,分子量为115.93。
室温下为不稳定的浅棕色易潮解固体,是很常用的氟化剂。
物化性质三氟化钴(化学式:CoF3),室温下为不稳定的浅棕色易潮解固体,密度为3.88g/mL(25℃),溶于水放出氧气,是很常用的氟化剂。在CO2气流中加热到250℃时,开始放出F2,在350℃时,则完全转变为CoF2。
与氟同族的氯也可生成钴的二元化合物,但很不稳定,三氧化二钴溶于盐酸时便会有氯气放出。溴化钴及碘化钴从未制得。
三氟化钴可以与许多金属或非金属单质反应生成相应的氟化物,自身被还原为二氟化钴。三氟化钴也有水合物,CoF3·3.5H2O,但结构尚不清楚。
用三氟化钴氟化有机化合物时,首先用二氟化钴与氟气在300℃左右反应生成三氟化钴,然后引入有机反应物与三氟化钴反应。三氟化钴被还原后生成的二氟化钴可以循环使用。氟化反应包含单电子转移及碳正离子中间体机理:
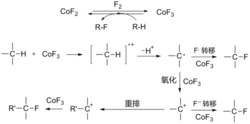
该反应通常用于全氟有机物的制取。三氟化钴的氧化性较强,一般反应都在气相、无溶剂或以无水氟化氢作介质中进行,常伴有重排或其他副反应的发生,用相关的KCoF4氟化可使反应的选择性增强。400℃左右时所有碳氢化合物的C-H键都可被转化为C-F键,并且氟也可以加到不饱和键上。
2CoF3+ R-H → CoF2+ R-F + HF
制取氯化钴(II)或氟化钴(II)与氟气在250°C时发生快速放热反应生成三氟化钴固体:
2CoCl2+ 3F2→ 2CoF3+ 2Cl21
此外,用三氟化氯来氟化金属钴或一氧化钴与氟气反应也可得到三氟化钴。它为六方晶系,与氟化铁和氟化铝同晶,是一个高自旋配合物。具潮解性,可被转化为[CoF6]3-离子,是少见的高自旋八面体钴配合物之一。
具体实验步骤如下:
将盛有CoF2的石英舟放入石英反应管中,从反应管的一端通入F2,反应开始进行得很慢,当将反应管加热至75℃左右时,由于反应放热,反应就猛烈起来,温度慢慢升至200℃,产物在F2气流中冷却;最后用氮气流驱除多余的F2。氟化反应与在前面相同的装置中进行,石英舟中为无水CoCl2或Co2O3,将反应管从室温开始渐渐升温至300℃,保持此温度直至反应管的末端有F2放出为止,然后用干燥的氮气将装置中多余的F2驱除出去。2
用途CoF3可与水发生反应,是非常强的氟化剂和氧化剂,被广泛用作氟化剂。用于有机氟化合物(尤其是全氟化合物)的制取,还原产物是二氟化钴。类似可以用作氟化试剂的金属氟化物还有三氟化锰、二氟化银等。3
储运运输库房低温,通风,干燥;密闭保存,防潮。
计算化学数据1、疏水参数计算参考值(XlogP):无
2、氢键供体数量:0
3、氢键受体数量:3
4、可旋转化学键数量:0
5、互变异构体数量:无
6、拓扑分子极性表面积:0
7、重原子数量:4
8、表面电荷:0
9、复杂度:0
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:42
本词条内容贡献者为:
唐浩宇 - 教授 - 湘潭大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国