历史
第零定律比起其他任何定律更为基本,但直到二十世纪三十年代前一直都未有察觉到有需要把这种现象以定律的形式表达。第零定律是由英国物理学家拉尔夫·福勒于1939年正式提出,比热力学第一定律和热力学第二定律晚了80余年,但是第零定律是后面几个定律的基础,所以叫做热力学第零定律。
概要一个热平衡系统的宏观物理性质(压强、温度、体积等)都不会随时间而改变。一杯放在餐桌上的热咖啡,由于咖啡正在冷却,所以这杯咖啡与外界环境并非处于平衡状态。当咖啡不再降温时,它的温度就相当于室温,并且与外界环境处于平衡状态。1
两个互相处于平衡状态的系统会满足以下条件:
两者各自处于平衡状态;
两者在可以交换热量的情况下,仍然保持平衡状态。进而推广之,如果能够肯定两个系统在可以交换热量的情况下物理性质也不会发生变化时,即使不容许两个系统交换热量,也可以肯定互为平衡状态。
因此,热平衡是热力学系统之间的一种关系。数学上,第零定律表示这是一种等价关系。(技术上,需要同时包括系统自己亦都处于热平衡。)
内容热力学第零定律的重要性在于它给出了温度的定义和温度的测量方法。定律中所说的热力学系统是指由大量分子、原子组成的物体或物体系。它为建立温度概念提供了实验基础。这个定律反映出:处在同一热平衡状态的所有的热力学系统都具有一个共同的宏观特征,这一特征是由这些互为热平衡系统的状态所决定的一个数值相等的状态函数,这个状态函数被定义为温度。而温度相等是热平衡之必要的条件。2
通常表述热力学中以热平衡概念为基础对温度作出定义的定律。通常表述为:与第三个系统处于热平衡状态的两个系统之间,必定处于热平衡状态。图中A热力学第零定律示意图、B热力学第零定律示意图、C热力学第零定律示意图为3个质量和组成固定,且与外界完全隔绝的热力系统。将其中的B、C用绝热壁隔开,同时使它们分别与A发生热接触。待A与B和A与C都达到热平衡时,再使B与C发生热接触。这时B和C的热力状态不再变化,这表明它们之间在热性质方面也已达到平衡。第零定律表明,一切互为热平衡的系统具有一个数值上相等的共同的宏观性质──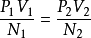 。
。
另一种表述处于热力学平衡状态的所有物质均具有某一共同的宏观物理性质。
适用范围第零定律是在不考虑引力场作用的情况下得出的,物质(特别是气体物质)在引力场中会自发产生一定的温度梯度。如果有封闭两个容器分别装有氢气和氧气,由于它们的分子量不同,它们在引力场中的温度梯度也不相同。如果最低处它们之间可交换热量,温度达到相同,但由于两种气体温度梯度不同,则在高处温度就不相同,也即不平衡。因此第零定律不适用引力场存在的情形。这与限定第二类永动机不成立的第二定律类似。3
温度关系第零定律经常被认为可以建立一个温度函数;更随便的说法是可以制造温度计。而这个问题是其中一个热力学和统计力学哲学的题目。1
在热力学变量的函数空间之中,恒温的部分会成为一块面并会为附近的面提供自然秩序。之后,该面会简单建立一个可以提供连续状态顺序的总体温度函数。该恒温面的维度是热力学变量的总数减一(例如对于有三个热力学变量 P、V、n 的理想气体,其恒温面是块二维面)。按此定义的温度实际上未必如摄氏温度尺般,而是一个函数。
以理想气体为例,若两团气体是处于热平衡,则:
Pi 是第 i 个系统的压强Vi 是第 i 个系统的体积Ni 是第 i 个系统的数量(摩尔数或者原子数目)面 PV / N = const 定义了所有相同温度的面,一个常见方法来标签这些面是令 PV / N = RT,R 是一个常数而温度 T 可以由此定义。经定义后,这些系统可用作温度计来较准其他系统。
多系统间平衡一个简单例子可以说明为什么需要到第零定律。如前所述,当两个系统间有小量广延量交换时(如微观波动)而两者的总能量不变时(能量减少不能逆转),此两个系统即处于平衡。
简单起见,N个系统与宇宙的其他部分绝应隔离,每一个系统的体积与组成都保持恒定,而各个系统之间都只能交换热量(熵)。此例子的结果可直接延伸至体积或积量的交换。
热力学第一与第二定律的结合把总能量波动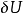 与第 i个系统的温度
与第 i个系统的温度 及熵的波动
及熵的波动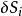 联系成:
联系成:
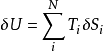 与宇宙其他部分绝热隔离,N个系统熵的总和必须为零。
与宇宙其他部分绝热隔离,N个系统熵的总和必须为零。
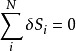
换句话说,熵只能在 N个系统之间交换。这个限制可以用来重写总能量波动的表达式成:
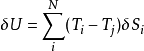
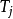 是N个系统中任何一个系统 j的温度。最后到达平衡时,总能量波动必须为零,因此:
是N个系统中任何一个系统 j的温度。最后到达平衡时,总能量波动必须为零,因此:
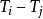 这条方程可被设想成反对称矩阵与熵波动矢量之乘积为零。若要令一个非零解存在,则:
这条方程可被设想成反对称矩阵与熵波动矢量之乘积为零。若要令一个非零解存在,则:
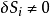
无论是那一个 j的选择,由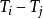 组成之矩阵的行列式值必定归零。
组成之矩阵的行列式值必定归零。
但是,根据雅可比定理,一个N×N反对称矩阵若N为奇数时,则其行列式值必为零;而若N为偶数时,则每一项 必须为零以令行列式值为零,亦即各个系统处于平衡状态
必须为零以令行列式值为零,亦即各个系统处于平衡状态 。此结果显示,奇数数目的系统必定处于平衡状态,而各系统的温度和熵波动则可以忽略不计;熵波动存在时,只有偶数数目的系统才须要各系统的温度相等以达致平衡状态。
。此结果显示,奇数数目的系统必定处于平衡状态,而各系统的温度和熵波动则可以忽略不计;熵波动存在时,只有偶数数目的系统才须要各系统的温度相等以达致平衡状态。
热力学第零定律解决了此奇偶矛盾。考虑N个系统中的任何三个互为平衡的系统,其中一个就系统可以按照第零定律而被忽略。因此,一个奇数数数的系统就可以约简成一个偶数数目的系统。此推导使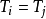 为平衡的必须条例。
为平衡的必须条例。
相同结果,可以应用到任何广延量中的波动如体积(相同压强)、或质量(相同化势)。因而,第零定律的所涉及的就不单只是温度罢了。
总的来说,第零定律打破了第一定律和第二定律内的某种反对称性。
意义热力学第零定律用来作为进行体系测量的基本依据,其重要性在于它说明了温度的定义和温度的测量方法。表述如下:
1.可以通过使两个体系相接触,并观察这两个体系的性质是否发生变化而判断这两个体系是否已经达到热平衡。
2.当外界条件不发生变化时,已经达成热平衡状态的体系,其内部的温度是均匀分布的,并具有确定不变的温度值。
3.一切互为平衡的体系具有相同的温度,所以一个体系的温度可以通过另一个与之平衡的体系的温度来表示,也可以通过第三个体系的温度来表示。
ps:初中物理公式,热学部分:1,吸热:Q吸=Cm(t-t0)=Cmt;2,放热:Q放=Cm(t0-t)CMt;3,热力学温度:T=t+273k。在大学物理中Cm与温度t有关。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国