概念
工程计算中提出相对挥发度的概念,目的是寻求用简单方法表示气液平衡关系。溶液中组分的挥发度是随温度而变的,故引入相对挥发度的概念。将溶液中易挥发组分的挥发度与难挥发组分的挥发度之比,称为相对挥发度,以αAB或α表示,则1
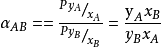
式中,yA ——气相中易挥发组分的摩尔分数;yB——气相中难挥发组分的摩尔分数;
xA——液相中易挥发组分的摩尔分数;xB——液相中难挥发组分的摩尔分数。
具体推导液体混合物中两组分的相平衡比的比值。组分 A对组分B的相对挥发度xAB可表示为:
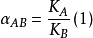
式中KA和KB分别为组分A和B的相平衡比(见传质分离过程)。同一混合液中,挥发性大的组分,一般相平衡比大,故易挥发组分对难挥发组分的相对挥发度大于1;反之则小于1。根据相平衡比的定义,式(1)可改写为:

式中yA和xA分别为组分A在汽相和液相中的摩尔分率;yB和xB分别为组分 B在汽相和液相中的摩尔分率。对于由组分A和B组成的双组分混合液,yA=1-yB,xA=1-xB。据此可以导得:
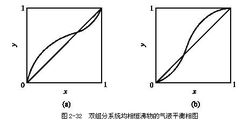
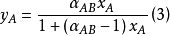 (3)式表明:如果αAB大于1,则yA大于xA,即汽相中组分A得以增浓,A为易挥发组分。αAB比1大得愈多,则yA比xA也大得愈多;如αAB小于1,则yA小于xA,也即组分B在汽相得到增浓,B为易挥发组分。αAB比1小得愈多,则B在汽相中的增浓愈显著。当αAB等于1时,则yA等于xA,这表明用蒸馏方法不能分离此混合液。因此αAB与1偏离的程度是蒸馏操作分离液体混合物难易程度的标志。
(3)式表明:如果αAB大于1,则yA大于xA,即汽相中组分A得以增浓,A为易挥发组分。αAB比1大得愈多,则yA比xA也大得愈多;如αAB小于1,则yA小于xA,也即组分B在汽相得到增浓,B为易挥发组分。αAB比1小得愈多,则B在汽相中的增浓愈显著。当αAB等于1时,则yA等于xA,这表明用蒸馏方法不能分离此混合液。因此αAB与1偏离的程度是蒸馏操作分离液体混合物难易程度的标志。
当混合物中液相为理想溶液且汽相为理想气体时,应用拉乌尔定律和道尔顿分压定律,可由式(2)导出:
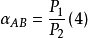 式中p1和p2分别为组分A和B的饱和蒸气压。此时相对挥发度为两组分的饱和蒸气压(纯组分挥发性的一种度量)之比。对于理想系统,相对挥发度与混合液的组成和温度关系很小,工程上可视为常数。但强非理想系统的浓度对相对挥发度有较大的影响。此外,在工业上有时还在混合液中加入某种添加物来增大待分离组分间的相对挥发度,使难以用普通蒸馏分离的混合液变得易于进行分离。这就是萃取精馏、恒沸精馏和加盐精馏等特殊精馏的基本依据。
式中p1和p2分别为组分A和B的饱和蒸气压。此时相对挥发度为两组分的饱和蒸气压(纯组分挥发性的一种度量)之比。对于理想系统,相对挥发度与混合液的组成和温度关系很小,工程上可视为常数。但强非理想系统的浓度对相对挥发度有较大的影响。此外,在工业上有时还在混合液中加入某种添加物来增大待分离组分间的相对挥发度,使难以用普通蒸馏分离的混合液变得易于进行分离。这就是萃取精馏、恒沸精馏和加盐精馏等特殊精馏的基本依据。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国