分解电压,即指使电解质在电极上分解生成电解产物所需施加的最小电压。
概念分解电压(decomposition voltage),指使电解质在电极上分解生成电解产物所需施加的最小电压。电解质的分解电压由其电解产物组成的原电池电动势、阴阳二电极的极化过电位和电路压降三部分组成。
电解质发生电解时,二电极上的电解产物形成原电池,其电动势方向与电解方向相反,外加电压首先得克服这种电动势。此反向电动势的大小,等于二电极的平衡电位差。此即为电解质的理论分解电压。
在理论分解电压下,电极上电解过程和原电池过程处于动平衡状态,不会出现宏观的电解产物。当提高外加电压至超过理论分解电压一定值,即电极达到一定极化时,便可观察到电解产物不断形成,电解过程便由此开始。此时的极化电极的电位与其平衡电位之差,就是极化超电位。极化超电位是外加电压中用来推动电极反应向电解方向单向地进行的部分。而电路压降地电解回路中各处电阻造成的电压损失,等于电流与各电阻的乘积之总和,需由外加电压补偿。
例如电解0.5mol/LH2SO4,通电时两极发生的半反应是:
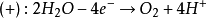
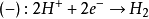
两极产生的氢气和氧气被铂电极吸附后,实际上就构成了氢电极和氧电极。这两个电极产生一个跟外加电压方向相反的电动势(叫反电动势)。因此要使电解顺利进行,外加电压必须大于反电动势,这就是分解电压产生的原因。电解时由于两个电极都存在超电势,使阳极的电极电势增大,阴极的电极电势减小,因此实际的反电动势要大于理论反电动势,使电解质的分解电压增大,电解时耗的电量增加。
测定电解质的分解电压(实际分解电压)由实验测定,同一电解质在不同电流密度和电极材料等情况下测得的分解电压也不同。电路中随加外电压的提高电流突然陡升的那个电压就是该电解质在给定条件的分解电压。1
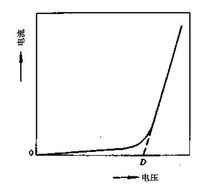
分解电压和超电压分解电压与理论分解电压之间的差称为超电压。电解过程中超电压的产生和两极反应的超电压有关,它直接受极板材料和析出物质的种类影响。
例如,电解CuSO4溶液,阴极产物是Cu。这与根据电极电势判断的结论是一致的。
以Zn为电极电解ZnSO4的水溶液时,根据电极电势判断的结论是在阴极产生H2,而实际上是Zn在极板上析出。原因就是H2在Zn极板上析出时的超电压很大(-0.77V),而Zn的标准电极电势为-0.76V,比H2在锌上的超电势数值大,所以Zn会优先析出,在极板上沉积。
更活泼金属的电解产物通常符合标准电极电势的判断。 以电解MgSO4为例,Mg(H2O)62+的标准电极电势为-2.37V,值过于小,即使考虑超电压进行修正后H+的电极电势依然远高于Mg的电极电势,故电解MgSO4的水溶液时仍得到H2。
电解中存在诸如超电势这样的动力学问题,不能仅根据热力学数据就下结论。
本词条内容贡献者为:
何星 - 副教授 - 上海交通大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国