生物光学标记(bio-optical marker)是指用具有光学特征的标记物标记生物分子,从而达到检测、识别的目的。根据应用的光学特征不同通常可分为荧光分子标记、荧光蛋白标记、生物发光标记、化学发光标记等。从标记目的来分则包括生物分子标记、生化标记、细胞学标记、形态学标记等。
概述生命分子检测、生命过程观测、特定生物组织识别,由于其微观、隐蔽通常难以直接观测到,甚至也超出了仪器的检测范围,因此必须在生物分子或细胞、组织上作特定的生物标记,使其能够‘脱颖而出’,再借助于相应的仪器实现检测。
在特定生物分子、细胞或组织上标记目前检测手段可探测感知的分子、纳米粒子,然后通过检测该分子/粒子的数量、分布等来获取特定分子、细胞或组织的特征,进而获得某一区域以及细胞或生物体内分子、生化及生理指标的反应及其信号。这个标记过程通常称为生物标记(Biomarker)。生物光学标记(bio-optical marker)则是指用具有光学特征的标记物标记生物分子,从而达到检测、识别的目的。根据应用的光学特征不同通常可分为荧光分子标记、荧光蛋白标记、生物发光标记、化学发光标记等。从标记目的来分则包括生物分子标记、生化标记、细胞学标记、形态学标记等。
生物光学标记,因为采用了光学的方式,借助于发展成熟的光学高灵敏检测仪器可以实现高对比度、高解像度、高灵敏、高信噪比、方便快捷的检测,在生物标记发展之初就被选作为主要的生物标记方式。特别是荧光蛋白被发现之后,生物光学标记更是获得了突飞猛进的应用发展。下村修(Osamu Shimomura)、马丁·查尔菲(Martin Charfie)与钱永健(Roger Tsien) 也正是因为发现和研究了绿色荧光蛋白获得了2008年的诺贝尔化学奖。 生物光学标记现已在生命科学和医学研究中被广泛用作示踪物。
研究应用历史在生物学研究中,科学家们常常利用能发射荧光的荧光分子来作为生物标记。将这种荧光分子通过化学方法挂在其他不可见的分子上,原来不可见的部分就变得可见了。生物学家一直利用这种标记方法,把原本透明的细胞或细胞器从黑暗的显微镜视场中“揪出来”。
传统的荧光分子在发光的同时,会产生具有毒性的氧自由基,导致被观察的细胞死亡,这叫做“光毒性”,因此,在绿色荧光蛋白发现以前,科学家们只能通过荧光标记来研究死亡细胞静态结构,或者不得不暂时忽略其毒性影响,只在短时间观测活细胞,而荧光蛋白的光毒性非常弱,非常适合用于标记各种活细胞。
荧光蛋白最初在1962年于一种学名Aequorea victoria的水母中发现。其基因所产生的蛋白质,在蓝色波长光线的激发下,会发出绿色萤光。这个发光的过程中还需要发光蛋白Aequorin的帮助,且这个蛋白质还需要与钙离子(Ca)产生交互作用。
绿色荧光蛋白的光毒性非常弱,非常适合用于标记活细胞。然而,绿色荧光蛋白被发现20多年后,才有人将其应用在生物样品标记上。1993年,马丁·沙尔菲成功地通过基因重组的方法使得除水母以外的其他生物(如大肠杆菌等)也能产生绿色荧光蛋白。他不仅证实了绿色荧光蛋白与活体生物的相容性,还建立了利用绿色荧光蛋白研究基因表达的基本方法,而许多现代重大疾病都与基因表达的异常有关。
后来,美籍华人钱永健系统地研究了绿色荧光蛋白的工作原理,并对它进行了大刀阔斧的化学改造,不但大大增强了它的发光效率,还发展出了红色、蓝色、黄色荧光蛋白,使得荧光蛋白真正成为了一个工具箱,供生物学家们按需要选用。目前生物实验室普遍使用的荧光蛋白,大部分是钱永健改造的变种。
有了这些荧光蛋白,利用光学的仪器,科学家们就好像在细胞内装上了“灯塔”,得以实时监测各种生命的过程。通过沙尔菲的基因克隆思路,迄今科学家们还培育出了荧光老鼠和荧光猪。
另外,除了上述的荧光分子和荧光蛋白标记外,2000年以来,随着生物纳米技术的发展,一些新型的、具有生物兼容性的光学纳米标记物也被研究开发出来,如上转换纳米粒子、量子点、长延时荧光粒子等都被研究和利用。用作细胞、活体的生物标记,作为生物光学成像 “传感”的有力武器。
生物光学标记种类及应用荧光分子/纳米粒子标记Fluorescent molecular/nanoparticle marker
荧光分子包括有机试剂或金属螯合物;荧光纳米粒子则有上转换、量子点等。其在紫外-可见-近红外区有较强的特征荧光,利用该分子/纳米粒子标记细胞、活体后,可实现光学的示踪检测等,或者该荧光探针的激发和发射波长、强度、寿命、偏振等荧光性质可随极性、折射率、黏度等所处环境性质改变而灵敏地改变,利用这一性质可进行生物检测。荧光分子/纳米粒子标记设计灵活、应用方便,在生物分子识别、细胞生理检测、活体特定组织光学成像等方面有着广泛的应用。
生物发光标记 Bioluminescence marker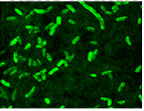
生物发光标记是用萤光素酶(Luciferase)基因标记细胞或 DNA的一种生物标记方法,标记后,细胞合成该萤光素酶,然后加入外源性的萤光素,在该酶的作用下,萤光素氧化后发光。该方法让研究人员能够直接监控活体生物体内的细胞活动和基因行为。通过这个系统,可以观测活体动物体内肿瘤的生长及转移、感染性疾病发展过程、特定基因的表达等生物学过程。因其操作极其简单、所得结果直观、灵敏度高等特点,已广泛应用于生命科学、医学研究及药物开发等方面。
荧光蛋白标记 Fluorescent protein marker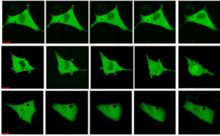
将荧光蛋白基因片段与目的基因连接后,转染进入细胞,待其正常表达后,在激发光下,利用荧光显微镜、流式细胞仪或者激光共聚焦显微镜即可对其进行观察检测。荧光蛋白有绿色荧光蛋白(GFP)、红色荧光蛋白(RFP),蓝色荧光蛋白(BFP)、黄色荧光蛋白(YFP)等。可对活细胞无害标记,长时间观测。因而广泛应用于转基因动物的研究、融合标记、基因治疗、蛋白在活细胞内功能定位及迁移变化、病原菌侵入活细胞的分子过程等。荧光蛋白作为新一代的基因转移报告物和/或定位标记物,在生命科学研究中越来越受到关注
化学发光标记 Chemiluminescence marker在待检测的分子(蛋白质、核酸等)上连接可激活发光的化合物的方法。也可以连接上半抗原(如地高辛精、生物素等),再用酶标记的抗半抗原抗体或抗生物素蛋白与之结合,结合于半抗原上的酶标记抗体或抗生物素蛋白能催化化学发光底物发生化学变化从而发光。如抗体分子以吖啶酯标记,加触发剂激活后发光,用于检测固相化的抗原。
发展前景借助于迅速发展的光学检测技术和成熟的光学成像仪器,生物光学标记从产生之初就表现出了强大的应用活力。其在分子检测、生物机制研究、肿瘤标记诊断等各个领域都有广泛的应用。生物光学标记技术为人们观察神秘的微观生物世界打开了一扇窗口,让人们能实实在在的“看”到以前看不到的生物过程和生命现象。生物光学技术方兴未艾,生物光学应用还有待进一步开拓。相信随着生物光学技术的发展,人们将能够在更小尺度、更精确地跟踪观测生命过程。
延伸阅读1. Zhang H, Wu S, Xing D, YAP Accelerates Aβ25-35-Induced Apoptosis through Upregulation of Bax Expression by Interaction with p73, Apoptosis, 16(8), 808-821 (2011).
2. Marjuki H, Mishin V P, Sleeman K, et al. Bioluminescence-Based Neuraminidase Inhibition Assay for Monitoring Influenza Virus Drug Susceptibility in Clinical Specimens[J]. Antimicrobial agents and chemotherapy, 57(11): 5209-5215, (2013).
3. Liu L, Zhang Z and Xing D, Cell death via mitochondrial apoptotic pathway due to activation of Bax by lysosomal photodamage, Free Radical Biology & Medicine, 51, 53-68 (2011)
4. Zhou A, Wei Y, Wu B, Chen Q, XingD, Pyropheophorbide A and c(RGDyK) Co-Modified Chitosan-Wrapped Upconversion Nanoparticle for Targeted Near-Infrared Photodynamic Therapy, Mol. Pharmaceut.9, 1580-1589 (2012).
5. Feng J, Zhang Y, and Xing D, Low-power laser irradiation promotes VEGF expression and vascular endothelial cell proliferation through the activation of ERK/Sp1 pathway, Cell. Signal. 24, 1116-1125 (2012).
6. Jin Y, Lee D H, Kim H Y, et al. In Vivo Bioluminescence Imaging for Prolonged Survival of Transplanted Human Neural Stem Cells Using 3D Biocompatible Scaffold in Corticectomized Rat Model[J]. PloS one, 9(9): e105129, (2014).
7. 刘静静, 胡晓俊, 李征然, 等. Luciferase2/mKate2 双报告基因对小鼠骨髓间充质干细胞的标记及活体光学成像研究[J]. 中山大学学报: 医学科学版, 35(3): 334-339, (2014).
8. 宗慎飞, 王著元, 杨晶, 等. 聚合物电解质包裹金核银壳纳米棒制备双模式光学细胞成像探针[J]. 科学通报, 58(7): 601-607, (2013).
9. 刘杰昊, 杨晓峰, 王玮, 等. 肿瘤靶向特异性光学分子探针的结构与设计策略[J]. 中国医学创新, (6), (2014).
本词条内容贡献者为:
魏言春 - 副研究员 - 华南师范大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国