研究历史发现历史
 钒先后被两次发现。第一次是在1801年由墨西哥城的矿物学教授节烈里瓦发现的。他发现它在亚钒酸盐样本中,这个样本就是Pb5(VO4)3Cl,由于这种新元素的盐溶液在加热时呈现鲜艳的红色,所以被取名为“爱丽特罗尼”,即“红色”的意思,并将这种物品送到巴黎。然而,法国化学家推断它是一种被污染的铬矿石,所以没有被人们公认。1
钒先后被两次发现。第一次是在1801年由墨西哥城的矿物学教授节烈里瓦发现的。他发现它在亚钒酸盐样本中,这个样本就是Pb5(VO4)3Cl,由于这种新元素的盐溶液在加热时呈现鲜艳的红色,所以被取名为“爱丽特罗尼”,即“红色”的意思,并将这种物品送到巴黎。然而,法国化学家推断它是一种被污染的铬矿石,所以没有被人们公认。1
 第二次发现是在1830年,瑞典化学家塞夫斯特伦2( Sefstrom.N.G,1787-1845)在研究斯马兰矿区的铁矿时,用酸溶解铁,在残渣中发现了钒。因为钒的化合物的颜色五颜六色,十分漂亮,所以就用古希腊神话中一位叫凡娜迪丝“Vanadis”的美丽女神的名字给这种新元素起名叫“Vanadium”。中文按其译音定名为钒。塞夫斯特伦、维勒、贝采里乌斯等人都曾研究过钒,确认钒的存在,但他们始终没有分离出单质钒。后来到了1830年写佛寺特勒木在由瑞典铁矿石提炼出的铁中发现了它,并肯定这是一种新元素称之为钒,他能够证明它是一种新的元素,并因此击败了一位与他竞争的化学家,来自在锡马潘(墨西哥)的沃勒(Friedrich Wöhler),他也在对另一种钒矿石进行研究。1
第二次发现是在1830年,瑞典化学家塞夫斯特伦2( Sefstrom.N.G,1787-1845)在研究斯马兰矿区的铁矿时,用酸溶解铁,在残渣中发现了钒。因为钒的化合物的颜色五颜六色,十分漂亮,所以就用古希腊神话中一位叫凡娜迪丝“Vanadis”的美丽女神的名字给这种新元素起名叫“Vanadium”。中文按其译音定名为钒。塞夫斯特伦、维勒、贝采里乌斯等人都曾研究过钒,确认钒的存在,但他们始终没有分离出单质钒。后来到了1830年写佛寺特勒木在由瑞典铁矿石提炼出的铁中发现了它,并肯定这是一种新元素称之为钒,他能够证明它是一种新的元素,并因此击败了一位与他竞争的化学家,来自在锡马潘(墨西哥)的沃勒(Friedrich Wöhler),他也在对另一种钒矿石进行研究。1
1840年,俄罗斯矿物工程师苏宾写道“含铜生铁、黑铜、铜锭是含钒合金,由于钒的存在,使它们具有较高的硬度”3。
1869年英国化学家罗斯科(Roscoe.H.E,1833-1915)用氢气还原二氧化钒,才第一次制得了纯净的金属钒,而且他证明了之前的金属样本其实是氮化钒(VN)。1
1939年,在俄罗斯的彼尔姆斯克的含铜砂岩中也发现了钒。
发展历史在发现钒这种金属后,人们慢慢了解到了它的性质,并开始将它应用到人们的生活当中。1882年,英国列·克鲁佐特钢铁公司用含钒1.1%的炼钢炉渣制得钒的磷酸盐,年产量约60t。用户是生产苯胺黑的染料厂。
在19世纪末20世纪初,俄罗斯开始利用碳还原法还原铁和钒氧化物,首次制备出钒铁合金(含V35%~40%)。1902~1903年俄罗斯进行了铝热法制取钒铁的试验。
1927年,美国的马尔登和赖奇用金属钙还原五氧化二钒(V2O5),第一次制得了含钒99.3%~99.8%的可锻性金属钒。
19世纪末,研究还发现了钒在钢中能显著改善钢材的机械性能,从而使钒在工业上才得到广泛应用。至20世纪初,人们开始大量开采钒矿。
到目前为止,世界上生产钒的矿石主要以钒钛磁铁矿为主,在俄罗斯、南非、中国、澳大利亚及美国等国家都有丰富的钒钛磁铁矿资源,此外在钒铀矿、铝土矿、磷岩矿、碳质页岩、石油燃烧灰渣、废催化剂等均可作为回收钒的资源
含量分布钒的踪迹遍布全世界。在地壳中,钒的含量并不少,平均在两万个原子中,就有一个钒原子,比铜、锡、锌、镍的含量都多,但钒的分布太分散了,几乎没有含量较多的矿床。在海水中,在海胆等海洋生物体内,在磁铁矿中,在多种沥青矿物和煤灰中,在落到地球的陨石和太阳的光谱线中,人们都发现了钒的踪影。钒是地球上广泛分布的微量元素,其含量约占地壳构成的0.02%,获取相对容易。
世界上已知的钒储量有98%产于钒钛磁铁矿。除钒钛磁铁矿外、钒资源还部分赋存于磷块岩矿,含铀砂岩,粉砂岩,铝土矿,含碳质的原油、煤、油页岩及沥青砂中。
世界钒钛磁铁矿的储量很大,并且集中在少数几个国家和地区,包括:独联体、美国、中国、南非、挪威、瑞典、芬兰、加拿大、澳大利亚,并且集中分布在南非洲、北美洲等地区。根据1988年美国矿业局统计资料表明,世界钒储量基础为1.6亿吨(以钒计)。按目前的开采量计算,世界现探明的钒资源可供开采150年。从储量基础看,南非占46%,独联体占23.6%,美国占13.1%,中国占11.6%,其它国家的总和不足6%。4
在南非,钒通常在钒磁铁矿的矿层中产生。这些矿层的平均品位为1.5%。据估计,南非钒储量约为1250万吨,世界第一。
矿物有钒酸钾铀矿、褐铅矿和绿硫钒矿、石煤矿等。中国是钒资源比较丰富的 国家,钒储量为2055万吨(以V2O5计)主要赋存钒钛磁铁矿中,且集中分布在四川的攀枝花市、河北承德市。攀枝花钒储量为1295万吨,占中国钒储量的63%。4
国家,钒储量为2055万吨(以V2O5计)主要赋存钒钛磁铁矿中,且集中分布在四川的攀枝花市、河北承德市。攀枝花钒储量为1295万吨,占中国钒储量的63%。4
|| ||
物理性质钒是一种银灰色的金属。熔点1890±10℃,属于高熔点稀有金属之列。它的沸点3380℃,纯钒质坚硬,无磁性,具有延展性,但是若含有少量的杂质,尤其是氮,氧,氢等,能显著降低其可塑性。5
|| ||
晶体结构:晶胞为体心立方晶胞,每个晶胞含有2个金属原子。5
晶胞参数:
|| ||
化学性质基本性质钒的性质和钽以及铌相似,英国化学家罗斯科研究了它的性质,确定它与钽和铌相似,这为它们三个在元素周期表中共建一个分族建立了基础。钒属于中等活泼的金属,化合价+2、+3、+4和+5。其中以5价态为最稳定,其次是4价态,五价钒的化合物具有氧化性能,低价钒则具有还原性。钒的价态越低还原性越强。电离能为6.74电子伏特,具有耐盐酸和硫酸的本领,并且在耐气、耐盐、耐水腐蚀的性能要比大多数不锈钢好。钒空气中不被氧化,可溶于氢氟酸、硝酸和王水。6
|| ||
电离能(kJ /mol):
|| ||
化合物钒能分别以二、三、四、五价于氧结合,形成四种氧化物,一氧化钒,三氧化二钒,二氧化钒,五氧化二钒。他们的性质如下:
|| ||
高温下,金属钒很容易与氧和氮作用。当金属钒在空气中加热时,钒氧化成棕黑色的三氧化二钒、深蓝色的四氧化二钒,并最终成为桔黄色的五氧化二钒:
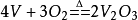
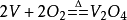
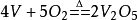
钒在氮气中加热至900~1300℃会生成氮化钒。钒与碳在高温下可生成碳化钒,但碳化反应必须在真空中进行。当钒在真空下或惰性气氛中与硅、硼、磷、砷一同加热时,可形成相应的硅化物、硼化物、磷化物和砷化物。不同价态的钒离子有不同的颜色:(VO2)+颜色为浅黄色或深绿色,(VO)2+颜色为蓝色,V3+为绿色,V2+为紫色。
钒盐我们平常说的钒盐是指这几种:含有V4+的,含有(VO3)-的(偏钒酸盐),含有(VO4)3-的(正钒酸盐),他们包括:偏钒酸铵、偏钒酸钠、偏钒酸钾、正钒酸钠、焦钒酸钠;四价盐:硫酸氧钒、草酸氧钒;四氯化钒等卤化钒类;三氯氧钒等卤氧化钒类。
钒的盐类的颜色真是五光十色,有绿的、红的、黑的、黄的, 绿的碧如翡翠,黑的犹如浓墨。如二价钒盐常呈紫色;三价钒盐呈绿色,四价钒盐呈浅蓝色,四价钒的碱性衍生物常是棕色或黑色,而五氧化二钒则是红色的。这些色彩缤纷的钒的化合物,被制成鲜艳的颜料:把它们加到玻璃中,制成彩色玻璃,也可以用来制造各种墨水。6
绿的碧如翡翠,黑的犹如浓墨。如二价钒盐常呈紫色;三价钒盐呈绿色,四价钒盐呈浅蓝色,四价钒的碱性衍生物常是棕色或黑色,而五氧化二钒则是红色的。这些色彩缤纷的钒的化合物,被制成鲜艳的颜料:把它们加到玻璃中,制成彩色玻璃,也可以用来制造各种墨水。6
同位素钒共有31种同位素,其中天然存在的是钒50和钒51,其他的全部通过人工合成。性质如下表:
|| ||
制备方法纯的金属钒一般是用钾在高压下将五氧化二钒还原而得到的。大多数钒是其它矿物加工时的副产品。工业上也可以以铝,焦炭还原五氧化二钒生产纯钒。7
焦炭还原五氧化二钒生产纯钒是将V2O5粉与高纯碳粉混合均匀,加10%樟脑乙醚溶液或酒精,压块后放入真空碳阻炉或感应炉内。炉内真空压力到6.66×10-1Pa后,升温至1573K,保温2h。冷却后将反应产物破碎。根据第一次还原产物的组分再配入适量碳化钒或氧化钒进行二次还原。二次还原炉内的真空压力为2.66×10-2Pa,温度控制在1973~2023K之间,并保温一段时间。真空碳还原法所得金属钒的成分(质量分数m/%)为:钒99.5,氧0.05,氮0.01,碳0.1。钒收率可达98%~99%。7
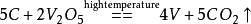
铝热还原法是将五氧化二钒和纯铝放在反应弹进行反应,生成钒铝合金。钒合金在2063K的高温和真空中脱铝,可制得含钒94%~97%的粗金属钒。4
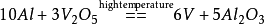
应用领域工业用途在钢中加入百分之几的钒,就能使钢的弹性、强度大增 ,抗磨损和抗爆裂性极好,既耐高温又抗奇寒,难怪在汽车、航空、铁路、电子技术、国防工业等部门,到处可见到钒的踪迹。此外,钒的氧化物已成为化学工业中最佳催化剂之一,有“化学面包”之 称。主要用于制造高速切削钢及其他合金钢和催化剂。把钒掺进钢里,可以制成钒钢。钒钢比普通钢结构更紧密,韧性、弹性与机械强度更高。钒钢制的穿甲弹,能够射穿40厘米厚的钢板。但是,在钢铁工业上,并不是把纯的金属钒加到钢铁中制成钒钢,而是直接采用含钒的铁矿炼成钒钢。8
称。主要用于制造高速切削钢及其他合金钢和催化剂。把钒掺进钢里,可以制成钒钢。钒钢比普通钢结构更紧密,韧性、弹性与机械强度更高。钒钢制的穿甲弹,能够射穿40厘米厚的钢板。但是,在钢铁工业上,并不是把纯的金属钒加到钢铁中制成钒钢,而是直接采用含钒的铁矿炼成钒钢。8
钒具有众多优异的物理性能和化学性能,因而钒的用途十分广泛,有金属“维生素”之称。最初的钒大多应用于钢铁,通过细化钢的组织和晶粒,提高晶粒粗化温度,从而起到增加钢的强度、韧性和耐磨性。后来,人们逐渐又发现了钒在钛合金中的优异改良作用,并应用到航空航天领域,从而使得航空航天工业取得了突破性的进展。随着科学技术水平的飞跃发展,人类对新材料的要求日益提高。钒在非钢铁领域的应用越来越广泛,其范围涵盖了航空航天、化学、电池、颜料、玻璃、光学、医药等众多领域。8
钒“现代工业的味精”,是发展现代工业、现代国防和现代科学技术不可缺少的重要材料。钒在冶金业中用量最大。从世界范围来看,钒在钢铁工业中的消耗量占其生产总量的85%。与此同时,钒在化工、钒电池、航空航天等其它领域的应用也在不断扩展,且具有良好发展前景。
钒在钢铁工业中主要用作合金添加剂,钢铁工业的发展变化对预测钒的需求至关重要。也就是说,钢铁对钒的需求趋势决定了钒工业的命运。
中国钢产量大约6亿吨,平均每吨钒的消费强度增加10g,折合五氧化二钒约为1.1万吨。而在美国,碳素钢和高强度低合金钢是钢铁工业中钒用量最大的钢种,占钢铁工业钒用量的60%以上,其次是高合金钢。
钒电池钒电池是目前发展势头强劲的优秀绿色环保蓄电池之一(它的制造、使用及废弃过程均不产生有害物质),它具有特殊的电池结构,可深度大电流密度放电;充电迅速;比能量高;价格低廉;应用领域十分广阔:如可作为大厦、机场、程控交换站备用电源;可作为太阳能等清洁发电系统的配套储能装置;为潜艇、远洋轮船提供电力以及用于电网调峰等。9
钒电池成本与铅酸电池相近,它还可制备兆瓦级电池组,大功率长时间提供电能,因此钒电池在大规模储能领域具有锂离子电池、镍氢电池不可比拟的性价比优势。钒电池生产工艺简单,价格经济,电性能优异,与制造复杂、价格昂贵的燃料电池相比,无论是在大规模储能还是电动汽车动力电源的应用前景方面,都更具竞争实力。9
与其它化学电源相比,钒电池具有明显的优越性,主要优点如下:1、功率大:通过增加单片电池的数量和电极面积,即可增加钒电池的功率,目前美国商业化示范运行的钒电池的功率已达6兆瓦。2、容量大:通过任意增加电解液的体积,即可任意增加钒电池的电量,可达吉瓦时以上;通过提高电解液的浓度,即可成倍增加钒电池的电量。3、效率高:由于钒电池的电极催化活性高,且正、负极活性物质分别存储在正、负极电解液储槽中,避免了正、负极活性物质的自放电消耗,钒电池的充放电能量转换效率高达75%以上,远高于铅酸电池的45%。4、寿命长:由于钒电池的正、负极活性物质只分别存在于正、负极电解液中,充放电时无其它电池常有的物相变化,可深度放电而不损伤电池,电池使用寿命长。目前商业化示范运行时间最长的钒电池模块已正常运行超过9年,充放循环寿命超过18000次,远远高于固定型铅酸电池的1000次。5、响应速度快:钒电池堆里充满电解液可在瞬间启动,在运行过程中充放电状态切换只需要0.02秒,响应速度1毫秒。6、可瞬间充电:通过更换电解液可实现钒电池瞬间充电。7、安全性高:钒电池无潜在的爆炸或着火危险,即使将正、负极电解液混合也无危险,只是电解液温度略有升高。8、成本低:除离子膜外,钒电池部件多为廉价的碳材料、工程塑料,材料来源丰富,易回收,不需要贵金属作电极催化剂,成本低。9、钒电池选址自由度大,可全自动封闭运行,无污染,维护简单,运营成本低。9
医疗用途钒是人体必需的微量元素在人体内含量大约为25mg,在体液pH4~8条件下 钒的主要形式为VO-3,即亚钒酸离子(metavandate);另一为+5价氧化形式VO4- 3即正钒酸离子(orthovanadate)。由于生物效应相似,一般钒酸盐(Va)统指这两种+5价氧化离子。VO-3经离子转运系统或自由进入细胞,在胞内被还原型谷胱甘肽还原成VO2+(+4价氧化态),即氧钒根离子(vanadyl)。由于磷酸和Mg2+离子在细胞内广泛存在VO-3与磷酸结构相似,VO2+与Mg2+大小相当(离子半径分别为160pm和165pm),因而二者就有可能通过与磷酸和Mg2+竞争结合配体干扰细胞的生化反应过程。例如,抑制ATP磷酸水解酶、核糖核酶磷酸果糖激酶、磷酸甘油醛激酶、6-磷酸葡萄糖酶、磷酸酪氨酸蛋白激酶。所以,钒进入细胞后具有广泛的生物学效应。钒化合物又具有合成相对容易、价格较低廉的优势,因此研究钒化合物的降压机制有利于对钒的开发和利用。
国内外对钒化合物的研究已有 20 多年的历史,早期多集中在钒化合物降糖作用的研究,也有报道钒能舒张猪的离体冠状动脉。近期国外有些研究开始用钒化合物治疗原发性高血压大鼠,已经取到肯定的实验结果。有报道认为 BMOV 可以降低 SHR 的高胰岛素血症和高血压。另有学者采用 SHR 和WKY 大鼠对比探讨钒化合物对血压的药物疗效,结果可见钒化合物使收缩压降低(149±3/mmHg,非治疗组184±3mmHgP




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国