氢化铀是一种毒性很强,棕灰色到棕黑色引火粉或脆性固体。 其在20℃的密度为10.95g/cm3,远低于铀(19.1g/cm3)。
结构立方晶系,cP32,空间群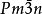 , β型氢化铀晶格常数a=664.3pm. 1
, β型氢化铀晶格常数a=664.3pm. 1
氢化铀存在两种晶体变体,均为立方晶系:在低温下获得的α型和当形成温度高于250℃时生长的β型。2 低温反应时生成α-UH3的亚稳相,其组成为UH3.00,黑色立方晶系晶体,a=416.0pm。在氢气中直到100℃还很稳定,但在250℃时,2~3h内就会转变为β-UH3。3
β-UH3为带有黑或棕色的深灰色结晶,属立方晶系,计算密度为10.92g/cm,用氦置换法测得其密度为10.95g/cm。具有UH3-x的非整比组成,如,450℃时,H/U=2.976~3.000,650℃时,H/U=2.837~2.929,700℃、5.07×103kPa时,H/U范围的下限值大幅度下降,820℃、8.4×103kPa时,H/U=0.7。在通常的合成条件下,制得的产物都具有近似于UH3的组成。离解压力为:
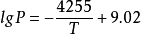
α和β晶型在低于180K时是铁磁性,高于180 K时,它们是顺磁性的。4
氢化铀不是一个填隙化合物,氢化后金属晶格扩大,在晶格中每个铀原子附近有6个铀原子和12个氢原子,氢占据较大的四面体缝隙。5氢在氢化铀中的密度大致与液态水或者液氢中相同。6氢化铀中存在U-H-U氢桥。
性质氢化铀具有金属导电性,微溶于盐酸和在硝酸中分解 。
氢化铀反应性很强。细粒UH3在空气中或氧中于-76℃可自燃;它与水发生剧烈反应,其程度取决于反应物的相对量和接触速度;与卤代有机溶剂的反应是危险的,非卤代有机溶剂不能溶解氢化铀或不发生反应;与热浓硫酸反应较快。与强氧化剂接触会导致火灾和爆炸。接触卤化碳会剧烈反应。
氢化铀离子可能会与某些干扰质谱测量,表现为以大众239的峰值,从而为钚-239信号的假性增高。7
制备2U+3H2=2UH3
铀暴露在氢气中会导致氢脆,氢气通过金属网格扩散形成氢化铀,氢化铀与铀之间存在明显的边界。通过真空中加热退火可以除去氢并恢复延展性。8
铀在氢气中加热到250℃到300℃可制得氢化铀,该反应非常迅速,进一步加热到500℃可以除去氢。该性质使得从氢化铀出发可以很方便制得碳化铀,氮化铀,卤化铀。2
用金属铀切片与氢气反应制备UH3。除去金属铀表面的氧化物,迅速将盛有试样的石英舟放入反应管中部(氢化物表观密度为3.4g/cm,若在反复合成及分解中呈粉末状时密度降为1.4g/cm以下,所以所用试样铀量应取决于石英舟的容量)。将系统抽真空至1×10-3Pa(1×10-5mmHg)以下,同时用电炉加热至250℃时,关闭与排气系统相连接的旋塞,通入经过净化装置净化的氢气,使其反应。若取100g铀切片试样,则反应约需要30min的时间(关闭系统后,若压力计所指压力无变化时,可认为反应结束,块状铀约需2h)。反应结束后,仍使氢压保持在100kPa,直至冷却到室温。这样制得的三氢化铀为β型。9
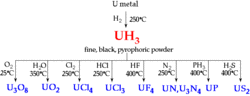
铀与沸水或蒸汽反应也生成氢化铀。
7U+6H2O=3UO2+4UH3
应用氢化铀可用于氢同位素分离,制备铀金属粉末,作为还原剂.
氢化铀在室温有低的离解压(约10−3 Pa),用于氚的贮存就能可靠地保持住氚,而温度升高到400 ℃ 以上,氢化物又很容易离解释放出所吸收的氢10。所以,长期以来,氚化铀被用作氚处理、贮存的最常用、最主要的固体贮氚材料。但是,氢化铀在实际应用中也存在一些问题,特别是它在氢化过程中容易破碎成细粉11,这种粉末降低了氢化铀的热导性,使温度难以控制12。同时,铀吸氢后体胀量很大,这必然增大了铀床床体的设计体积或减少了铀床的装料量。可以通过掺杂锆等金属改善吸氢性能。
同时,氘化铀可以作为中子引发剂 和中子减速剂。
富集到5%的铀235的氢化铀可以作为混合核燃料和中子减速剂的主动自调节核反应堆模块。在专利中,可以通过铀氢化使得氢气渗透到整体铀金属粒中,由于氢化铀的中子减速作用使得中子减速到允许发生核裂变。铀235同时作为核燃料。当反应开始之后,反应将持续进行升温直到大约800摄氏度,氢化铀分解,由于氢化铀的减少,中子减速也将减少,因此核反应将趋于停止;当温度回复到较低水平时,氢气将再次与金属铀化合,缓慢地重新启动核反应。13
历史氢化铀用于一系列实验来确定铀的临界质量。
1943年早期阶段的曼哈顿计划时,氢化铀和氘化铀曾被认为是一个有前途的原子弹材料;然而,它被1944年的春天抛弃了,因为结果证明这样的设计将是低效的。
1953年美国于内华达试验场进行的一系列核试验中成功引爆了氢化铀原子弹。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国