基本介绍
吸收带是指吸收峰在紫外光谱中的波带位置,化合物的结构密切相关。根据大量实验数据的归纳及电子跃迁和分子轨道的种类,通常将紫外-可见光区的吸收带分为四类:R吸收带、K 吸收带、B吸收带和E吸收带。1
分类R吸收带R吸收带是由羰基、硝基等单一生色基团中孤对电子跃迁而产生的吸收带,其强度较弱,吸收峰在200~400nm之间。含C=O、一N=O、—NO2、—N=N—基的有机物可产生这类谱带。它是跃迁形成的吸收带,由于e很小,吸收谱带较弱,易被强吸收谱带掩盖,并易受溶剂极性的影响而发生偏移。
K吸收带K吸收带多由含有共轭双键(如丁二烯、丙烯醛)等化合物产生的一类谱带,其强度较大,吸收峰通常在217~280nm之间。共轭烯烃、取代芳香化合物可产生这类谱带。它是π→π*跃迁形成的吸收带,εmax>10000,吸收谱带较强。
B吸收带B吸收带是芳香族化合物的特征吸收带,出现振动的精细结构的吸收。B带的精细结构常用来识别芳香族化合物。但在极性溶剂中测定或苯环上有取代基且与苯环形成共轭时,则精细结构消失。吸收峰通常在230~270nm之间,占≈100,B吸收带的精细结构常用来判断芳香族化合物。但当苯环上有取代基且与苯环共轭或在极性溶剂中测定时,这些精细结构会简单化或消失。
E吸收带也是芳香族化合物的特征吸收带,有两个吸收峰,分别位于E1带及E2带。E2带的吸收约在180nm(ε大于10000);E2带约在200nm(ε=7000),都属强吸收。E1带是观察不到的。当苯环上有发色团取代而且与苯环共轭时,E2带常和K带合并,吸收峰向长波移动。
综上所述,在有机物和高分子的紫外吸收光谱中,R、K、B、E吸收带的分类不仅反映 出各基团的跃迁方式,而且还揭示了分子结构中各基团间的相互作用。2
影响因素吸收带的位置并不是固定不变的,而是易受分子中结构因素和测定条件等多种因素的影响,在较宽的波长范围内变动。其中分子结构的影响因素包括位阻效应和跨环效应,其核心是对分子中电子共轭结构的影响;测定条件的影响因素包括溶剂的极性和体系的pH。
位阻效应化合物中若有两个发色团产生共轭效应,可使吸收带长移。但若两个发色团由于立体阻碍妨碍它们处于同一平面上,就会影响共轭效应,这种影响在光谱图上可以清晰地显示出来。如:
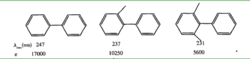
各种异构现象(顺反异构及几何异构)也可使紫外吸收带产生明显差异,其原因除了如
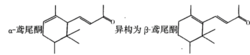
是由于延长了共轭体系的缘故,另一方面也是位阻效应的影响。如二苯乙烯,反式结构的K带比顺式明显长移,且吸收系数也有所增加。其原因就是因为顺式结构有立体阻碍,苯环不能与乙烯双键在同一平面上,不易产生共轭。
跨环效应跨环效应是指非共轭基团之间的相互作用。在环状体系中,分子中非共轭的两个发色团因为空间位置的原因,发生轨道间的相互作用,使得吸收带长移,同时吸光强度增强,这种作用即为跨环效应。但该效应产生的光谱,并不等同于两个发色团的共扼光谱。
如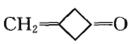 虽然双键与酮基不产生共轭体系,但由于环内的立体排列,使羰基氧的孤电子对和双键的π电子发生作用产生部分π→π*共轭,以致使其由n→π*跃迁产生的R带向长波移动,出现在284nm,同时在214nm处显示出一中等强度的吸收带。此外,当C=O的π轨道与一个杂原子的p轨道能够产生有效交盖时,也出现跨环效应。如:
虽然双键与酮基不产生共轭体系,但由于环内的立体排列,使羰基氧的孤电子对和双键的π电子发生作用产生部分π→π*共轭,以致使其由n→π*跃迁产生的R带向长波移动,出现在284nm,同时在214nm处显示出一中等强度的吸收带。此外,当C=O的π轨道与一个杂原子的p轨道能够产生有效交盖时,也出现跨环效应。如: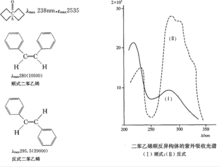
溶剂效应溶剂除影响吸收峰位置外,还影响吸收强度和光谱形状。化合物在溶液中的紫外吸收光谱受溶剂影响较大,所以一般应注明所用溶剂。溶剂的极性不同,会使n— π和π→π跃迁所产生的吸收峰位置向不同方向移动,溶剂极性增大,一般会使,跃 迁吸收峰向长波方向移动;而使n—π跃迁吸收峰向短波方向移动,后者的移动一般比前者移动大。例如异丙叉丙酮的溶剂效应。
极性较大的溶剂,使π→π*跃迁吸收峰长移,是因为激发态的极性总比基态极性大,因而激发态与极性溶剂之间相互作用所降低的能量比基态与极性溶剂之间相互作用所降低的能量大,因而跃迁能级差变小,所以产生长移。而在n→π*跃迁中,基态的极性大,非键电子(n电子)与极性溶剂之间能形成较强的氢键,使基态能量降低大于激发态与极性溶剂相互作用所降低的能量,因而跃迁能级差变大,故产生短移。
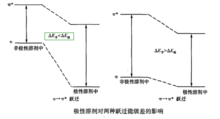
体系pH的影响体系的pH对紫外吸收光谱的影响是比较普遍的,无论是对酸性或碱性样品都有明显的影响。酚类和胺类化合物由于体系的pH不同,其解离情况不同,而产生不同的吸收光谱。3




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国