化学性质
亚砷酸化学式为H3AsO3,也可以写作As(OH)3的氢氧化物形式或As2O3·nH2O的水合物形式。
酸性很微弱的酸性,Ka1=1.03*10-9。
碱性碱性极微弱,在强酸性溶液(如10mol的硫酸溶液)中能够转化为[As(H2O)6]3+离子,和盐酸作用生成AsCl3。
电离1、酸式电离:H3AsO3为路易斯酸。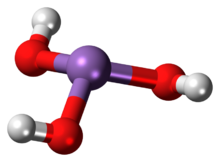 电离方程式为:
电离方程式为:
H3AsO3 + H2O =[As(OH)4]- + H+
[As(OH)4]- + H2O =[As(OH)5]2- + H+
[As(OH)5]2- =[AsO(OH)4]3- + H+
和硼酸一样,亚砷酸的电离是通过和水中的氢氧根结合实现的(最后一步除外)但是因为能结合3个氢氧根,所以亚砷酸为三元弱酸。1
2、碱性电离:
As(OH)3 + 3H+ + 3H2O =[As(H2O)6]3+
用途用于提炼元素砷,是冶炼砷合金和制造半导体的原料。玻璃工业用作澄清剂和脱色剂,以增强玻璃制品透光性。皮革工业用以制亚砷酸钠作皮革保藏剂。农业上用作防治病虫害的消毒剂和除锈剂,也用作其他含砷杀虫农药的原料。也用于涂料和染料的制造,可作化学试剂。还用于气体脱硫、木材防腐、锅炉防垢以及陶瓷和搪瓷等方面。2
毒性致癌。致死量(经口人)为60mg。慢性中毒能造成胃肠功能紊乱,导致周期性结肠炎、慢性肝炎,重者可肝硬变。对黏膜、皮肤、神经系统、肾和心脏有损害。粉尘中毒时,首先看到黏膜、眼和皮肤的改变。急性经口中毒时,采用催吐、洗胃,静脉注射葡萄糖溶液措施。对皮肤疾患可用抗坏血酸和静脉注射硫代硫酸钠等。容许浓度为0.3mg/m3。操作时要戴防毒口罩,佩戴防护眼镜,穿防尘工作服和贴身内衣,戴橡皮、塑料或结实布做的手套,严格遵守个人卫生措施。2




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国