蓖麻毒素为具有两条肽链的高毒性的植物蛋白。它主要存在于蓖麻籽中。该毒素易损伤肝、肾等实质器官,发生出血、变性、坏死病变。并能凝集和溶解红细胞,抑制麻痹心血管和呼吸中枢,是致死的主要原因之一。
小鼠静脉注射LD50值为2.7μg/kg,腹腔注射为7~10μg/kg;对狗LD50值为0.6μg/kg;人致死量约为7mg。
蓖麻毒素除染毒水源和食物经消化道中毒外,还可作为国际间谍情报人员和恐怖分子进行暗害和破坏活动的毒素战剂武器。1978年在伦敦的国际间谍人员曾用装有蓖麻毒素的伞尖在公开场所行刺,一名被刺人员中毒身亡。同时在法国巴黎也有类似事件和发生。1
结构特点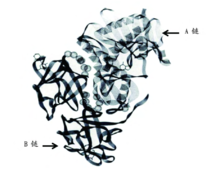 蓖麻毒素(约占蓖麻蛋白的 5%,分子量约为 66 kD)是一种Ⅱ型异二聚体核糖体失活蛋白,由核糖体失活酶(蓖麻毒素 A 链)及与半乳糖/N-乙酰半乳糖胺特异结合的凝集素(蓖麻毒素 B 链)组成,二者之间连接一个二硫键。对蓖麻毒素的一级结构进行分析发现,A 链含有 267 个氨基酸残基,分子量约为 32 kD,具有催化活性,是蓖麻毒素蛋白的效应链。A 链中 N 端第 4 位及 C 端附近分别含有 1 个赖氨酸(Lys)残基,是蓖麻毒素 A 链毒性作用的关键中心。B链具有 2 个结构域,这 2 个结构域具有同源性,由基因复制产生。结构域 1 中含有氨基末端,而结构域 2 中含有羧基末端。蓖麻毒素 B 链由 267 个氨基酸残基组成,具有结合活性,是蓖麻毒素的结合链。2
蓖麻毒素(约占蓖麻蛋白的 5%,分子量约为 66 kD)是一种Ⅱ型异二聚体核糖体失活蛋白,由核糖体失活酶(蓖麻毒素 A 链)及与半乳糖/N-乙酰半乳糖胺特异结合的凝集素(蓖麻毒素 B 链)组成,二者之间连接一个二硫键。对蓖麻毒素的一级结构进行分析发现,A 链含有 267 个氨基酸残基,分子量约为 32 kD,具有催化活性,是蓖麻毒素蛋白的效应链。A 链中 N 端第 4 位及 C 端附近分别含有 1 个赖氨酸(Lys)残基,是蓖麻毒素 A 链毒性作用的关键中心。B链具有 2 个结构域,这 2 个结构域具有同源性,由基因复制产生。结构域 1 中含有氨基末端,而结构域 2 中含有羧基末端。蓖麻毒素 B 链由 267 个氨基酸残基组成,具有结合活性,是蓖麻毒素的结合链。2
理化性质 蓖麻毒素的一、二级结构已清楚,由A、B两条链组成。A链比B链稍短,两链之间以一个二硫键相连接。它含有共价键结合的糖分子,糖的主要组成是甘露糖、葡萄糖和半乳糖。分子量为66,000。在0.1克分子半乳糖溶液中,毒素可在冰箱中贮存数月而不失活性,但煮沸易失去活性。
蓖麻毒素的一、二级结构已清楚,由A、B两条链组成。A链比B链稍短,两链之间以一个二硫键相连接。它含有共价键结合的糖分子,糖的主要组成是甘露糖、葡萄糖和半乳糖。分子量为66,000。在0.1克分子半乳糖溶液中,毒素可在冰箱中贮存数月而不失活性,但煮沸易失去活性。
蓖麻毒素是从蓖麻籽中提取的植物糖蛋白,分子量64000。毒素由A和B两条多肽链组成,两链间由一个二硫键连接。目前,A链和B链的氨基酸序列以及二级结构已基本清楚。毒素B链上含有两个半乳糖或半乳糖残基结合位点,可和细胞表面的含半乳糖残基的受体结合,通过内陷作用进入细胞质,发挥毒性作用。蓖麻毒素A、B链上还分别含有1和2个糖支链,链末端均为甘露糖残基,可以和网状内皮细胞特别是巨噬细胞结合。后者细胞表面富含甘露糖受体,可优先摄取蓖麻毒素,这对于毒素发挥生物功能有重要的作用。1
毒理蓖麻毒素是一种细胞毒。当毒素进入体内,A、B链分开。A链通过渗透经细胞膜进入细胞浆,主要使真核细胞的核糖体抑制失活,从而抑制蛋白质的合成。B链与细胞表面结合,通过内陷作用转入细胞内,它能促使A链进入胞浆。
蓖麻毒素对小鼠艾氏腹水瘤细胞、LD12白血病、B16黑痣瘤和列文斯肺癌细胞均有明显的抑制作用,主要通过抑制蛋白质合成来杀伤癌细胞。另外发现它与其他药物有增效作用如蓖麻毒素与亚德里亚霉素(adriamycin)伍用对杀伤白血病细胞有显著的增效作用。3
临床表现小鼠静脉注射LD50值为2.7μg/kg,腹腔注射为7~10μg/kg;对狗LD50值为0.6μg/kg;人致死量约为7mg。中毒后数小时出现症状。早期有精神不振,恶心呕吐,腹痛、腹泻、便血;继则出现脱水、血压下降,休克嗜睡;严重者可出现抽搐、昏迷,牙关紧闭;最后因循环衰竭而死亡。少数病人可出现发烧、黄疸、便血、蛋白尿、无尿或血尿,终因酸中毒、尿毒症而死亡。该毒素易损伤肝、肾等实质器官,发生出血、变性、坏死病变。并能凝集和溶解红细胞,抑制麻痹心血管和呼吸中枢,是致死的主要原因之一。
毒性作用机理抑制蛋白质合成蓖麻毒素具有强烈的细胞毒性,属于蛋白合成抑制剂或核糖体失活剂,这也是在构建免疫毒素时,应用到蓖麻毒素的主要原因。
合成的机理在20世纪70年代已经明确。首先,毒素依靠B链上的半乳糖结合位点与细胞表面含末端半乳糖残基的受体结合,促进整个毒素分子以内陷方式进入细胞,形成细胞内囊,毒素从细胞内囊中进入细胞质,随后蛋白链间二硫键被还原裂解,游离出A链。A链是一种蛋白酶,作用于真核细胞核糖体60S大亚单位的28S rRNA,水解A4324位点的腺嘌呤N-糖甙甙键,使其脱去腺嘌呤,丧失抗RNA酶的抗性而被降解,不能与延长因子(EF-2)结合,从而干扰了核糖体,EF-2,鸟嘌呤三磷酸腺苷(GTP)复合体的形成,导致蛋白质合成的抑制,最终细胞死亡。已引起研究者注意的是:① B链对A链发挥毒性具有重要的促进作用。② 在细胞内链间二硫键的还原裂解对毒素发挥毒性作用具有重要作用。③ 最新的研究表明:B链上的半乳糖结合位点也参与了毒素的体内毒性。3
诱导细胞因子损伤蓖麻毒素诱导细胞因子的机理目前多数认为是通过刺激淋巴样细胞产生的。主要为巨噬细胞和肝Kupffer′s细胞。这些细胞表面含有甘露糖受体,可与蓖麻毒素分子中3个末端甘露糖残基特异结合而优先被摄取。蓖麻毒素诱导细胞因子的分泌有剂量和时间依赖性。毒素是否可诱导其他细胞因子的产生以及各细胞因子之间是否具有网络免疫调节的作用,尚待探讨。
1986年,Tracey等发现蓖麻毒素中毒大鼠的肠道损伤类似TNF/Chchectin处理的大鼠肠道。1991年Nadkami和Deshphude认为蓖麻毒素中毒后的许多现象,例如:发热,肝出血性坏死,腹水,胸水的渗出,肠道的出血坏死性炎症等等早期的急性反应都与肿瘤坏死因子(TNF-α),白细胞介素(IL-1),IL-6的分泌有关。1993年,Licastro等检测到蓖麻毒素诱导体外培养的外周血单核细胞分泌TNF-α和IL-1β,同时在蓖麻毒素中毒大鼠的血浆中亦可检测到低水平的TNF-α。1994年Mudlooon等发现,体内注射抗TNF的抗体,将明显降低蓖麻毒素对小鼠的氧化损伤。1997年,董巨莹等亦报道了TNF在蓖麻毒素中毒小鼠肝脏的免疫组织化学定位。细胞因子参与机体损伤的另一个例子是:对于由蓖麻毒素构建的免疫毒素1,2期临床试验中病人出现的副作用:包括发热、肌痛、毛细血管渗漏综合症等可以通过封闭或拮抗这些细胞因子的功能而减轻。
蓖麻毒素的毒性具有明显的剂量依赖性,毒素诱导细胞因子的产生,引起体内脂质过氧化损伤以及诱导靶细胞凋亡等等都是在小剂量范围内具有的,而大剂量的蓖麻毒素仍主要表现为抑制蛋白质合成的毒性。毒素诱导细胞因子的产生及引起体内脂质过氧化损伤的作用,均与其糖链末端甘露糖残基被巨噬细胞特异性摄取,并激活巨噬细胞有关,是毒素损伤的继发作用。蓖麻毒素等蛋白质合成抑制剂诱导凋亡的理论研究对现有的凋亡理论可能会有重要的补充价值。3
脂质过氧化损伤蓖麻毒素与巨噬细胞的相互作用,不仅诱导细胞免疫,而且诱导产生自由基和活性氧,引起脂质过氧化作用。1991年,Muldoon和Stohes发现蓖麻毒素可以诱导小鼠体内的脂质过氧化作用,结果导致尿液中丙二醛、甲醛、丙酮的含量增加。1992年的研究表明,各脏器中脂质过氧化强度(MDA含量),还原型谷胱甘肽的减少以及DNA单链断裂程度在毒素中毒36小时后最为强烈,且肝脏的损伤最为严重。结合以往的研究:谷胱甘肽的使用可以部分对抗致死剂量的毒素效应,具有潜在的化学保护作用,因此,Muldoon等认为蓖麻毒素引起的氧化作用可 以归属到蓖麻毒素的毒性机理中去。
TNF-α抗体,铁离子对蓖麻毒素诱导的脂质过氧化和氧化损伤起重要的调节作用。给小鼠注射抗TNF-α的抗体,可以明显降低尿液丙二醛,甲醛,丙酮的含量。铁离子以及去铁敏(desferrioxamine)的掺入,可分别增加和减少蓖麻毒素诱导的脂质过氧化的水平。蓖麻毒素引起体内氧化损伤的机理还待更深入的探讨。3
诱导细胞凋亡坏死和凋亡是细胞死亡的两种方式。在引起细胞凋亡的三大类因素中,毒素,抗癌药物是其中之一。以往认为化疗药物是通过引起靶细胞发生不可逆代谢障碍而杀死肿瘤细胞,近年来认为是通过改变生理环境而诱发细胞发生PCD(programmed cell death)而达到疗效。
1989年,Leek等报道:在蓖麻毒素中毒的肠道病理研究中利用免疫组织化学和电子显微镜观察到肠道上皮细胞的胞浆中存在凋亡样的变化。1990年,Waring报道;蓖麻毒素可诱导巨噬细胞,未成熟T细胞出现DNA破碎(DNA fragmentation),而后者被认为是与凋亡有关的生化改变之一。1991年,他们报道了蓖麻毒素诱导上皮样细胞发生凋亡样的形态学改变。1996年,Fu等报道了蓖麻毒素可诱导小鼠体内甲状腺,脾脏的细胞出现凋亡现象。
蓖麻毒素等蛋白质合成抑制剂诱导细胞凋亡的机制与它们抑制蛋白合成作用无关,亦不需要Ca2+依赖性核酸内切酶的参与,而是与其升高细胞内的三磷酸肌醇水平有关。另外,有报道:巨噬细胞的粘附可以阻止蓖麻毒素诱导的巨噬细胞凋亡现象的发生。蓖麻毒素的抗吞噬细胞作用可能直接导致DNA断裂和诱导细胞凋亡。资料表明:引起细胞坏死的有害因素在强度很大时可导致细胞坏死,但强度较小时却引起细胞发生凋亡。蓖麻毒素诱导的细胞凋亡也存在明显的剂量依赖性。总之,蓖麻毒素诱导细胞发生凋亡与传统的蓖麻毒素作为蛋白质合成抑制剂并不构成矛盾。3
检测方法蓖麻毒素具有很强的毒性作用,毫克级的剂量即可致人或动物死亡。但截至目前,适用于人的解毒药和特异性抗毒素特效药尚未被研制出来。因此,建立快速有效的检测方法成为国内外学者研究的热点。根据蓖麻毒素的理化性质、生物化学特性及免疫学特性,建立了免疫吸收分析、生物传感器分析及生物质谱分析等方法。4
免疫标记分析法免疫标记方法是将抗原或抗体进行生物学标记,利用蓖麻毒素抗原位点能与抗体发生特异性结合的特点而建立的检测方法,是检测蓖麻毒素最常用的技术手段。常用的免疫抗体标记方法有酶联免疫吸附法、胶体金标记法及放射免疫法。Poli 等利用自制的抗体(以羊为抗体制备动物制得)进行研究,结果表明,ELISA 方法可检测到生物样品中微克级的蓖麻毒素。王宗义等通过进一步研究,建立了夹心 ELISA 方法,检出限可达 2.5 ng/mL。
早期酶联免疫吸附法主要采用多克隆抗体,可能存在一定程度上的交叉反应,影响检测结果的精确性。而单克隆抗体是利用某一抗原表位为抗体,具有特异性较高的特点。因此,以单克隆抗体为基础的蓖麻毒素检测方法,是快速、灵敏、经济、实用的定量检测方法。刘文森利用胶体金技术标记所制备的单克隆抗体,进行检测试剂条的制备。结果表明,随着蓖麻毒素浓度的增加,胶体金试剂条的颜色逐渐减弱,试剂条的检测灵敏度可达 10 μg/mL,满足检测需求。4
放射免疫检测法随着生物标记技术的进一步发展,研究者成功建立了放射免疫检测方法。该方法主要是利用抗原-抗体特异性结合而进行体外超微量蓖麻毒素检测,具有高度灵敏性、精确性的特点。放射免疫方法可检测出样品中100 pg 数量级的蓖麻毒素,适用于对蓖麻毒素中毒者血液中蓖麻毒素含量的检测。但该方法的缺点是操作处理比较繁琐,对设备的要求比酶联免疫法高,且对人员的专业性要求较高及放射元素的处理等条件限制了该方法的广泛应用。4
高效液相色谱法高效液相色谱检测将待测物质溶于流动相中,利用色谱柱固定相将流动相的组成进行分离,对检测器收集到的峰信号转换为待测物质浓度,进而来判定待测物质含量的一种方法,具有速度快、分辨率高、灵敏度高等特点。刘文森采用 PROTEIN KW-802.5 凝胶色谱柱,在柱温 25 ℃、流速 1 mL/min、进样量 10 μL 的条件下进行蓖麻毒素检测条件的建立。结果发现,蓖麻毒素在波长 280 nm条件下具有最大的吸收峰,出峰时间约为 8.96 min,在0/093~5/970 μg 具有良好的线性关系,最低检测限达 23.33 ng。4
生物传感法生物传感器是将生物技术和电子技术联合使用,将待测物与识别元件特异性结合后产生的生物敏感物质的化学信号转变为电信号、光信号等,从而达到分析检测目的。该方法无需特殊标记物,具有选择性好、操作简单、实时在线监测的特点,是医学诊断、食品卫生检验等领域安全快速检测的研究热点。4
生物质谱技术基质辅助激光解吸/电离(MALDI)及电喷雾等技术为分析极性强、难挥发等特点的生物样品提供了可靠条件。肽质量指纹谱(peptide mass fingerpritin,PMF)是利用特异性蛋白酶对不同蛋白质一级结构进行水解处理后得到具有独特特征的肽混合物,称其为指纹谱。该方法是目前进行蛋白质鉴定的常用方法。将待测蛋白质样品经垂直板电泳或二维电泳分离,经酶切、肽段提取后,将所得的肽段混合物进一步分离,通过电喷雾-质谱技术在线测定蛋白质的肽谱,从而实现鉴定。该方法不需要进行肽混合物的分离,具有操作简单、分析快速及灵敏度高的特点。4
本词条内容贡献者为:
成玉林 - 副教授 - 重庆大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国