发现理论
1901年,范霍夫因发现化学动力学定律和渗透压,提出了化学反应热力学动态平衡原理,获第一个诺贝尔化学奖。
1906年能斯特提出了热力学第三定律,认为通过任何有限个步骤都不可能达到绝对零度。这个理论在生产实践中得到广泛应用,因此获1920年诺贝尔化学奖。
1931年翁萨格发表论文“不可逆过程的倒数关系”,阐明了关于不可逆反应过程中电压与热量之间的关系。对热力学理论作出了突破性贡献。这一重要发现放置了20年,后又重新被认识。1968年获诺贝尔化学奖。
1950年代,普利戈金提出了著名的耗散结构理论。1977年,他因此获诺贝尔化学奖。这一理论是当代热力学理论发展上具有重要意义的大事。它的影响涉及化学、物理、生物学等广泛领域,为我们理解生命过程等复杂现象提供了新的启示。1
第一定律实质
能量守恒与转换定律是自然界的基本规律之一。它指出: 自然界中的一切物质都具有能量, 能量不可能被创造, 也不可能被消灭; 但能量可以从一种形态转变为另一种形态, 且在能量的转化过程中能量的总量保持不变。
热力学第一定律是能量守恒与转换定律在热现象中的应用, 它确定了热力过程中热力系与外界进行能量交换时, 各种形态能量数量上的守恒关系。
我们知道, 运动是物质的属性, 能量是物质运动的度量。分子运动学说阐明了热能是组成物质的分子、原子等微粒的杂乱运动———热运动的能量。既然热能和其他形态的能量都是物质的运动, 那么热能和其他形态的能量可以相互转换, 并在转化时能量守恒完全是理所当然的。
在工程热力学的范围内, 主要考虑的是热能和机械能之间的相互转换与守恒, 所以第一定律可表述为:“热是能的一种, 机械能变热能, 或热能变机械能的时候, 它们间的比值是一定的。” 或“ 热可以变为功, 功也可变为热。一定量的热消失时必产生相应量的功;消耗一定量的功时必出现与之对应的一定量的热。”
热力学第一定律是人类在实践中累积的经验总结, 它不能用数学或其他的理论来证明, 但第一类永动机迄今仍未造成以及由第一定律所得出的一切推论都与实际经验相符合等事实, 可以充分说明它的正确性。2
基本内容
能量是永恒的,他不会被谁制造出来,也不会被谁消灭。但是热能可以给动能提供动力,而动能还能够再转化成热能。
普遍的能量转化和守恒定律在一切涉及热现象的宏观过程中的具体表现。热力学的基本定律之一。
表征热力学系统能量的是内能。通过作功和传热,系统与外界交换能量,使内能有所变化。根据普遍的能量守恒定律,系统由初态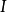 经过任意过程到达终态
经过任意过程到达终态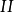 后,内能的增量
后,内能的增量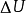 应等于在此过程中外界对系统传递的热量
应等于在此过程中外界对系统传递的热量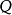 和系统对外界作功
和系统对外界作功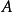 之差,即
之差,即
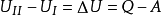
或

式中:
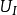 ——系统初态
——系统初态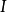 时的能量;
时的能量;
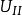 ——系统终态
——系统终态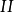 时的能量;
时的能量;
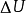 ——系统内能增量;
——系统内能增量;
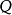 ——外界对系统传递的热量;
——外界对系统传递的热量;
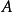 ——系统对外界做功差。
——系统对外界做功差。
这就是热力学第一定律的表达式。如果除作功、传热外,还有因物质从外界进入系统而带入的能量 ,则应为
,则应为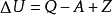 当然,上述
当然,上述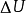 、
、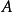 、
、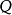 、
、 均可正可负。
均可正可负。
微积分表达式
热力学第一定律的能量方程式就是系统变化过程中的能量平衡方程式, 是分析状态变化过程的根本方程式。它可以从系统在状态变化过程中各项能量的变化和它们的总量守恒这一原则推出。把热力学第一定律的原则应用于系统中的能量变化时可写成如下形式:
进入系统的能量- 离开系统的能量= 系统中储存能量的增加
上式是系统能量平衡的基本表达式, 任何系统、任何过程均可据此原则建立其平衡式。对于闭口系统, 进入和离开系统的能量只包括热量和作功两项;对于开口系统, 因有物质进出分界面, 所以进入系统的能量和离开系统的能量除以上两项外, 还有随同物质带进、带出系统的能量。
由于这些区别, 热力学第一定律应用于不同热力系统时, 可得不同的能量方程。
对于一个微元过程, 第一定律解析式的微积分形式是:
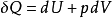 ,
,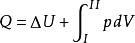
热力学第一定律的另一种表述是:第一类永动机是不可能造成的。这是许多人幻想制造的能不断地作功而无需任何燃料和动力的机器,是能够无中生有、源源不断提供能量的机器。显然,第一类永动机违背了能量守恒定律。
第二定律表述
热力学第二定律是阐明与热现象相关的各种过程进行的方向、条件及限度的定律。由于工程实践中热现象普遍存在, 热力学第二定律应用范围极为广泛,诸如热量传递、热功互变、化学反应、燃料燃烧、气体扩散、混合、分离、溶解、结晶、辐射、生物化学、生命现象、信息理论、低温物理、气象以及其他许多领域。
热力学第二定律的克劳修斯说法:
1850 年, 克劳修斯(Dudolf Clausius)从热量传递方向性的角度提出: 热不可能自发地、不付代价地从低温物体传至高温物体。
这里指的是“自发地、不付代价地”。通过热泵装置的逆向循环可以将热量自低温物体传向高温物体, 并不违反热力学第二定律, 因为它是花了代价而非自发进行的。非自发过程(热量自低温传向高温) 的进行, 必须同时伴随一个自发过程(机械能转变为热能) 作为代价、补充条件, 后者称为补偿过程。
热力学第二定律的开尔文说法:
1824 年, 卡诺(Sadi Carnot )最早提出了热能转化为机械能的根本条件:“ 凡有温度差的地方都能产生动力。”实质上, 它是热力学第二定律的一种表达方式。随着蒸汽机的出现, 人们在提高热机效率的研究中认识到, 只有一个热源的热动力装置是无法工作的, 要使热能连续地转化为机械能至少需要两个( 或多于两个)温度不同的热源, 通常以大气中的空气或环境温度下的水作为低温热源, 另外还需有高于环境温度的高温热源, 例如高温烟气。1851 年左右, 开尔文( LordKelvin)和普朗克(Max Planck) 等人从热能转化为机械能的角度先后提出更为严密的表述, 被称为热力学第二定律的开尔文说法: 不可能制造出从单一热源吸热、使之全部转化为功而不留下其他任何变化的热力发动机。2
方向性
1、 功热转化
功可以自动地转化为热,功转热是不可逆过程, 其反向过程, 即降低流体的热力学能或收集散给环境的热量转化为功重新举起重物回复原位的过程, 则不能单独地、自动地进行, 热不可能全部无条件地转化为功。
2、热永远只能由热处传到冷处(在自然状态下)。3
热量一定自动地从高温物体传向低温物体; 而反向过程, 热量由低温传回高温、系统回复到原状的过程,则不能自动进行, 需要依靠外界的帮助。
熵及熵增原理
熵是与热力学第二定律紧密相关的状态参数。它是判别实际过程的方向,提供过程能否实现、是否可逆的判据, 在过程不可逆程度的量度、热力学第二定律的量化等方面有至关重要的作用。
克劳修斯首次从宏观角度提出熵概念(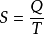 ),而后波尔兹曼又从微观角度提出熵概念(
),而后波尔兹曼又从微观角度提出熵概念(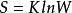 ),其两者是相通的,近代的普里戈金提出了耗散结构理论,将熵理论中引进了熵流的概念,阐述了系统内如果流出的熵流(
),其两者是相通的,近代的普里戈金提出了耗散结构理论,将熵理论中引进了熵流的概念,阐述了系统内如果流出的熵流(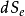 )大于熵产生(
)大于熵产生(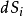 )时,可以导致系统内熵减少,即
)时,可以导致系统内熵减少,即
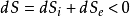
这种情形应称为相对熵减。但是,若把系统内外一并考察仍然服从熵增原理。
熵增原理最经典的表述是:“绝热系统的熵永不减少”,近代人们又把这个表述推广为“在孤立系统内,任何变化不可能导致熵的减少”。熵增原理如同能量守恒定律一样,要求每时每刻都成立。关于系统有四种说法,分别叫孤立、封闭、开放和绝热系统,孤立系统是指那些与外界环境既没有物质也没有能量交换的系统,或者是系统内部以及与之有联系的外部两者总和,封闭系统是指那些与外界环境有能量交换,但没有物质交换的系统,开放系统是指与外界既有能量又有物质交换的系统,而绝热系统是指既没有粒子交换也没有热能交换,但有非热能如电能、机械能等的交换。
第三定律表述
1912 年, 能斯特根据他所提出的热定理推论, 得出:绝对零度不可能达到。叙述成定律的形式为:“ 不可能应用有限个方法使物系的温度达到绝对零度。”
上述定律是热力学第三定律的表述方式之一。绝对零度不可能达到, 看来是自然界中的一个客观规律。这个规律的本质意义为, 物体分子和原子中和热能有关的各种运动形态不可能全部被停止。这与量子力学的观点相符合, 也符合辩证唯物主义的观点:“ 运动是物质的不可分割的属性”。任何一种运动形态看来都不可能完全消失。
根据能斯特热定理推出绝对零度不可能达到的推理如下:据能斯特热定理,物系在接近绝对零度下进行定温过程时, 物系的熵不变。物系的熵不变的过程本为孤立系统的可逆绝热过程。所以, 在接近绝对零度时绝热过程也具有了定温的特性, 这时就不可能再依靠绝热过程来进一步降低物系的温度以达到绝对零度。
所以, 热力学第三定律的上述两种叙述方式是等效的, 其中任何一种都可以从另一种推出。
第二定律告诉我们,得有温度更低的东西才能使热量转移,所以,在绝对零度,你不能让任何东西变得更冷。
“在绝对零度下任何纯粹物质完整晶体的熵等于零”。即
 式中
式中
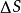 ——熵变化值;
——熵变化值;
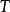 ——定温过程。2
——定温过程。2
第零定律表述
如果两个热力学系统中的每一个都与第三个热力学系统处于热平衡(温度相同),则它们彼此也必定处于热平衡。这一结论称做“热力学第零定律”。
热力学第零定律的重要性在于它给出了温度的定义和温度的测量方法。
定律中所说的热力学系统是指由大量分子、原子组成的物体或物体系。它为建立温度概念提供了实验基础。这个定律反映出:处在同一热平衡状态的所有的热力学系统都具有一个共同的宏观特征,这一特征是由这些互为热平衡系统的状态所决定的一个数值相等的状态函数,这个状态函数被定义为温度。而温度相等是热平衡之必要的条件。
适用范围
第零定律是在不考虑引力场作用的情况下得出的,物质(特别是气体物质)在引力场中会自发产生一定的温度梯度。如果有封闭两个容器分别装有氢气和氧气,由于它们的分子量不同,它们在引力场中的温度梯度也不相同。如果最低处它们之间可交换热量,温度达到相同,但由于两种气体温度梯度不同,则在高处温度就不相同,也即不平衡。因此第零定律不适用引力场存在的情形。这与限定第二类永动机不成立的第二定律类似。
意义
热力学第零定律用来作为进行体系测量的基本依据,其重要性在于它说明了温度的定义和温度的测量方法。表述如下:
1、可以通过使两个体系相接触,并观察这两个体系的性质是否发生变化而判断这两个体系是否已经达到热平衡。
2、当外界条件不发生变化时,已经达成热平衡状态的体系,其内部的温度是均匀分布的,并具有确定不变的温度值。
3、一切互为平衡的体系具有相同的温度,所以一个体系的温度可以通过另一个与之平衡的体系的温度来表示,也可以通过第三个体系的温度来表示。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国