近视是我国的“国病”,是我国视觉障碍的首要原因。目前对近视的病因和发病机制还知之甚少,因此近视的治疗手段还很有限。近视形成中一个关键的病理改变是巩膜成纤维细胞—肌成纤维细胞转分化(以下简称:成纤维细胞转分化)增多、胶原减少引起的巩膜组织重构,但其诱导因素一直未被解析。该团队前期系列研究发现,缺氧是近视形成中巩膜病理改变的关键触发因素之一。因此,缺氧如何诱导巩膜重构导致近视形成是领域内的关键科学问题。

研究团队首先利用小鼠和豚鼠两种近视模型,发现近视诱导中巩膜糖酵解限速酶表达水平和乳酸水平显著高于对照组。增强巩膜糖酵解或增加乳酸水平均可诱导巩膜成纤维细胞转分化增多、胶原减少、组织重构和近视形成;相反,药理学干预或基因敲降等方法抑制巩膜糖酵解或减少乳酸,可消除或抑制巩膜重构和近视形成。此外,分析UK Biobank中近视GWAS 数据发现编码糖酵解通路关键酶 ENO2 和 TPI1 的基因显著富集,提示糖酵解信号通路异常也可能与人类近视形成相关。 那么巩膜中增多的乳酸如何发挥生物学效应呢?利用动物模型和细胞实验发现:巩膜乳酸堆积增多可增加组蛋白乳酸化修饰;其中组蛋白H3的18位赖氨酸残基的乳酸化修饰(H3K18la)可通过上调Notch1基因的表达,促进巩膜成纤维细胞转分化、组织重构,导致近视形成。 随后,利用巩膜特异性敲降HIF-1α小鼠模型,证明缺氧是近视形成中巩膜糖酵解增强、乳酸增多的诱导因素。除了缺氧是否有其他上游信号通路可以激活巩膜糖酵解,诱导近视?研究发现,近视诱导中巩膜胰岛素信号通路显著激活。而我们都知道,高糖饮食能促进胰岛素分泌,作者进一步实验证明了高糖饮食不仅可以诱导豚鼠形成近视,还可以加剧形觉剥夺诱导的近视形成。在机制上也证明了高糖饮食可以激活巩膜胰岛素信号通路并激活“糖酵解—乳酸—乳酸化—Notch1”信号轴,诱导巩膜成纤维细胞转分化增多、胶原减少,导致近视。据统计,过去50年全球糖消耗量增加了3倍,该研究结果也可能部分解释了近30年全球近视发病率急剧增长的原因,这也提示:在近视形成的青少年时期减少糖摄入可以作为近视防控的策略之一。
综上所述,这项研究不仅为近视巩膜重构的内在机制提供了新见解,而且本研究发现近距离诱导的巩膜缺氧与高糖饮食引起的胰岛素增加均可激活巩膜糖酵解诱导近视。据此提出对近视的临床防控手段之一,餐后1小时内避免或减少近距离工作,可以避免餐后胰岛素升高和近距离工作导致的巩膜缺氧两诱导近视的叠加效应起到防控近视的效果。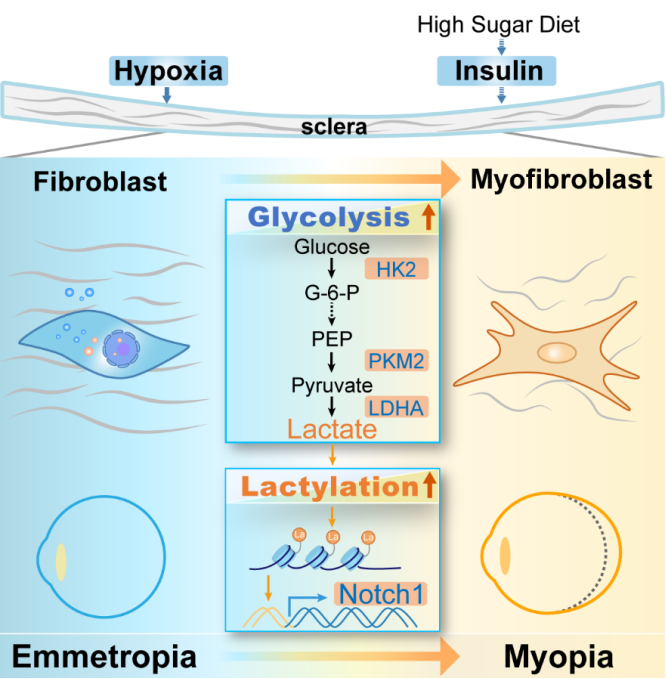




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国