基本含义
 蛋白质是由氨基酸以“脱水缩合”的方式组成的多肽链经过盘曲折叠形成的具有一定空间结构的物质。
蛋白质是由氨基酸以“脱水缩合”的方式组成的多肽链经过盘曲折叠形成的具有一定空间结构的物质。
蛋白质中一定含有碳、氢、氧、氮元素,也可能含有硫、磷等元素。
蛋白质是由α-氨基酸按一定顺序结合形成一条多肽链,再由一条或一条以上的多肽链按照其特定方式结合而成的高分子化合物。蛋白质就是构成人体组织器官的支架和主要物质,在人体生命活动中,起着重要作用,可以说没有蛋白质就没有生命活动的存在。
男性缺失蛋白质比女性缺失蛋白质更需要重视,男士一旦缺失蛋白质,会导致男性精子质量下降,精子活力降低以及精子不液化造成男性不育。
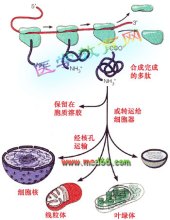
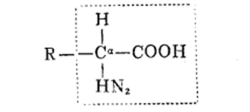 蛋白质是一种复杂的有机化合物,旧称“朊**(ruǎn)**”。氨基酸是组成蛋白质的基本单位,氨基酸通过脱水缩合连成肽链。蛋白质是由一条或多条多肽链组成的生物大分子,每一条多肽链有二十至数百个氨基酸残基(-R)不等;各种氨基酸残基按一定的顺序排列。蛋白质的氨基酸序列是由对应基因所编码。除了遗传密码所编码的20种基本氨基酸,在蛋白质中,某些氨基酸残基还可以被翻译后修饰而发生化学结构的变化,从而对蛋白质进行激活或调控。多个蛋白质可以一起,往往是通过结合在一起形成稳定的蛋白质复合物,折叠或螺旋构成一定的空间结构,从而发挥某一特定功能。合成多肽的细胞器是细胞质中糙面型内质网上的核糖体。蛋白质的不同在于其氨基酸的种类、数目、排列顺序和肽链空间结构的不同。
蛋白质是一种复杂的有机化合物,旧称“朊**(ruǎn)**”。氨基酸是组成蛋白质的基本单位,氨基酸通过脱水缩合连成肽链。蛋白质是由一条或多条多肽链组成的生物大分子,每一条多肽链有二十至数百个氨基酸残基(-R)不等;各种氨基酸残基按一定的顺序排列。蛋白质的氨基酸序列是由对应基因所编码。除了遗传密码所编码的20种基本氨基酸,在蛋白质中,某些氨基酸残基还可以被翻译后修饰而发生化学结构的变化,从而对蛋白质进行激活或调控。多个蛋白质可以一起,往往是通过结合在一起形成稳定的蛋白质复合物,折叠或螺旋构成一定的空间结构,从而发挥某一特定功能。合成多肽的细胞器是细胞质中糙面型内质网上的核糖体。蛋白质的不同在于其氨基酸的种类、数目、排列顺序和肽链空间结构的不同。
食入的蛋白质在体内经过消化被水解成氨基酸被吸收后,合成人体所需蛋白质,同时新的蛋白质又在不断代谢与分解,时刻处于动态平衡中。因此,食物蛋白质的质和量、各种氨基酸的比例,关系到人体蛋白质合成的量,尤其是青少年的生长发育、孕产妇的优生优育、老年人的健康长寿,都与膳食中蛋白质的量有着密切的关系。蛋白质又分为完全蛋白质和不完全蛋白质。缺乏必需氨基酸或者含量很少的蛋白质称不完全蛋白质,如谷、麦类、玉米所含的蛋白质和动物皮骨中的明胶等。
相关计算
原子数
由m个氨基酸,n条肽链组成的蛋白质分子,至少含有n个—COOH,至少含有n个—NH2,肽键m-n个,O原子m+n个。
分子质量
设氨基酸的平均相对分子质量为a,含b个二硫键*,蛋白质的相对分子质量=ma-18(m-n)-2b*
基因控制
基因中的核苷酸 6
信使RNA中的核苷酸 3
蛋白质中氨基酸 1
组成及特点
蛋白质是由C(碳)、H(氢)、O(氧)、N(氮)组成,一般蛋白质可能还会含有P(磷)、S(硫)、Fe(铁)、Zn(锌)、Cu(铜)、B(硼)、Mn(锰)、I(碘)、Mo(钼)等。
这些元素在蛋白质中的组成百分比约为:碳50%、氢7%、氧23%、氮16%、硫0~3%、其他微量。
(1)一切蛋白质都含氮元素,且各种蛋白质的含氮量很接近,平均为16%;
(2)蛋白质系数:任何生物样品中每1g元氮的存在,就表示大约有100/16=6.25g蛋白质的存在, 6.25常称为蛋白质常数。
整体结构
蛋白质是以氨基酸为基本单位构成的生物高分子。蛋白质分子上氨基酸的序列和由此形成的立体结构构成了蛋白质结构的多样性。蛋白质具有一级、二级、三级、四级结构,蛋白质分子的结构决定了它的功能。
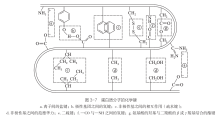
一级结构(primary structure):氨基酸残基在蛋白质肽链中的排列顺序称为蛋白质的一级结构,每种蛋白质都有独立而确切的氨基酸序列。肽键是一级结构中连接氨基酸残基的主要化学键,有些蛋白质还包括二硫键。
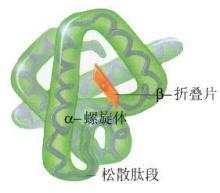
二级结构(secondary structure):蛋白质分子中肽链并非直链状,而是按一定的规律卷曲(如α-螺旋结构)或折叠(如β-折叠结构)形成特定的空间结构,这是蛋白质的二级结构。蛋白质的二级结构主要依靠肽链中氨基酸残基亚氨基(-NH-)上的氢原子和羰基上的氧原子之间形成的氢键而实现的。二级结构的形式有α-螺旋,β-折叠,β-转角,Ω-环。其中α-螺旋是常见的二级结构,且多为右手螺旋。β-折叠是多肽链形成片层结构,呈锯齿状。β-转角和Ω-环则存在于球状蛋白中。
三级结构(tertiary structure):在二级结构的基础上,肽链还按照一定的空间结构进一步形成更复杂的三级结构。肌红蛋白,血红蛋白等正是通过这种结构使其表面的空穴恰好容纳一个血红素分子。维系球状蛋白质三级结构的作用力有盐键、氢键、疏水作用和范德华力,这些作用力统称为次级键。此外,二硫键在稳定某些蛋白质的空间结构上也起着重要作用。
四级结构(quaternary structure):具有三级结构的多肽链按一定空间排列方式结合在一起形成的聚集体结构称为蛋白质的四级结构。如血红蛋白由4个具有三级结构的多肽链构成,其中两个是α-链,另两个是β-链,其四级结构近似椭球形状。
连接方法
用约20种氨基酸作原料,在细胞质中的核糖体上,将氨基酸分子互相连接成肽链。一个氨基酸分子的氨基和另一个氨基酸分子的羧基,脱去一分子水而连接起来,这种结合方式叫做脱水缩合。通过缩合反应,在羧基和氨基之间形成的连接两个氨基酸分子的那个键叫做肽键。由肽键连接形成的化合物称为肽。
检测方法
分别向甲、乙两支试管加入3毫升蛋清稀释液和清水,再依次向两支试管中加入双缩脲试剂A液和B液。观察甲、乙两试管中溶液发生的颜色变化。上述的演示实验结果表明,双缩脲试剂与蛋白质呈现紫色反应。
生理需要
2000年,中国营养学会重新修订了推荐的膳食营养素摄入量,新修订的蛋白质推荐摄入量如下:
|| || 中国居民膳食蛋白质的推荐摄入量
**● RNI(推荐摄入量):**是指可以满足某一特定性别、年龄及生理状况群体中绝大多数个体(97%~98%)的需要量的摄入水平。长期摄入RNI水平,可以满足机体对该营养素的需要,维持组织中适当的营养素储备,保持健康。
代谢吸收
蛋白质在胃液消化酶的作用下,初步水解,在小肠中完成整个消化吸收过程。氨基酸的吸收通过小肠黏膜细胞,是由主动运转系统进行,分别转运中性、酸性和碱性氨基酸。在肠内被消化吸收的蛋白质,不仅来自于食物,也有肠黏膜细胞脱落和消化液的分泌等,每天有70g左右蛋白质进入消化系统,其中大部分被消化和重吸收。未被吸收的蛋白质由粪便排出体外。
病症
过量
表现
肾脏要排泄进食的蛋白质,当分解蛋白质时会产生大量的氮素这样会增加肾脏的负担。蛋白质,尤其是动物性蛋白摄入过多,对人体同样有害。首先过多的动物蛋白质的摄入,就必然摄入较多的动物脂肪和胆固醇。其次蛋白质过多本身也会产生有害影响。正常情况下,所以必须将过多的蛋白质脱氨分解,氮则由尿排出体外,这加重了代谢负担,而且,这一过程需要大量水分,从而加重了肾脏的负荷,若肾功能本来不好,则危害就更大。过多的动物蛋白摄入,也造成含硫氨基酸摄入过多,这样可加速骨骼中钙质的丢失,易产生骨质疏松。
危害
1、一旦蛋白质在体内转化为脂肪,血液的酸性就会提高,这样就会消耗大量的钙质,结果储存在骨骼当中的钙质就被消耗了,使骨质变脆。
2、肾脏要排泄进食的蛋白质,当分解蛋白质时会产生大量的氮素这样会增加肾脏的负担。
缺乏症
蛋白质缺乏在成人和儿童中都有发生,但处于生长阶段的儿童更为敏感。蛋白质的缺乏常见症状是代谢率下降,对疾病抵抗力减退,易患病,远期效果是器官的损害,常见的是儿童的生长发育迟缓、营养不良、体质量下降、淡漠、易激怒、贫血以及干瘦病或水肿,并因为易感染而继发疾病。蛋白质的缺乏,往往又与能量的缺乏共同存在即蛋白质—热能营养不良,分为两种,一种指热能摄入基本满足而蛋白质严重不足的营养性疾病,称加西卡病。另一种即为“消瘦”,指蛋白质和热能摄入均严重不足的营养性疾病。
用处
1、蛋白质是建造和修复身体的重要原料,人体的发育以及受损细胞的修复和更新,都离不开蛋白质。
2、蛋白质也能被分解为人体的生命活动提供能量。
性质
两性
蛋白质是由α-氨基酸通过肽键构成的高分子化合物,在蛋白质分子中存在着氨基和羧基,因此跟氨基酸相似,蛋白质也是两性物质。
水解反应
蛋白质在酸、碱或酶的作用下发生水解反应,经过多肽,最后得到多种α-氨基酸。
蛋白质水解时,应找准结构中键的“断裂点”,水解时肽键部分或全部断裂。
胶体性质
有些蛋白质能够溶解在水里(例如鸡蛋白能溶解在水里)形成溶液。
蛋白质的分子直径达到了胶体微粒的大小(10-9~10-7m)时,所以蛋白质具有胶体的性质。
沉淀
原因:加入高浓度的中性盐、加入有机溶剂、加入重金属、加入生物碱或酸类、少量的盐(如硫酸铵、硫酸钠等)能促进蛋白质的溶解。如果向蛋白质水溶液中加入浓的无机盐溶液,可使蛋白质的溶解度降低,而从溶液中析出,这种作用叫做盐析。
这样盐析出的蛋白质仍旧可以溶解在水中,而不影响原来蛋白质的性质,因此盐析是个可逆过程。利用这个性质,采用分段盐析方法可以分离提纯蛋白质。
变性
在热、酸、碱、重金属盐、紫外线等作用下,蛋白质会发生性质上的改变而凝结起来。这种凝结是不可逆的,不能再使它们恢复成原来的蛋白质。蛋白质的这种变化叫做变性,蛋白质变性之后,紫外吸收,化学活性以及粘度都会上升,变得容易水解,但溶解度会下降。
蛋白质变性后,就失去了原有的可溶性,也就失去了它们生理上的作用。因此蛋白质的变性凝固是个不可逆过程。
造成蛋白质变性的原因
物理因素包括:加热、加压、搅拌、振荡、紫外线照射、X射线、超声波等。
化学因素包括:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等。
颜色反应
蛋白质是由不同氨基酸残基组成的,这些氨基酸残基所含的基团也会发生一些颜色反应。
1.茚三酮反应
将蛋白质溶液与茚三酮稀溶液混合后加热,溶液呈蓝色。所有蛋白质都能与茚三酮发生显色反应。
2.缩二脲反应
将蛋白质溶液与强碱溶液和硫酸铜稀溶液混合后,铜离子与相邻两个肽键上的氮原子和氧原子形成螯合离子而呈现紫红色,此反应称为蛋白质的缩二脲反应。二肽以上的肽和蛋白质都能发生缩二脲反应
3.蛋白黄反应
含有苯丙氨酸、酪氨酸和色氢酸残基的蛋白质与浓硝酸作用后呈现黄色,称为蛋白黄反应。这是因为这些氨基酸残基中的苯环与浓硝酸发生硝化反应,生成了黄色的硝基化合物,皮肤 、指甲遇浓硝酸变黄就是基于这个原因。
4.米勒反应
含有酪氨酸残基的蛋白质遇硝酸汞的硝酸溶液呈现红色,称为米勒反应。这是由于酪氨酸残基中的酚羟基与汞离子形成了红色化合物,由于大多数蛋白质中都含有酪氨酸残基,因此米勒反应具有普遍性。
气味反应
蛋白质在灼烧分解时,可以产生一种烧焦羽毛的特殊气味。利用这一性质可以鉴别蛋白质。
折叠
对蛋白质折叠机理的研究,对保留蛋白质活性,维持蛋白质稳定性和包涵体蛋白质折叠复性都具有重要的意义。早在上世纪30年代,我国生化界先驱吴宪教授就对蛋白质的变性作用进行了阐释,30年后,Anfinsen通过对核糖核酸酶A的经典研究表明,去折叠的蛋白质在体外可以自发的进行再折叠,仅仅是序列本身已经包括了蛋白质正确折叠的所有信息,并提出蛋白质折叠的热力学假说,为此Anfinsen获得1972年诺贝尔化学奖。这一理论有两个关键点:(1)蛋白质的状态处于去折叠和天然构象的平衡中;(2) 天然构象的蛋白质处于热力学最低的能量状态。尽管蛋白质的氨基酸序列在蛋白质的正确折叠中起着核心的作用,各种各样的因素,包括信号序列,辅助因子,分子伴侣,环境条件,均会影响蛋白质的折叠,新生蛋白质折叠并组装成有功能的蛋白质,并非都是自发的,在多数情况下是需要其它蛋白质的帮助,已经鉴定了许多参与蛋白质折叠的折叠酶和分子伴侣,蛋白质“自发折叠”的经典概念发生了转变和更新,但这并不与折叠的热力学假说相矛盾,而是在动力学上完善了热力学观点。在蛋白质的折叠过程中,有许多作用力参与,包括一些构象的空间阻碍,范德华力,氢键的相互作用,疏水效应,离子相互作用,多肽和周围溶剂相互作用产生的熵驱动的折叠,但对于蛋白质获得天然结构这一复杂过程的特异性,我们还知之甚少,许多实验和理论的工作都在加深我们对折叠的认识,但是问题仍然没有解决。
在折叠的机制研究上早期的理论认为,折叠是从变性状态通过中间状态到天然状态的一个逐步的过程,并对折叠中间体进行了深入研究,认为折叠是在热力学驱动下按单一的途径进行的。后来的研究表明折叠过程存在实验可测的多种中间体,折叠通过有限的路径进行。新的理论强调在折叠的初始阶段存在多样性,蛋白质通过许多的途径进入折叠漏斗,从而折叠在整体上被描述成一个漏斗样的图像,折叠的动力学过程被认为是部分折叠的蛋白质整体上的进行性装配,并且伴随有自由能和熵的变化,蛋白质最终寻找到自己的正确的折叠结构,这一理论称为能量图景,漏斗下方的凹凸反映蛋白质构象瞬间进入局部自由能最小区域。
能量图景的示意图,高度代表能量尺度,宽度代表构象尺度,在漏斗(funnel)的下方存在别的低能量状态,共存的不同能量状态的蛋白质种类也降到最小。
这一理论认为结构同源的蛋白质可以通过不同的折叠途径形成相似的天然构象,人酸性成纤维生长因子(hFGF-1)和蝾螈酸性成纤维生长因子(nFGF-1)氨基酸序列具有约80%同源性,并且具有结构同源性(12个β-折叠反向平行排列形成β折叠桶),在盐酸胍诱导去折叠的过程中,hFGF-1可以监测到具有熔球体样的折叠中间体,而nFGF-1经由两态(天然状态到变性状态)去折叠,没有检测到中间体的存在,折叠的动力学研究也表明两种蛋白采用不同的折叠机制。对于同一蛋白质,采用的渗透压调节剂不同,蛋白质折叠的途径也不相同,说明不同的渗透压调节剂对蛋白质的稳定效应不同。这两个例子都说明折叠机制的复杂性,也与上面所介绍的理论相吻合。
生理功能
构造人的身体
 蛋白质是一切生命的物质基础,是机体细胞的重要组成部分,是人体组织更新和修补的主要原料。人体的每个组织:毛发、皮肤、肌肉、骨骼、内脏、大脑、血液、神经、内分泌等都是由蛋白质组成,所以说饮食造就人本身。蛋白质对人的生长发育非常重要。
蛋白质是一切生命的物质基础,是机体细胞的重要组成部分,是人体组织更新和修补的主要原料。人体的每个组织:毛发、皮肤、肌肉、骨骼、内脏、大脑、血液、神经、内分泌等都是由蛋白质组成,所以说饮食造就人本身。蛋白质对人的生长发育非常重要。
比如大脑发育的特点是一次性完成细胞增殖,人的大脑细胞的增长有二个高峰期。第一个是胎儿三个月的时候;第二个是出生后到一岁,特别是0-6个月的婴儿是大脑细胞猛烈增长的时期。到一岁大脑细胞增殖基本完成,其数量已达成人的9/10。所以0到1岁儿童对蛋白质的摄入要求很有特色,对儿童的智力发展尤关重要。
结构物质
人的身体由百兆亿个细胞组成,细胞可以说是生命的最小单位,它们处于永不停息的衰老、死亡、新生的新陈代谢过程中。例如年轻人的表皮28天更新一次,而胃黏膜两三天就要全部更新。所以一个人如果蛋白质的摄入、吸收、利用都很好,那么皮肤就是光泽而又有弹性的。反之,人则经常处于亚健康状态。组织受损后,包括外伤,不能得到及时和高质量的修补,便会加速肌体衰退。
载体的运输
维持肌体正常的新陈代谢和各类物质在体内的输送。载体蛋白对维持人体的正常生命活动是至关重要的。可以在体内运载各种物质。比如血红蛋白——输送氧(红血球更新速率250万/秒)、脂蛋白———输送脂肪、细胞膜上的受体还有转运蛋白等。维持与构成
维持机体内的渗透压的平衡:白蛋白。维持体液的酸碱平衡。构成神经递质乙酰胆碱、五羟色氨等。维持神经系统的正常功能:味觉、视觉和记忆。
抗体的免疫
有白细胞、淋巴细胞、巨噬细胞、抗体(免疫球蛋白)、补体、干扰素等。七天更新一次。当蛋白质充足时,这个部队就很强,在需要时,数小时内可以增加100倍。
酶的催化
构成人体必需的催化和调节功能的各种酶。我们身体有数千种酶,每一种只能参与一种生化反应。人体细胞里每分钟要进行一百多次生化反应。酶有促进食物的消化、吸收、利用的作用。相应的酶充足,反应就会顺利、快捷的进行,我们就会精力充沛,不易生病。否则,反应就变慢或者被阻断。
激素的调节
具有调节体内各器官的生理活性。胰岛素是由51个氨基酸分子合成。生长激素是由191个氨基酸分子合成(与生长素无关)。
胶原蛋白
占身体蛋白质的1/3,生成结缔组织,构成身体骨架。如骨骼、血管、韧带等,决定了皮肤的弹性,保护大脑(在大脑脑细胞中,很大一部分是胶原细胞,并且形成血脑屏障保护大脑)
能源物质
提供生命活动的能量。
发展历程
 **蛋白质是荷兰科学家格利特·马尔德在1838年发现的。**他观察到有生命的东西离开了蛋白质就不能生存。蛋白质是生物体内一种极重要的高分子有机物,占人体干重的54%。蛋白质主要由氨基酸组成,因氨基酸的组合排列不同而组成各种类型的蛋白质。人体中估计有10万种以上的蛋白质。生命是物质运动的高级形式,这种运动方式是通过蛋白质来实现的,所以蛋白质有极其重要的生物学意义。人体的生长、发育、运动、遗传、繁殖等一切生命活动都离不开蛋白质。生命运动需要蛋白质,也离不开蛋白质。
**蛋白质是荷兰科学家格利特·马尔德在1838年发现的。**他观察到有生命的东西离开了蛋白质就不能生存。蛋白质是生物体内一种极重要的高分子有机物,占人体干重的54%。蛋白质主要由氨基酸组成,因氨基酸的组合排列不同而组成各种类型的蛋白质。人体中估计有10万种以上的蛋白质。生命是物质运动的高级形式,这种运动方式是通过蛋白质来实现的,所以蛋白质有极其重要的生物学意义。人体的生长、发育、运动、遗传、繁殖等一切生命活动都离不开蛋白质。生命运动需要蛋白质,也离不开蛋白质。
 人体内的一些生理活性物质如胺类、神经递质、多肽类激素、抗体、酶、核蛋白以及细胞膜上、血液中起“载体”作用的蛋白都离不开蛋白质,它对调节生理功能,维持新陈代谢起着极其重要的作用。人体运动系统中肌肉的成分以及肌肉在收缩、作功、完成动作过程中的代谢无不与蛋白质有关,离开了蛋白质,体育锻炼就无从谈起。
人体内的一些生理活性物质如胺类、神经递质、多肽类激素、抗体、酶、核蛋白以及细胞膜上、血液中起“载体”作用的蛋白都离不开蛋白质,它对调节生理功能,维持新陈代谢起着极其重要的作用。人体运动系统中肌肉的成分以及肌肉在收缩、作功、完成动作过程中的代谢无不与蛋白质有关,离开了蛋白质,体育锻炼就无从谈起。
在生物学中,蛋白质被解释为是由氨基酸借肽键联接起来形成的多肽,然后由多肽连接起来形成的物质。通俗易懂些说,它就是构成人体组织器官的支架和主要物质。蛋白质缺乏:成年人:肌肉消瘦、肌体免疫力下降、贫血,严重者将产生水肿。未成年人:生长发育停滞、贫血、智力发育差,视觉差。蛋白质过量:蛋白质在体内不能贮存,多了肌体无法吸收,过量摄入蛋白质,将会因代谢障碍产生蛋白质中毒甚至于死亡。
2021年10月30日,中国农业科学院饲料研究所发布,我国在国际上首次实现从一氧化碳到蛋白质的合成,已经形成万吨级的工业生产能力,获得首个饲料和饲料添加剂新产品证书。该证书由农业农村部于2021年8月颁发,新饲证字(2021)01号。
2022年7月,谷歌旗下人工智能公司DeepMind进一步破解了几乎所有已知的蛋白质结构,其AlphaFold算法构建的数据库中如今包含了超过2亿种已知蛋白质结构,为开发新药物或新技术来应对饥荒或污染等全球性挑战铺平了道路。4
分类
需求情况分类
食物中的蛋白质必须经过肠胃道消化,分解成氨基酸才能被人体吸收利用,人体对蛋白质的需要实际就是对氨基酸的需要。吸收后的氨基酸只有在数量和种类上都能满足人体需要身体才能利用它们合成自身的蛋白质。营养学上将氨基酸分为必需氨基酸和非必需氨基酸两类。
必需氨基酸指的是人体自身不能合成或合成速度不能满足人体需要,必须从食物中摄取的氨基酸。对成人来说,这类氨基酸有8种,包括赖氨酸、蛋氨酸、亮氨酸、异亮氨酸、苏氨酸、缬氨酸、色氨酸、苯丙氨酸。对婴儿来说,有9种,多一种组氨酸。
非必需氨基酸并不是说人体不需要这些氨基酸,而是说人体可以自身合成或由其它氨基酸转化而得到,不一定非从食物直接摄取不可。这类氨基酸包括甘氨酸、丙氨酸、丝氨酸、天冬氨酸、谷氨酸(及其胺)、脯氨酸、精氨酸、组氨酸、酪氨酸、胱氨酸。有些非必需氨基酸如胱氨酸和酪氨酸如果供给充裕还可以节省必需氨基酸中蛋氨酸和苯丙氨酸的需要量。
食物蛋白质的营养价值取决于所含氨基酸的种类和数量,所以在营养上尚可根据食物蛋白质的氨基酸组成,分为完全蛋白质、半完全蛋白质和不完全蛋白质三类。
1.完全蛋白质所含必需氨基酸种类齐全、数量充足、比例适当,不但能维持成人的健康,并能促进儿童生长发育,如乳类中的酪蛋白、乳白蛋白,蛋类中的卵白蛋白、卵磷蛋白,肉类中的白蛋白、肌蛋白,大豆中的大豆蛋白,小麦中的麦谷蛋白,玉米中的谷蛋白等。
2.半完全蛋白质所含必需氨基酸种类齐全,但有的氨基酸数量不足,比例不适当,可以维持生命,但不能促进生长发育,如小麦中的麦胶蛋白等。
3.不完全蛋白质所含必需氨基酸种类不全,既不能维持生命,也不能促进生长发育,如玉米中的玉米胶蛋白,动物结缔组织和肉皮中的胶质蛋白,豌豆中的豆球蛋白等。
外形分类
根据蛋白质分子的外形,可以将其分作3类:
1.球状蛋白质分子形状接近球形,水溶性较好,种类很多,可行使多种多样的生物学功能。
2.纤维状蛋白质分子外形呈棒状或纤维状,大多数不溶于水,是生物体重要的结构成分,或对生物体起保护作用。
3.膜蛋白质一般折叠成近球形,插入生物膜,也有一些通过非共价键或共价键结合在生物膜的表面。生物膜的多数功能是通过膜蛋白实现的。
结构种类
纤维蛋白(fibrous protein):一类主要的不溶于水的蛋白质,通常都含有呈现相同二级结构的多肽链许多纤维蛋白结合紧密,并为单个细胞或整个生物体提供机械强度,起着保护或结构上的作用。
球蛋白(globular protein):紧凑的,近似球形的,含有折叠紧密的多肽链的一类蛋白质,许多都溶于水。典形的球蛋白含有能特异的识别其它化合物的凹陷或裂隙部位。
角蛋白(keratin):由处于α-螺旋或β-折叠构象的平行的多肽链组成不溶于水的起着保护或结构作用蛋白质。
胶原(蛋白)(collagen):是动物结缔组织最丰富的一种蛋白质,它是由原胶原蛋白分子组成。原胶原蛋白是一种具有右手超螺旋结构的蛋白




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国