

01
先打个比方来总体认识一下动脉粥样硬化的形成。清澈的流水在河里流动,当水里泥沙过多时,水流速度会变慢,而且泥沙容易沉积在河底坑洼不平的地方,渐渐地在河底形成淤泥。
在动脉粥样硬化的形成过程中,血液中的低密度脂蛋白和极低密度脂蛋白就好比是泥沙,而高血压、吸烟等刺激因素所引起的血管内皮细胞损伤就好比河底的坑洼,低密度脂蛋白和极低密度脂蛋白很容易沉积在损伤的血管内皮细胞下,渐渐形成动脉粥样硬化。

▲ 动脉粥样硬化就是存在于动脉血管中的脂质泡沫细胞,炎症细胞等不良物质,在动脉血管内膜不断聚集形成的硬化性斑块
随着病程的进展,斑块会不断增大或斑块内出血使斑块隆起,导致血管腔变窄,甚至完全闭塞。斑块不断受到血流的冲击,若发生破裂,其内容物将进入血流成为栓子,引发栓塞。
栓塞可引起急性供血中断,从而导致相应的器官出现缺血性病变,常发生于脑、心脏、肾脏、下肢等部位。


02
1. 高血压
高血压患者动脉粥样硬化发病率明显增高。高血压和动脉粥样硬化互为因果,二者常同时存在。
2. 高血脂
高胆固醇血症是动脉粥样硬化的致病性因素。
3. 吸烟
吸烟明显增加动脉粥样硬化的发病率,且与每日吸烟数量成正比。
4. 糖尿病
糖尿病患者动脉粥样硬化的发病率较无糖尿病者高两倍。
5. 肥胖
中心性肥胖者、体重在短时间内迅速增加者,更易患本病。
6. 遗传因素
家族中有年轻动脉粥样硬化患者,近亲发病率明显增高。

03
研究发现,**间充质干细胞(MSCs)**可以分化为内皮细胞,加速受损内皮修复,抑制动脉狭窄的形成。另外,体外的间充质干细胞能够向受损部位募集,并进一步分化为内皮细胞,修复损伤血管。
目前,已经有越来越多的研究证实了干细胞对于修复血管内皮,促进血管新生,以及通过调控炎症对动脉粥样硬化产生的作用。
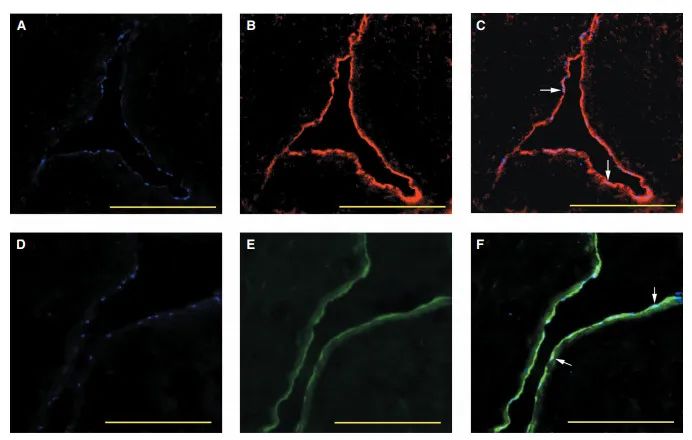
▲ 间充质干细胞治疗后,切片显示移植细胞参与修复血管,向内皮细胞分化(图b)
研究发现脐带组织中提取出的干细胞,能够在缺血微环境条件下分化成内皮细胞,参与血管新生,促进缺血局部的血流恢复。
那么,干细胞又是如何从这几方面“着手”来做到预防动脉粥样硬化的?
1. 调节脂质代谢
动脉粥样硬化是一种**循环脂质(例如血液中的脂肪和胆固醇)**沿着动脉壁聚集的病症。这种脂肪物质变厚并形成称为斑块的结构,斑块会变窄,并最终可能阻止血液流过动脉。而干细胞在调节脂质代谢上有着不错疗效。
在《Stem Cell Res Ther》发表的一篇文章中,研究者收集了78名使用自体干细胞治疗动脉硬化的患者数据,包括他们给药前后的脂质分布、内膜中膜厚度 (IMT)等。

▲ 数据表明:脂肪干细胞给药对发生动脉硬化的患者是安全有效的
而当研究者对比后发现:12名在治疗前高密度脂蛋白值异常 (≤ 40mg/dL) 患者,有11名 (91.7%) 在治疗后改善;18例IMT值异常(≥1.1mm)的患者,在治疗后IMT值均显著减少;28例残余样颗粒胆固醇水平异常患者里,有24例得到改善(85.7%)。10名临界动脉硬化疾病的患者在接受干细胞治疗后得到改善,例如低密度脂蛋白降低和甘油三酯水平降低。
实验证实:脂肪干细胞可以改善血清中的高密度脂蛋白,低密度脂蛋白和残余样颗粒胆固醇水平,调节脂质代谢,能够安全有效地改善动脉粥样硬化。
2. 内皮细胞保护
通过实验证明,干细胞可增强内皮细胞分化,提高内皮细胞活力,加速受损动脉内膜的修复过程,减少或消除斑块的堆积。
这主要得益于干细胞的旁分泌功能,它能分泌肝生长因子、白介素8、血管生成素等血管生成因子,促进血管生成与重塑,恢复内皮细胞功能,并减少细胞凋亡。
英国伦敦大学的研究人员的一项研究试验中,他们使用荧光标记来追踪一种被称为红系骨髓祖细胞(erythromyeloid progenitor, EMP)的干细胞命运。已知这些细胞会产生红细胞和某些类型的免疫细胞,在培养皿中培养的EMP干细胞也会产生内皮细胞。
这一发现,改变了人们对血管是怎样产生的科学认识,使用干细胞产生新的血管和修复受损血管成为可能。
3. 清除炎症细胞
干细胞移植能清除炎症细胞进而减缓AS进程,主要表现为减少浸润的炎性巨噬细胞迁移、抑制其活化、改变巨噬细胞的可塑性、打破M1/M2的平衡、调节T/B细胞的免疫平衡。
研究显示:动脉粥样硬化从斑块发展到破裂,每一步都伴随着炎症,具有调节、抑制炎症潜力的干细胞疗法自然成了科学家们的重点研究对象。
2019年发表于《Journal of Clinical Medicine》的一篇综述显示:目前已有大量研究证实干细胞在动脉粥样硬化上的炎症调节作用,主要机制在于:它能产生大量的抗炎因子(包括IL-10和TGF-β1),同时抑制促炎因子(如IL-1β,IL-6和TNF-α),它还能抑制NK细胞增殖与T细胞分化,从而抑制炎症反应,减缓斑块的形成。
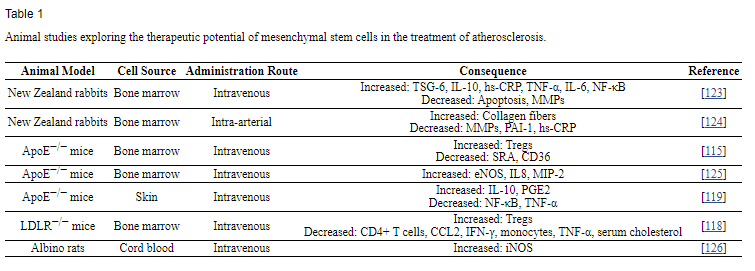
▲ 干细胞在动物实验中治疗动脉粥样硬化中的效用
而干细胞不仅是“抗炎"好手,它还是一个维持平衡的帮手,它能通过分泌细胞营养因子如KGF、HGF、GM-CSF、Ang-1等去改善细胞的微环境,为免疫系统保驾护航。
4. 支持血供造血
在AS的修复过程中提供营养物质,干细胞移植支持造血功能,加速体内的营养物质交换,提高血管修复效率,促进新血管的生成。
据ClinicalTrials.gov数据显示 ,目前已启动超10项干细胞移植的临床试验项目,应用于动脉粥样硬化的研究工作。
来自美国Ochsner-LSU健康科学中心的研究者发现:依托于强大的旁分泌功能,干细胞能重塑患者的血管,维持脑血流量。

▲ 文章刊登于《Stem Cells》,影响因子6.277
研究发现胎盘间充质干细胞(hPMSCs)能够表达大量的血管紧张素转换酶-2 (ACE-2),它的产物(Ang1-7)与相关受体结合后,能发挥血管舒张、抗氧化、和抗炎等作用。
ACE2/Ang1-7信号也一直被认为是中风治疗的重要靶点。而间充质干细胞所释放的胞外囊泡能够到达脑部,其“运输”的ACE-2及其产物可以维持急性脑中风模型小鼠的脑血流量,缩小脑梗死体积,对防止中风慢性脑结构和功能损伤的延续具有重要意义。
而除了以上一些主要的作用机制外,干细胞还可通过分化诱导为健康的细胞,在机体发挥各种作用,维持机体状态的稳定,从而改善健康状况。
由此可见,***干细胞调理可各种脂类代谢功能,能降低血液中的总胆固醇、甘油三酯、低密度脂蛋白浓度等指标,提高机体的糖代谢功能,有效降低血糖水平,提高机体能量的供给和消耗平衡功能,从而达到改善高血脂症状,帮助预防或干预脑中风、冠心病等风险,***可以说对于动脉粥样硬化的调理与治疗,干细胞无疑是一种非常合适的手段,具有广阔的应用前景。
免责声明:内容来源于网络,版权归原作者所有。本文为科普性知识,仅作信息交流之目的,不做商业用途,如涉及作品内容、版权和其它问题,请联系我们删除
END




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国