多糖基薄膜因其具有生物相容性、生物活性和生物可降解性等而备受医学领域关注。值得一提的是,多糖基薄膜在生理环境下的力学性能衰减和结构失稳严重限制了其应用。
针对该问题,中国科学技术大学俞书宏院士课题组受到自然界中鱼鳞和皮肤等富水生物组织所具有的分级异质纤维结构及其优异的力学性能和稳定性启发,提出一种基于分子/纳米双尺度网络的非均质交联与水合作用的力学增强机制,进而制备出一种与单尺度网络结构材料相比具有优异的湿态力学性能的多糖基纳米复合薄膜,进一步将功能化修饰的薄膜应用于引导骨再生研究,最终展示出所提出的力学增强机制的卓越性并将为指导制备先进的生物医用材料提供更多可能。相关研究成果发表于《国家科学评论》(National Science Review 2024, 11, nwad333)。
基于所提出的力学增强机制,研究团队首先使用海藻酸钠(SA)和细菌纤维素纳米纤维(BC)基元,按序结合钙离子交联和再水合步骤,制备出具有异质交联水合双尺度网络结构的多糖基纳米复合薄膜。系统性力学测试(包括单轴拉伸、缝线拉伸和原位撕裂拉伸等)结果表明,所提出的双尺度网络结构复合膜较单一尺度网络结构的薄膜在拉伸强度、韧性、杨氏模量、缝线拉力和断裂能等方面均具有显著优势(图1)。
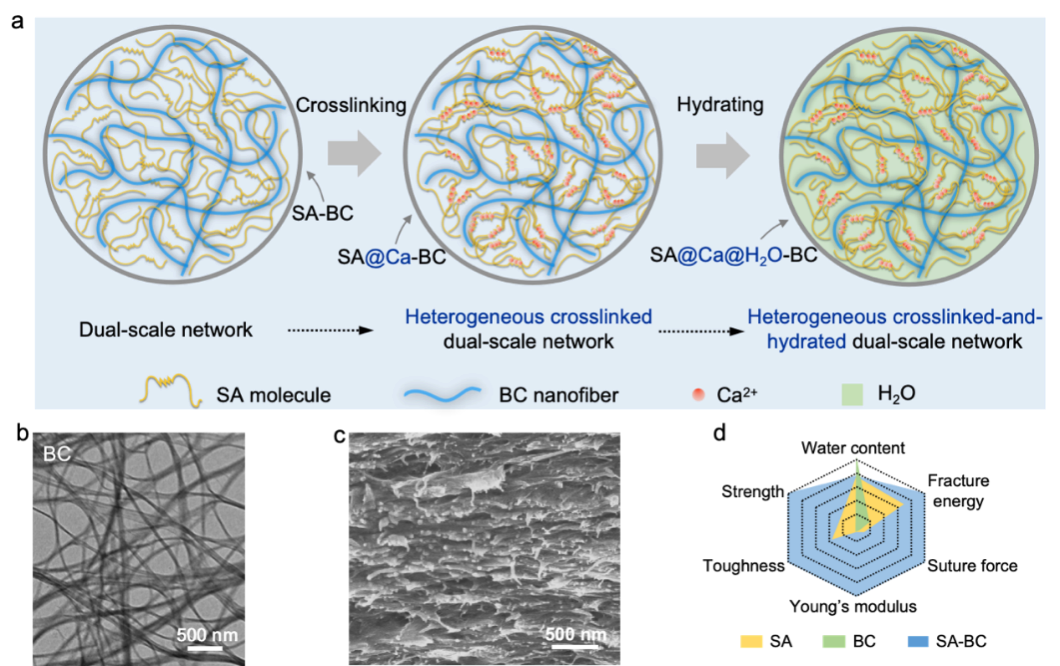
图1.a. 异质交联水合双尺度网络结构多糖基薄膜的制备示意图。b.BC的透射电镜图,呈现出典型的纳米纤维网络结构。c. 多糖基复合薄膜的横截面扫描电镜图,海藻酸钠和细菌纤维素纳米纤维相互交织。d. 具有双尺度网络结构的多糖基纳米复合薄膜的综合力学性能。
结合理论模拟研究,进一步分析该力学增强机制可知,Ca2+交联和水合作用主要发生于SA分子网络结构中,经过Ca2+交联和水合后的SA分子网络结构较为稳定,可起到屏障作用限制水分子的过度侵入渗透。在这种情况下,BC纳米纤维网络结构可免受水分子的侵入影响,有效发挥力学增强的作用。整体上,分子尺度和纳米尺度双重网络各司其职,最终所构筑的复合薄膜展现出优异的湿态力学性能,能够在湿态条件下稳定存在并提供结构支撑,为其在生理环境的医学应用奠定了基础。研究团队对所构筑的多糖基薄膜进行壳聚糖(CS)-羟基磷灰石(nHAP)薄层功能化修饰,构筑出双层膜,并对其进行生物学应用探索。系统性的体内、外实验结果表明,经过功能化修饰后的多糖基薄膜具有良好的生物相容性、抑菌性和成骨性等生物学性能,展示出在生物医学领域中巨大的应用潜力(图2-3)。
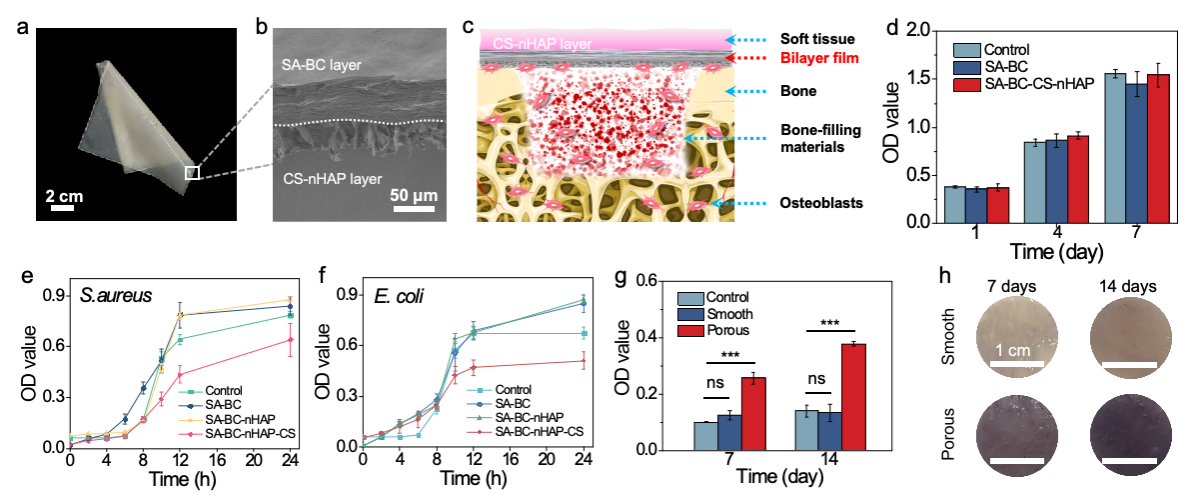
图2.a-c.通过功能化修饰而构筑出的双层膜应用于引导骨再生(a.双层膜光学图像,b.双层膜横截面扫描电镜图,c.双层膜应用于引导骨再生示意)。d-h.双层膜具有良好的生物学性能(d. 生物相容性,e-f.抑菌性,g-h. 体外诱导成骨性)。
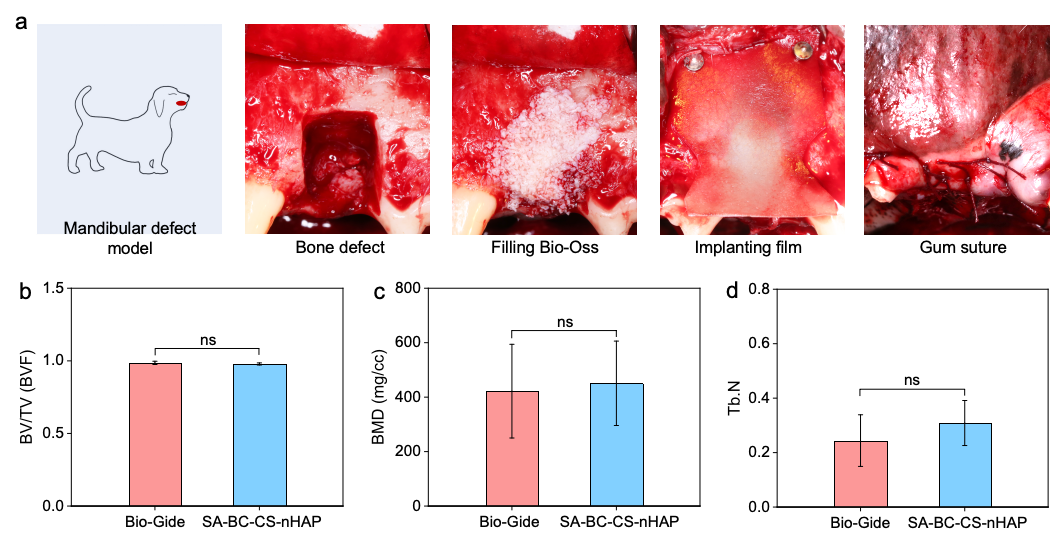
图3.犬下颌骨修复实验表明双层膜具有良好的成骨能力。
该研究提出了一种仿生异质交联水合双尺度网络结构的力学增强策略,并基于此制备出一种在湿态环境下具有优异力学性能的纳米复合薄膜材料,通过功能化薄层修饰展示了该复合膜在生物医学引导骨再生领域的应用潜力,为先进仿生医用材料的设计制备提供一条合理的路径,将促进有关仿生材料在医学领域中的应用。






 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国