5月8日,国家药监局党组成员、副局长黄果带队,到北京部分企业调研细胞和基因治疗产品研发进展,并主持召开企业和科研机构座谈会,围绕鼓励创新和加强监管进行交流。
黄果强调,细胞和基因治疗产品已成为全球医药发展的前沿和热点,药品监管部门要加强政策引导,助推产业高质量发展。要提高研发质量,完善评价体系标准,加强沟通交流服务,让细胞和基因治疗产品早日惠及患者。
据悉,经药品监管部门批准,我国已有400余个细胞和基因治疗产品正在开展药物临床试验,其中干细胞产品近一百个。适应症涵盖了肿瘤、呼吸系统、神经系统、心血管系统、消化系统、风湿免疫等多类疾病。
临床阶段的国产细胞疗法适应症分布情况
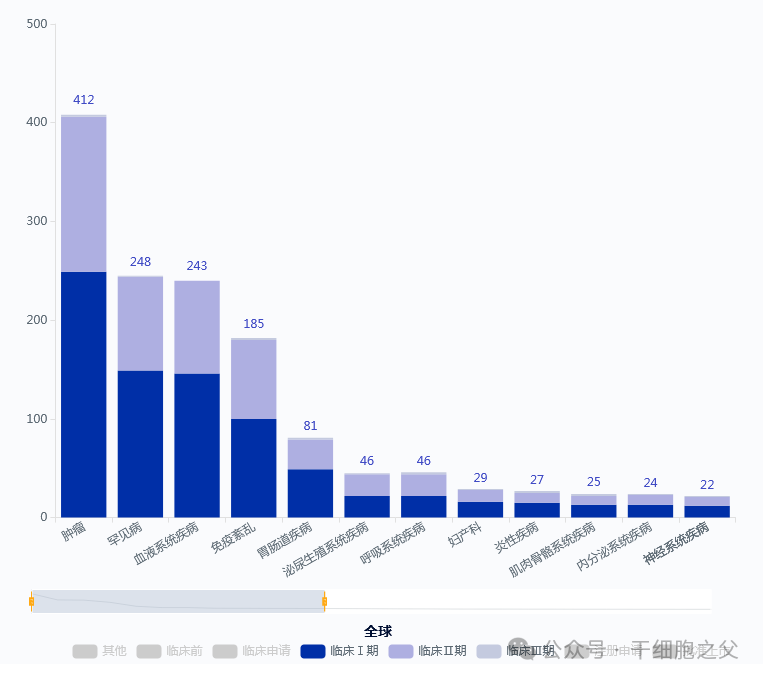
图片来源:药智数据
干细胞是当今医学研究领域最前沿、最热门的方向之一。我国相关研究也持续升温,并诞生了一批具有国际影响力的原创成果。
截至5月15日,国家药品监督管理局药品审评中心发布的临床试验默示许可显示,共有62款间充质干细胞新药获得临床试验许可。这些药品的干细胞主要来源包括脐带、脂肪、宫血、羊膜、骨髓、牙髓、胎盘等,涉及到30多家公司。
适应症涵盖了多个疾病类型,包括神经科(脑卒中、脊髓损伤、老年痴呆症)、骨科(膝骨关节炎、股骨头坏死)、肝病、肺病、肠病、风湿免疫科(狼疮、硬皮病、强直性脊柱炎、皮炎、类风湿关节炎)、皮肤病与烧伤、内分泌科(糖尿病足溃疡)、牙科、妇产科、心内科、血液内科(GvHD)等。
受理号药品名称与适应症明细如下:
1、神经科(脑卒中、脊髓损伤、老年痴呆症)7款
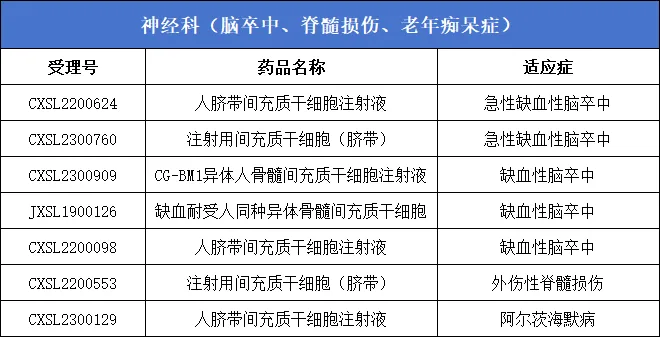
2、骨科(膝骨关节炎、股骨头坏死)8款
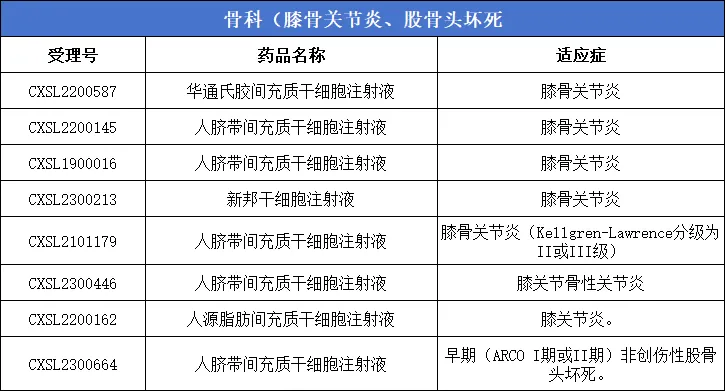
3、肝病:6款
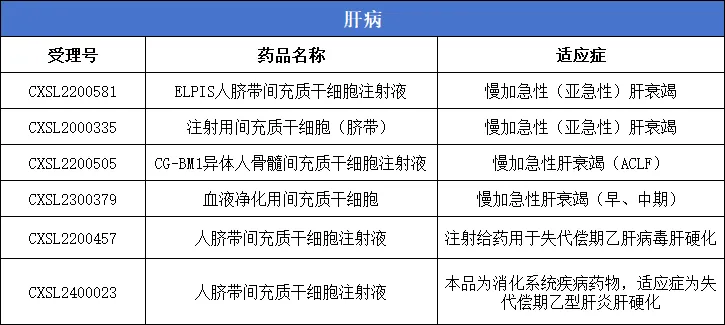
4、肺病:14款
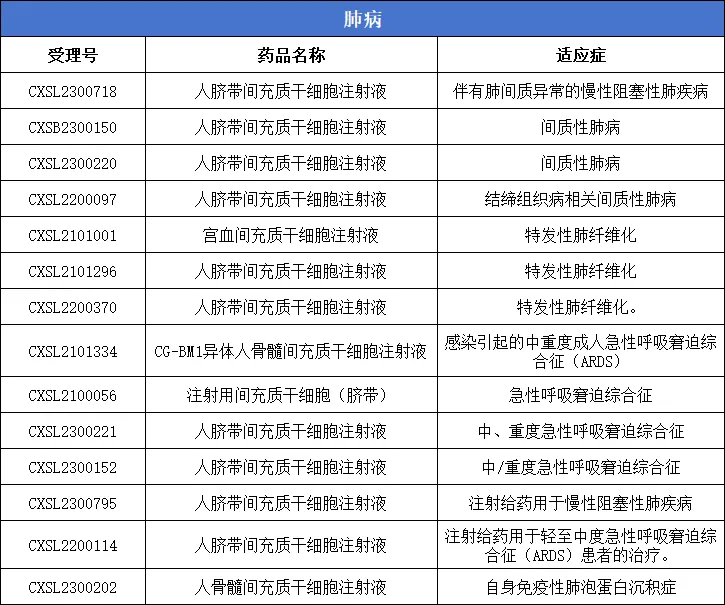
5、肠病:5款
6、风湿免疫科(狼疮、硬皮病、强直性脊柱炎、皮炎、类风湿关节炎)7款
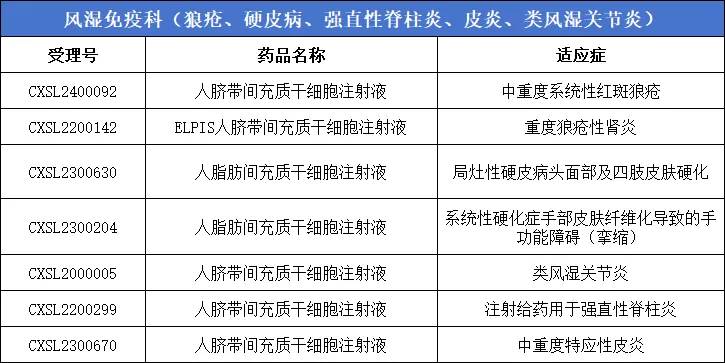
7、皮肤病与烧伤:2款

**8、内分泌科(糖尿病足溃疡)**3款
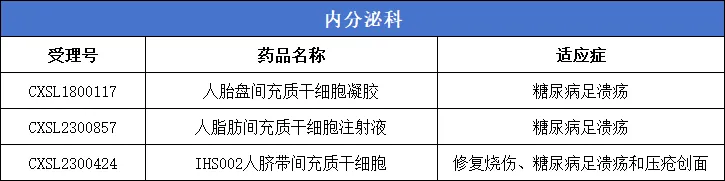
9、牙科:1款

10、妇产科:1款

11、心内科:2款
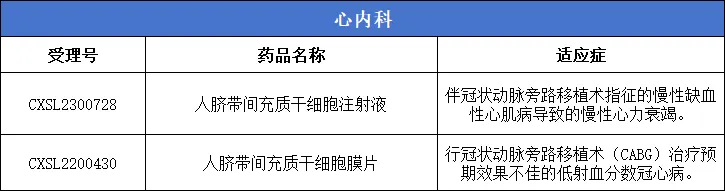
13、血液内科(GvHD)
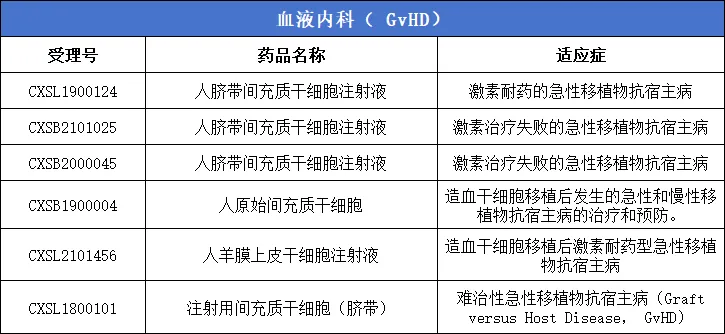
干细胞疗法作为一项新兴的技术,需要进行强有力的监管,在保证患者健康的同时,还有利于推动整个行业的健康发展。
2023年全球干细胞治疗市场收入为2.86亿美元左右,且具有广阔的发展潜力。预计到2028年,干细胞市场估值将高达6.15亿美元。
目前全球范围内获批的干细胞产品主要集中在日本、韩国、美国、欧盟等地。近几年,我国也在大力扶持干细胞技术的发展,相信在不久的将来,干细胞将会像“智能手机”一样,深入影响我们每个人的生活。我们也期待随着干细胞药物研究规模的不断扩大,再生医疗技术能让更多的患者获益。






 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国