
学科新知聚焦业内权威专家,从学科发展的高度全面梳理、深入解读肿瘤医学各领域的国内外研究现状与进展,为医护以及科研人员立体勾勒恶性肿瘤领域的最新研究进展,赋能临床科研和学术推广,为医学研究者搭建一个共享知识、交流经验的平台,推动肿瘤医学领域的国际化合作与发展。
本期学科新知分享的是遵义医科大学第二附属医院胸部肿瘤科何思思教授和遵义医科大学附属医院胸外科陈成教授对非小细胞肺癌耐药临床前沿进展的精彩解读。
概述
/ CONTENTS
EGFR突变是我国晚期非小细胞肺癌(NSCLC)中最常见的基因突变类型,自2010年开始,表皮生长因子受体-酪氨酸激酶抑制剂(EGFR-TKI)成为EGFR突变NSCLC患者的首选一线治疗方案,然而尽管其初期反应良好,但在一年内,高达60%的患者就会因T790M突变产生耐药性。
为克服这一挑战,二代和三代EGFR-TKI药物相继问世,其中以奥希替尼为代表的第三代EGFR-TKI成功解决了T790M耐药突变的难题。但靶向药最终都可能会出现耐药,当第三代EGFR-TKI出现耐药时,又该如何解决呢?
1
靶向治疗下EGFR突变非小细胞肺癌患者耐药机制
01
获得性EGFR-TKI耐药机制
不同EGFR TKI的依赖性和非依赖性耐药发生率不同。一、二代EGFR TKI治疗主要发生EGFR依赖性耐药,接受三代EGFR TKI作为二线治疗的患者中约20%发生EGFR依赖性耐药,一线应用发生率则为15%~20%(图1)。
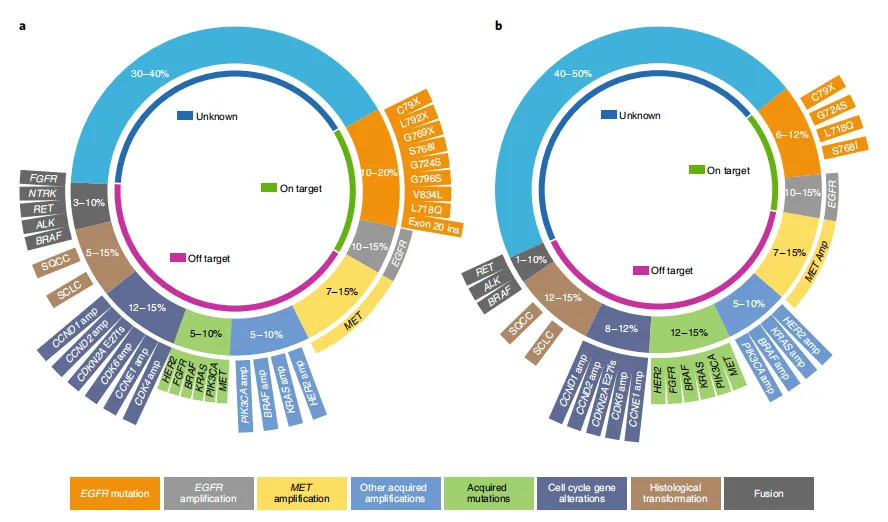
图1 第三代EGFR TKI奥希替尼获得性耐药机制
(a)二线治疗(b)一线治疗
(1)EGFR依赖性耐药机制
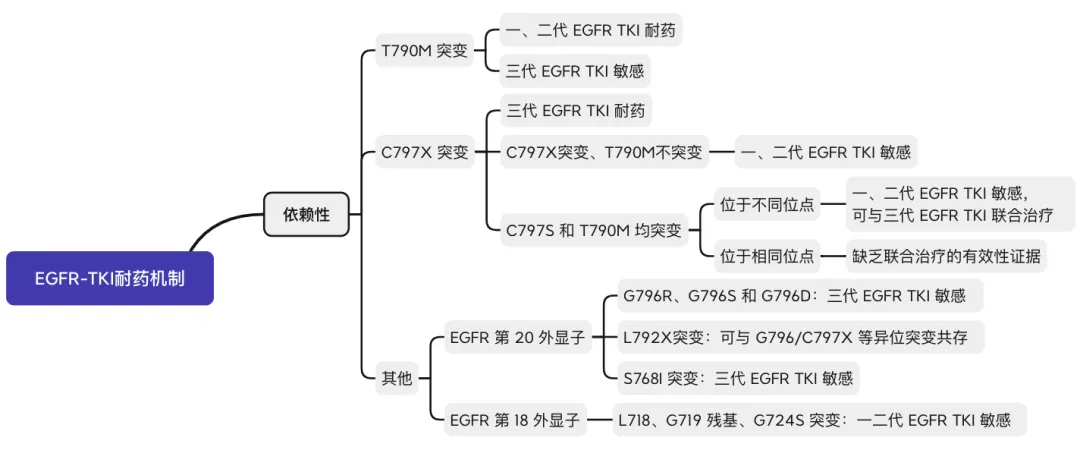
(2)EGFR非依赖性耐药机制
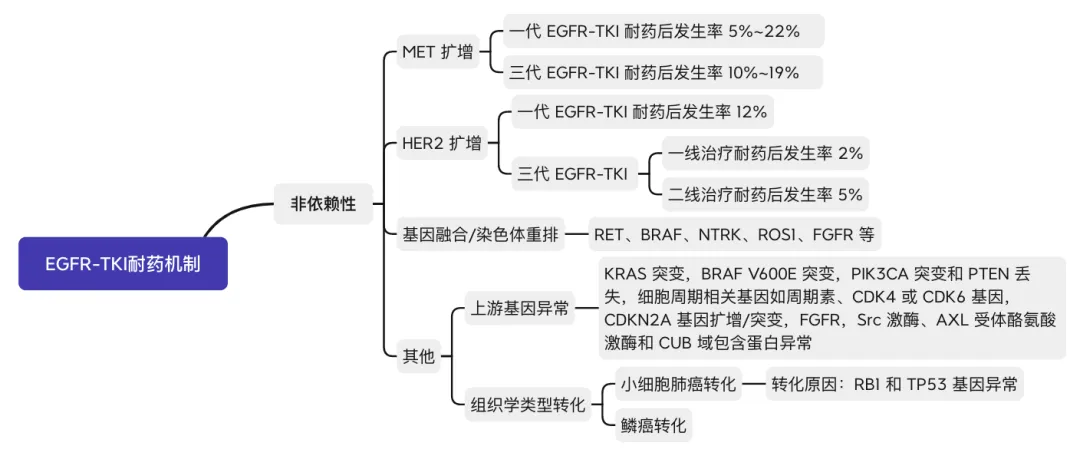
02
表观遗传在耐药中的作用
表观遗传调控作为一种独立于DNA序列变化的基因表达可遗传改变,其调控异常可导致癌基因的过度表达以及抑癌基因的沉默,从而促进肿瘤的发生、发展和耐药性的形成。
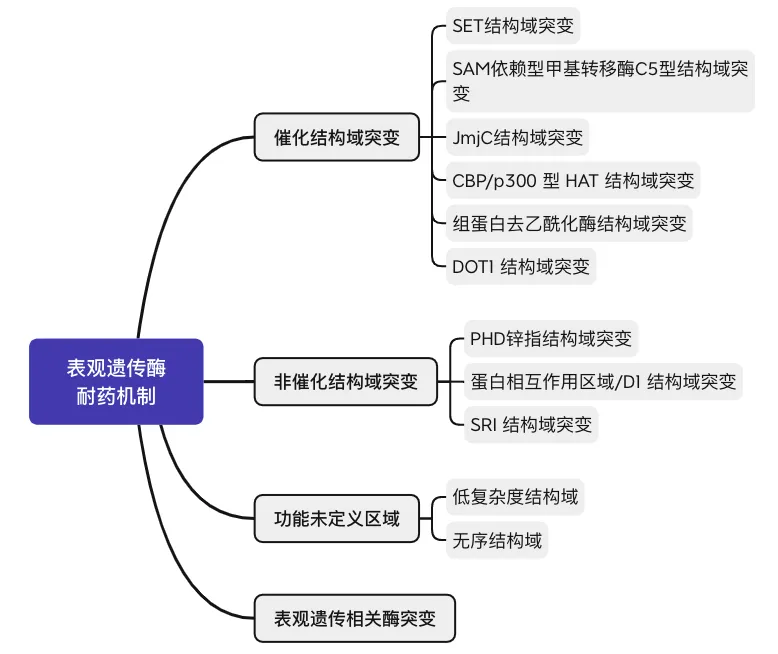
2
如何逆转耐药?
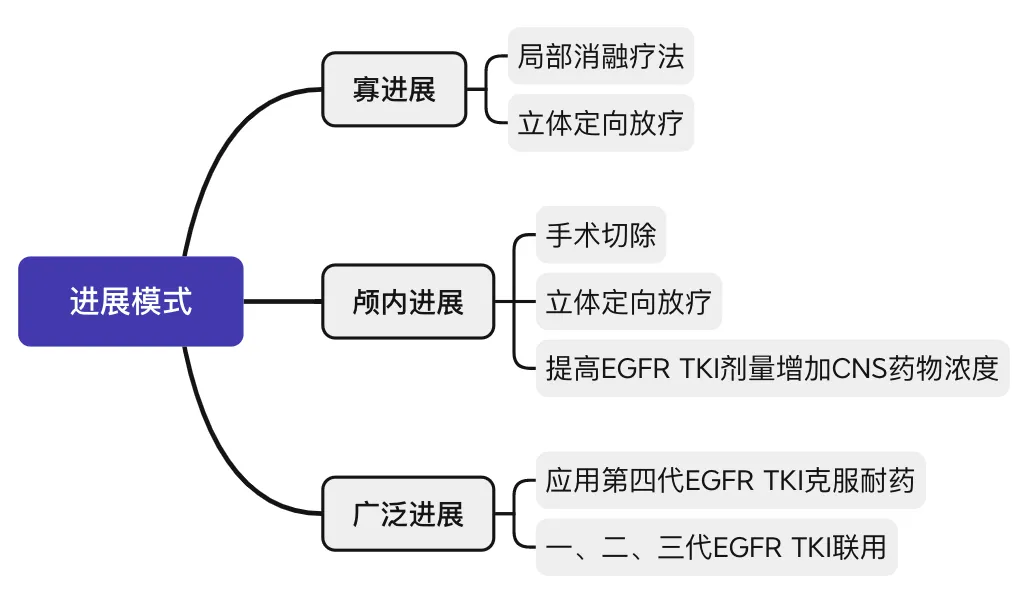
接受靶向治疗后,患者的临床疾病进展速度和模式差异很大。因此,需要根据疾病进展的特征,结合对上述耐药性机制的理解,确定最佳的管理策略。
01
披荆斩棘,四代EGFR-TKI初现成效
针对EGFR-TKI部分特异性耐药机制,多款第四代EGFR-TKI现已问世,部分药物已经进入临床试验阶段,虽仍需进一步临床研究验证其疗效和安全性,但这些新药物的出现无疑为EGFR TKI耐药的治疗提供了新的思路和可能性。
(1)EAI045
EAI045+西妥昔单抗在L858R/T790M±C797S Ba/F3细胞和L858R/T790M±C797S基因工程小鼠模型中均显示出理想的抑瘤效果,EAI045联合PD-1抑制剂可能是T790M和C797S突变耐药的新型抑制剂。
(2)JBJ-04-125-02
EAI045须与西妥昔单抗联合应用,但西妥昔单抗会因脱靶产生毒副作用。因此新型变构抑制剂—JBJ-04-125-02应运而生,可独立在体内体外抑制EGFR L858R–T790M–C797S形式的EGFR。
(3)BLU-945
BLU-945对EGFR 19Del或L858R/T790M/C797S三重突变的癌细胞具有强大的杀伤力。在动物实验中单用第三代靶向药无效,而BLU-945治疗能使肿瘤基本稳定或持续缩小;联合奥希替尼治疗更能迅速使肿瘤完全消失。
02
另辟蹊径,联合疗法助力患者求生
(1)双靶联合治疗
首先可考虑同时给予一代和三代EGFR TKI,EGFR T790M和C797S位于不同位点,第一代EGFR TKI(靶向C797S)与第三代TKI(靶向T790M)联合应用可恢复EGFR抑制,提供短期临床益处,可能具备持久的反应潜力。
此外可考虑EGFR TKI与其他靶向药物的联合应用以解决脱靶耐药性。目前包括ORCHARD试验(NCT03944772)在内的多项试验正在评估奥希替尼与各种非EGFR靶向疗法联合治疗在EGFR突变的NSCLC患者中的安全性和有效性。
(2)靶向联合化疗/抗血管治疗
1)靶向联合化疗
EGFR TKI与化疗联合使用可有效延迟EGFR TKI耐药性,从理论上来说,最大限度地使用细胞减灭术可以最大程度地减少或根除任何TKI耐受的存活细胞亚克隆,从而延缓耐药克隆和临床复发的出现。Ⅲ期NEJ009试验也证实,化疗+吉非替尼联合治疗与单用吉非替尼治疗相比PFS显著延长(20.9个月:11.9个月;HR=0.490;P<0.001)
2)靶向联合抗血管治疗
抗血管生成药物贝伐珠单抗可改变肿瘤血管结构,影响药物的输送和有效性,抑制肿瘤生长。临床前研究数据表明,抗血管生成剂与EGFR TKI具有协同作用。厄洛替尼与贝伐珠单抗的联合应用也在单臂Ⅱ期试验BELIEF中显示出活性,并在随机Ⅱ期试验(JO25567)中与单用厄洛替尼相比显示出显著的PFS益处。
(3)免疫联合化疗
目前免疫检查点抑制剂(ICI)已被广泛用于缺乏可靶向驱动突变的NSCLC患者,但其在EGFR阳性NSCLC治疗中的作用尚未明确。既往研究数据表明,抗PD-1/PD-L1抗体在EGFR突变的NSCLC患者中的疗效有限,进行一线ICI单药治疗或ICI-化疗联合治疗均未观察到明显受益。
IMpower150试验将阿替利珠单抗和贝伐珠单抗加入铂类双药化疗(ABCP方案)是唯一一种对EGFR突变患者亚组显示受益的免疫肿瘤学方案,ABCP组在携带EGFR敏感突变的患者亚组中OS和PFS显著提高,证实免疫肿瘤学和抗血管生成药物在EGFR突变环境中可能具有协同作用。
遵义医科大学第二附属医院胸部肿瘤科何思思教授与遵义医科大学附属医院胸外科陈成教授共同牵头的一项回顾性研究探讨了替雷利珠单抗联合贝伐珠单抗、培美曲塞和卡铂(TBCP组)治疗经TKI治疗失败的晚期驱动基因突变非鳞状NSCLC的疗效与安全性,该研究详细内容即将在2024 ASCO上发布。数据分析表明,与接受贝伐珠单抗、卡铂和培美曲塞(BCP组)治疗的患者相比,TBCP组的mPFS(14.20个月 vs 8.65个月)和ORR(66.7% vs 33.3%)显著高于BCP组,表现出良好的抗肿瘤疗效和可控的安全性。未来需通过更大样本量的前瞻性临床试验进一步确认。
遵义医科大学第二附属医院胸部肿瘤科与遵义医科大学附属医院胸外科已将上述研究纳入科室临床实践和科研方向之一,以进一步提升患者的治疗效果和生存质量,为患者提供更加全面和个性化的治疗方案。


参考文献(向上滑动阅览)
[1]Passaro A, Jänne PA, Mok T, Peters S. Overcoming therapy resistance in EGFR-mutant lung cancer. Nat Cancer. 2021;2(4):377-391.
[2]Chen S, Zhao Y, Liu S, et al. Epigenetic enzyme mutations as mediators of anti-cancer drug resistance. Drug Resist Updat. 2022;61:100821.
[3]Cooper AJ, Sequist LV, Lin JJ. Third-generation EGFR and ALK inhibitors: mechanisms of resistance and management [published correction appears in Nat Rev Clin Oncol. 2022 Nov;19(11):744]. Nat Rev Clin Oncol. 2022;19(8):499-514.
[4]Cortiula F, Reymen B, Peters S, et al. Immunotherapy in unresectable stage ⅡI non-small-cell lung cancer: state of the art and novel therapeutic approaches. Ann Oncol. 2022;33(9):893-908.




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国