容易复发、感染,长期生存率低,这是白血病治疗中长久以来面临的难题。虽然随着医学的进步,白血病治疗取得了突破性进展,CAR-T细胞治疗和异基因造血干细胞移植为不少难治复发白血病患者带来生的希望,但问题还没有被彻底解决。临床治疗中,部分接受CAR-T细胞治疗的患者依旧出现了复发,同时移植物抗宿主病(GVHD)等异基因造血干细胞移植相关的并发症会导致死亡率升高。
如何将命悬一线的病人拉回来?浙江大学医学院附属第一医院、良渚实验室的黄河教授团队设计了一种全新的CAR-T细胞治疗序贯异基因造血干细胞移植一体化方案,将两种治疗手段进行了强强联合,成功解决了传统治疗方案遗留的多项难题。
北京时间4月25日,这项研究成果以“原创性论文”(Original Article)形式发表在医学领域顶级期刊《新英格兰医学杂志》上。浙江大学医学院附属第一医院、良渚实验室的胡永仙教授、张明明副主任医师和浙江大学博士研究生杨婷婷为论文共同第一作者,黄河教授、胡永仙教授、王东睿研究员和上海雅科生物科技有限公司张鸿声教授为论文共同通讯作者。
灵机一动 将危机化为转机
血液系统恶性疾病按照其细胞来源,可以分为B细胞肿瘤、T细胞肿瘤和髓系白血病三大类型。其中T细胞和髓系肿瘤恶性程度更高,也更容易复发和转移。目前,商业化的CAR-T细胞治疗也仅针对B细胞恶性肿瘤。CD7在多种T细胞肿瘤和30%的急性髓性白血病中高表达,因此备受研究者们关注。
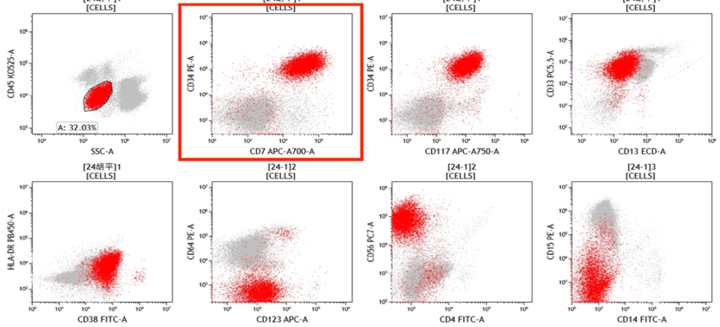
CD7分子在急性髓性白血病细胞中高表达
黄河教授团队在前期研究中开发了靶向CD7的 CAR-T细胞,并通过临床研究验证其有显著疗效,但复发、感染的问题依然存在,要想进一步提高患者长期生存率,必须再出新招。目前医疗界的一个思路是在CAR-T免疫疗法后,再桥接异基因造血干细胞移植作为巩固治疗,然而在临床治疗中,困难重重。
“移植手术的前提是要体内基本没有肿瘤细胞,还要摧毁体内的造血和免疫系统,所以传统的移植方案需要先进行清髓性预处理化疗和移植物抗宿主病(GVHD)预防,所使用的化疗及免疫抑制药物具有较大毒性和副作用,同时会清除体内的CAR-T细胞影响其抗肿瘤效果。”黄河说。
同时这个过程对病人身体打击也很大,就好比长枪短炮一阵轰鸣后,敌人消灭了,战场也变废墟了,很多终末期病人不一定承受得了,就算病人过了大化疗这一关,后续的抗排斥反应治疗会降低免疫力,增加感染风险。
临床提出问题,基础研究立马跟进。团队里的两支队伍思维一碰撞,提出了一个大胆想法。
“部分患者在CD7 CAR-T治疗后出现严重的全血细胞减少及骨髓抑制。骨髓抑制本来是一个副作用,但如果能巧妙加以利用,正好可以满足异基因造血干细胞移植的条件。”这样一来,就能跳过清髓性预处理和移植物抗宿主病(GVHD)预防的中间环节,实现CAR-T免疫疗法和异基因造血干细胞移植的“无缝对接”。
实证研究 临床疗效更胜一筹
由此,团队设计了一种全新的CAR-T细胞治疗序贯异基因造血干细胞移植一体化方案:CD7 CAR-T细胞在患者体内快速扩增,彻底清除多药耐药的白血病细胞; 利用患者接受CD7 CAR-T细胞治疗后的骨髓抑制状态,避免allo-HSCT大剂量清髓性预处理化疗,直接回输同一供者来源的异基因造血干细胞;利用CAR-T细胞清除CD7阳性正常T淋巴细胞的特点,无需免疫抑制剂即可一定程度上预防GVHD;患者体内持续存在的CD7 CAR-T细胞以及造血干细胞移植后免疫重建的移植物抗白血病效应(GVL)共同预防白血病复发。这个方案一步到位,既让CAR-T细胞持续发挥作用,又能减少化疗药物对人体的毒副作用。
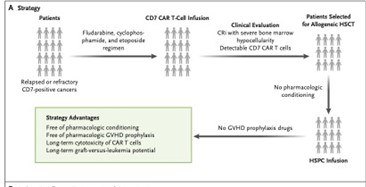
CD7 CAR-T序贯异基因造血干细胞移植新体系
在随后的临床研究中,这一新方案收获了显著疗效。患者原有的全血细胞减少都得到有效恢复,可评估的患者除1例自体造血恢复外,其余均达到完全供者嵌合。一年随访病人的长期生存率达到68%,而挽救性化疗只有20%,同时,治疗后的病人无需免疫抑制剂且allo-HSCT相关感染发生率显著降低。
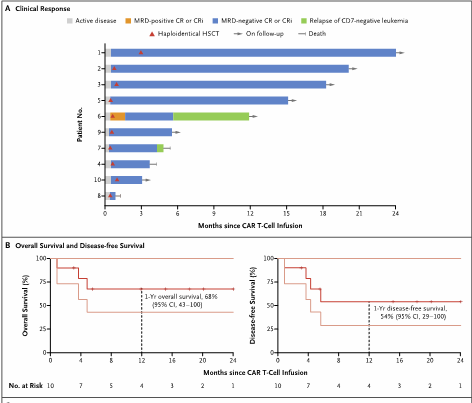
患者疗效和长期生存
“不仅病人的造血功能恢复良好,而且感染、复发、GVHD等常见并发症发生率明显下降。很大一部分患者都能适用这套方案并且从中受益。”黄河说。
来自绍兴的周大妈,今年68岁,白血病治疗后再次复发,身体非常虚弱,做不了常规移植手术,本来已经打算放弃治疗,来杭州接受了这套CAR-T细胞治疗序贯异基因造血干细胞移植一体化方案后,不仅恢复良好,不用吃抗排异药,而且生活质量有了很大提高,出院后还能帮忙带孙子。
临床治疗取得突破性成果,再次回到基础研究,正所谓知其然知其所以然。团队进一步对方案背后的机制开展了深入研究。所有患者体内均能检测到CAR-T细胞,正是它们长期发挥作用,一直在努力清除CD7阳性的肿瘤细胞,所以疾病得到了完全缓解。同时,长期存续的CAR-T细胞也清除了造血干细胞分化而来的CD7阳性T细胞,进而控制了GVHD。一系列研究从内源机制上解释了这套一体化方案效果显著的奥秘所在,为将来更大规模的临床试验打下基础。
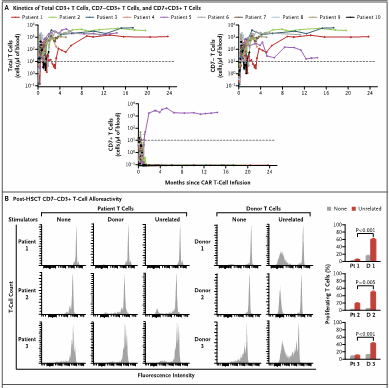
患者体内持续存在的CD7 CAR-T细胞
国际首创 被专家誉为“杭州方案”
团队首创的“强强联合”新方案为那些无法接受传统异基因干细胞移植的白血病患者提供了一种全新的治疗选择,为更多终末期恶性血液疾病患者带来新的希望,也为医学界探索更有效的治疗手段开辟了新的道路。
该一体化治疗体系也因其独特的设计和突破性的疗效,在2023年12月第65届美国血液学大会(ASH)做口头报告时被国际专家誉为“一石四鸟”的“杭州方案”:CAR-T细胞靶向清除肿瘤细胞;不需清髓性预处理化疗;无需免疫抑制剂预防GVHD;CAR-T长期存续与GVL共同发挥预防肿瘤复发的作用。
法国马赛大学血液学研究所主任Didier Blaise教授在《新英格兰医学杂》发表同期述评:“研究成果为该领域作出重要贡献,因为该方案为那些没有任何其他治疗选择的终末期患者提供了一种治愈性治疗策略。”

黄河说,这次的新成果也得益于团队此前的长期积累,以及多专业交叉融合、紧密协作,从基础研究、临床转化到临床应用的全链条式攻关突破,“我们希望不断通过科学研究反哺临床研究,提出新的治疗体系和方法,为病人带去生命的希望。”






 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国