在进化过程中,睡眠对于所有具有神经系统的生物来说都是普遍且必不可少的。但问题是,睡眠会导致更容易被猎杀。为什么动物会在捕食者的持续威胁下仍然要睡觉,以及睡眠如何影响我们的大脑,至今仍然是个谜。

图源:www.pexels.com
我们普遍的感觉是,睡眠是一件不可抗拒的事情,即便通过咖啡等饮品获得更长时间的清醒,但困倦感却会越来越重。因此睡眠不可能轻易通过药物来剥夺,这也暗示着睡眠本身就有维系生存的必要性。
为了解释睡眠的必要性,很多研究都从不同角度给出了答案:睡眠可以维持正常的激素分泌节律,可以降低心脑血管疾病的风险,甚至还可以维持我们皮肤的水润光滑。但这些理由还不足以让生物冒着被猎杀的风险也要睡觉,背后的根本原因依然扑朔迷离。
曾有研究显示,当我们清醒时,体内的睡眠压力会积聚。我们保持清醒的时间越长,这种压力就会增加,而在睡眠期间会下降,在一夜好眠后会降至最低。
是什么导致体内的睡眠压力增加到我们觉得必须睡觉的水平,晚上会发生什么将这种压力降低到我们准备开始新的一天的程度?或者说,睡眠压力的本质是什么?
科学家将目光投向了生命的核心——DNA。但DNA时时刻刻面临着断裂的危险,在我们白天辛勤学习或工作的时候,DNA就会出现大量的断裂,某些药物如奥沙利铂等也会通过诱导DNA断裂来促使细胞死亡。
但是学习和工作诱导的DNA断裂并不是毫无意义。由于DNA实在太过繁复,为了更加高效地让需要的基因快速表达,DNA会在特定位点断开,这样使得学习和工作需要的蛋白得以迅速合成。

图源:www.eurekalert.org
研究发现,工作学习的时间越长,注意力越是长时间集中,一天下来断裂的DNA就会越多。虽然它们保证了高效的运转,但是这样的机制显然遗害无穷。断裂的DNA就像是一颗定时炸弹,随时可能导致细胞死亡或者发生癌变。
近期Molecular Cell杂志上发表了一项新研究, 以色列的研究人员通过研究斑马鱼的睡眠机制发现,这些断裂的DNA会在睡眠过程中被修复,从而朝着解开睡眠谜团迈出新的一步。

图源:doi: 10.1016/j.molcel.2021.10.026.
研究团队发现,神经元中的DNA损伤在清醒期间会持续累积。当你沉迷于“996”时,大脑中过度的DNA损伤已经达到必须要降低的危险水平。
为了制造更多的DNA断裂,研究人员使用辐射等手段在斑马鱼中诱导了DNA损伤,以检查它如何影响睡眠。斑马鱼具有夜间睡眠的特性,也有与人类相似的简单大脑,是研究这种现象的最佳模式生物。
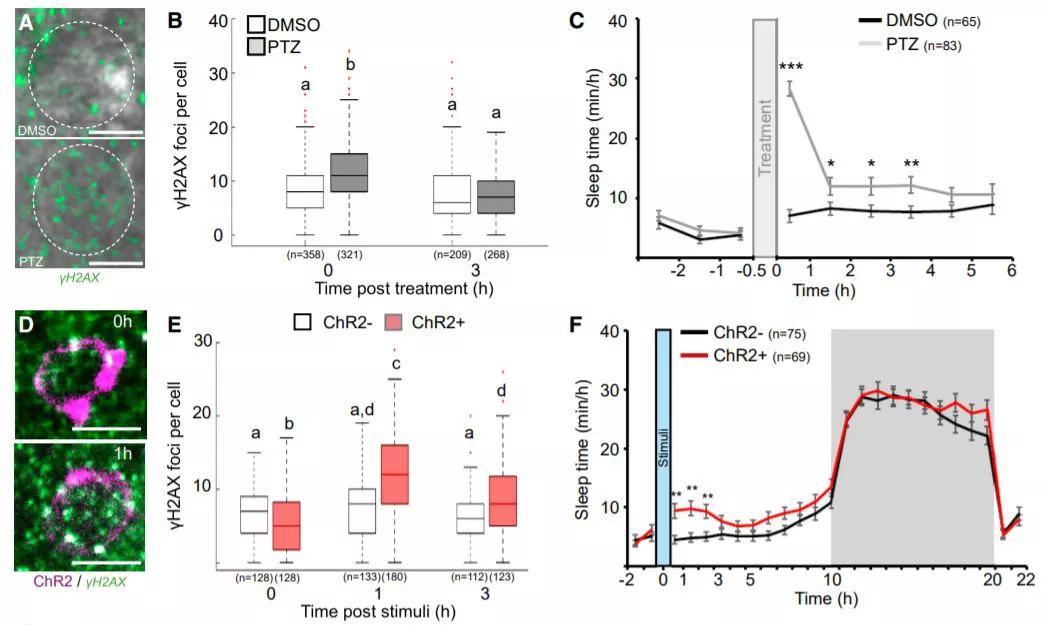
图源:doi: 10.1016/j.molcel.2021.10.026.
实验表明,在某个时刻DNA损伤的积累达到了最大阈值,并且睡眠压力增加到一定程度,以至于触发了睡眠的冲动,鱼就会进入睡眠状态。随后的睡眠促进了DNA修复,从而减少了DNA损伤。
在证实累积的DNA损伤是驱动睡眠的因素后,研究人员渴望了解是否有可能确定斑马鱼需要睡眠的最短时间。他们发现,每晚6小时的睡眠足以减少DNA损伤。如果睡眠不足6小时,DNA损伤就不会充分减少,斑马鱼即使在白天也会继续睡眠。
接下来,研究人员需要弄清楚大脑中告诉我们需要睡眠以促进DNA修复的分子是什么?他们发现PARP1蛋白在其中至关重要。
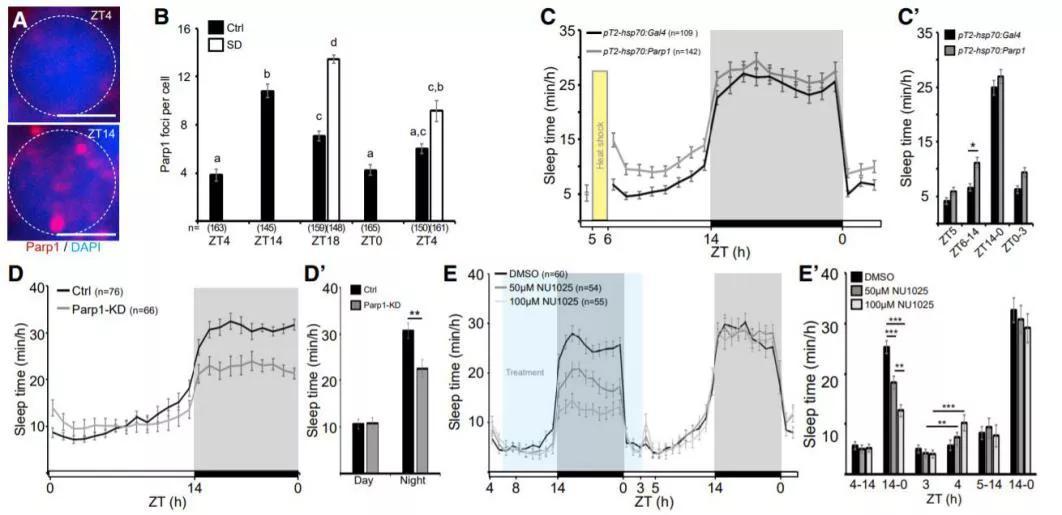
图源:doi: 10.1016/j.molcel.2021.10.026.
PARP1是DNA损伤修复系统的一部分,是最早做出反应的蛋白质之一。PARP1会标记细胞中的DNA损伤位点,并招募其他分子一起来修复DNA损伤。
通过分子生物学实验,研究人员发现增加PARP1不仅可以促进睡眠,还可以增加睡眠中DNA的修复。相反,减少PARP1会让斑马鱼意识不到自己需要睡觉,也没有发生DNA损伤修复。
进一步的研究使用脑电图在小鼠身上进行测试。就像斑马鱼一样,PARP1活性的抑制降低了非快速眼动睡眠的持续时间和质量。这说明PARP1能够告诉大脑它需要睡眠,否则它将面临危险。

图源:doi: 10.1016/j.molcel.2021.10.026.
文章的通讯作者表示,接下来的任务是研究PARP1感知损伤阈值的具体机制。他们的发现很可能可以用于解释睡眠障碍和神经退行性疾病之间的潜在联系。
而对我们来说,又多了一个上班打盹的借口了。辛勤工作的超人们,今晚还继续加班吗?
参考文献:
[1] David Zada, et al. Parp1 promotes sleep, which enhances DNA repair in neurons. Mol Cell. 2021 Nov 12;S1097-2765(21)00933-3. doi: 10.1016/j.molcel.2021.10.026.





 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国