帕金森病(PD)是一种常见的中老年神经系统退行性疾病。震颤、肌强直、动作迟缓、姿势平衡障碍的运动症状和睡眠障碍、嗅觉障碍、自主神经功能障碍、认知和精神障碍等非运动症状的临床表现为显著特征。我国65岁以上人群患病率为1.7%。随着疾病进展,PD的运动和非运动症状会逐渐加重,一方面损害患者的日常活动,另一方面,也带来巨大的社会和医疗负担。
*PD的治疗原则
一、综合治疗
每一位PD患者可以先后或同时表现有运动症状和非运动症状,但在整个病程中都会有这两类症状,有时会产生多种非运动症状。不仅运动症状会影响患者的工作能力和日常生活能力,非运动症状也会明显干扰患者的生活质量。因此,应对PD的运动症状和非运动症状采取全面综合治疗。
二、多学科治疗模式
PD治疗方法和手段包括药物治疗、手术治疗、肉毒毒素治疗、运动疗法、心理干预、照料护理等。药物治疗作为首选,且是整个治疗过程中的主要治疗手段,手术治疗则是药物治疗不佳时的有效补充手段,肉毒毒素注射是治疗局部痉挛和肌张力障碍的有效方法,运动与康复治疗、心理干预与照料护理则适用于PD治疗全程。在条件允许情况下,组建多学科团队,可以更有效地治疗和管理PD患者,为患者带来更大的益处。
三、全程管理
目前应用的治疗手段,无论药物或手术,只能改善症状,不能阻止病情的发展,更无法治愈。因此,治疗不仅立足当前,而且需长期管理,以达到长期获益。
*药物治疗
一PD的用药原则
疾病的运动和非运动症状会影响患者的工作和日常生活能力,用药原则以达到有效改善症状、避免或降低不良反应、提高工作能力和生活质量为目标。
提倡早诊断、早治疗,不仅可以更好地改善症状,而且能延缓疾病的进展。
坚持“剂量滴定”以避免产生药物急性不良反应,力求实现“尽可能以小剂量达到满意临床效果”的用药原则,可避免或降低运动并发症尤其是异动症的发生率。
治疗应遵循循证医学证据,也应强调个体化特点,不同患者的用药选择需要综合考虑患者的疾病特点和疾病严重度、发病年龄、就业状况、有无认知障碍、有无共病、药物可能的不良反应、患者的意愿、经济承受能力等因素。尽可能避免、推迟或减少药物的不良反应和运动并发症。
抗PD药物治疗时不能突然停药,特别是使用左旋多巴及大剂量多巴胺受体激动剂时,以免发生撤药恶性综合征。
二、早期PD的药物治疗
根据临床症状严重度的不同,将Hoehn-Yahr 分级1.0~2.5级定义为早期。疾病一旦发生将随时间推移而渐进性加重,有证据提示在疾病早期阶段的病程进展较后期阶段进展快。因此一旦早期诊断,即应开始早期治疗,争取掌握疾病修饰时机,对疾病治疗的长程管理有重要作用。
早期治疗可以分为非药物治疗(包括认识和了解疾病,补充营养、加强运动康复、坚定战胜疾病的信心,以及社会和家人对患者的理解、关心与支持)和药物治疗。一般开始多以单药治疗,但也可采用两种不同作用机制(针对多靶点)的药物小剂量联合应用,力求疗效最佳,维持时间更长,而急性不良反应和运动并发症发生率更低。
(一)早期PD的疾病修饰疗法
疾病修饰治疗的目的是既能延缓疾病的进展,又能改善患者的症状。
可能有疾病修饰作用的药物主要包括单胺氧化酶B型抑制剂(MAO-BI)和多巴胺受体激动剂(DAs)。MAO-BI中的雷沙吉兰和司来吉兰可能具有疾病修饰的作用;研究提示DAs中的罗匹尼罗可能有疾病修饰作用。
(二)早期PD的症状治疗
目前有多种可有效改善PD的药物。在选择药物时应以患者为中心,根据患者的年龄、症状表现、疾病严重程度、共患病、工作和生活环境等进行选择和调整。
1. 复方左旋多巴(多巴丝肼、卡比双多巴):左旋多巴是治疗PD的标准疗法,是PD药物治疗中最有效的对症治疗药物。随着疾病进展和左旋多巴长期使用会产生运动并发症,包括症状波动和异动症。
早期应用小剂量左旋多巴(400 mg/d以内)不增加异动症的产生;与左旋多巴的治疗时间相比,高剂量的左旋多巴和长病程对异动症的发生风险影响更大。
因此,早期并不建议刻意推迟使用左旋多巴,特别对于晚发型PD患者或者运动功能改善需求高的较年轻患者,复方左旋多巴可以作为首选,但应维持满足症状控制前提下尽可能低的有效剂量。
2. 多巴胺受体激动剂:主要推崇采用非麦角类,并作为早发型患者病程初期的首选药物,包括普拉克索、罗匹尼罗、吡贝地尔、罗替高汀和阿扑吗啡。需要指出的是多巴胺受体激动剂大多有嗜睡和精神不良反应发生的风险,需从小剂量滴定逐渐递增剂量。
在疾病早期左旋多巴和多巴胺受体激动剂均小剂量联合使用,充分利用两种药物的协同效应和延迟剂量依赖性不良反应,临床上现很常用,早期添加DAs可能推迟异动症的发生。
3. MAO-BI:包括第一代MAO-BI司来吉兰常释片和口崩片及第二代MAO-BI雷沙吉兰,以及双通道阻滞剂沙芬酰胺、唑尼沙胺。对PD的运动症状有改善,主要推荐用于治疗早期PD患者,特别是早发型或初治的PD患者,也用于进展期PD患者的添加治疗。
在改善运动并发症方面,雷沙吉兰相对于司来吉兰证据更充分。使用司来吉兰时勿在傍晚或晚上应用,以免引起失眠。
4. 儿茶酚-O-甲基转移酶抑制剂(COMTI):有恩他卡朋、托卡朋和奥匹卡朋及与复方左旋多巴组合的恩他卡朋双多巴片(为恩他卡朋/左旋多巴/卡比多巴复合制剂,按左旋多巴剂量不同分成4种剂型)。在疾病早期首选恩他卡朋双多巴片治疗可以改善症状,在疾病中晚期添加COMTI治疗可以进一步改善症状。
需指出的是恩他卡朋须与复方左旋多巴同服,单用无效,托卡朋每日首剂与复方左旋多巴同服,此后可以单用,一般每间隔6 h服用,但需严密监测肝功能。
5. 抗胆碱能药:苯海索,适用于有震颤的患者,对无震颤的患者不推荐应用。
对60岁以下的患者,需告知长期应用可能会导致认知功能下降,所以要定期筛查认知功能,一旦发现认知功能下降则应停用;对60岁以上的患者尽可能不用或少用;若必须应用则应控制剂量。
6.金刚烷胺:对少动、强直、震颤均有改善作用,对改善异动症有效。
*推荐意见:
(1)早发型PD,不伴智能减退,可有如下选择:①非麦角类DAs;②MAO-BI;③复方左旋多巴;④恩他卡朋双多巴片;⑤金刚烷胺;⑥抗胆碱能药。伴智能减退,应选择复方左旋多巴。首选药物并非按照以上顺序,需根据不同患者的具体情况,而选择不同方案。若顺应欧美治疗指南首选①方案,也可首选②方案,或可首选③方案;若因特殊工作之需,力求显著改善运动症状,则可首选③或④方案;也可小剂量应用①或②方案时,同时小剂量合用③方案;若考虑药物经济因素,对强直少动型患者可首选⑤方案,对震颤型患者也可首选⑥方案。
(2)晚发型PD,或伴智能减退的早发型患者:一般首选复方左旋多巴治疗。随症状加重、疗效减退时可添加DAs、MAO-BI或COMTI治疗。抗胆碱能药尽可能不用,尤其老年男性患者,因有较多不良反应。
图1是主要依据临床症状和不同年龄以及病情发展情况下推荐如何选择用药的详细流程图,以供参考。
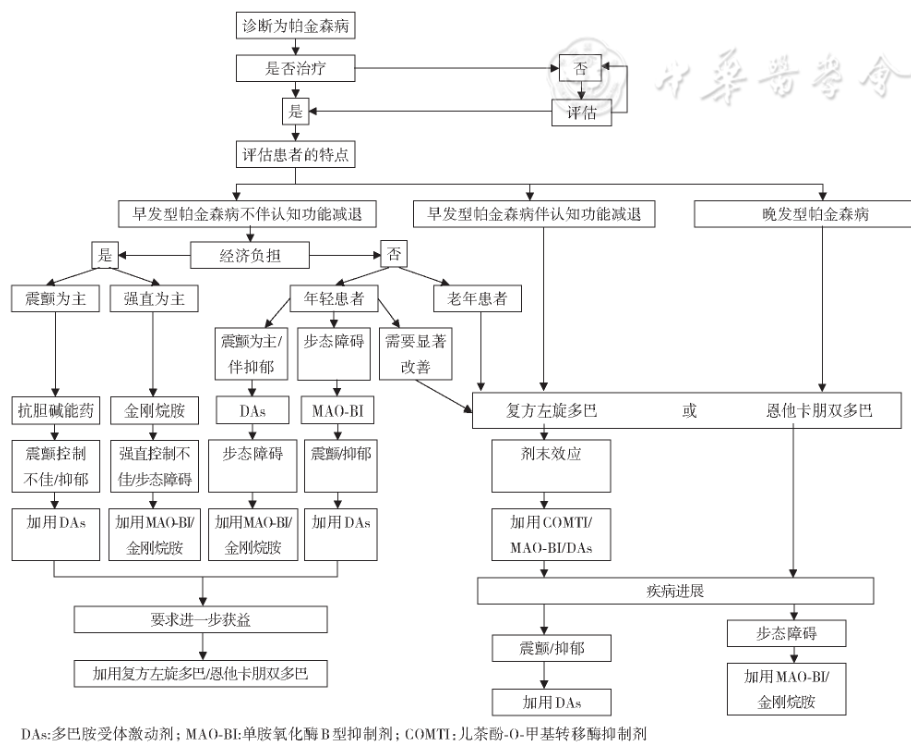
图1 帕金森病的药物治疗流程
三、中晚期PD的药物治疗
根据临床症状严重度的不同,将H-Y分级3~5级定义为中晚期PD,尤其是晚期PD的临床表现极其复杂,其中有疾病本身的进展,也有药物不良反应或运动并发症的因素参与。对中晚期PD患者的治疗,既要继续力求改善运动症状,又要妥善处理一些运动并发症和非运动症状。
(一)运动症状及姿势平衡障碍的治疗
疾病进入中晚期阶段,运动症状进一步加重,行动迟缓更加严重,日常生活能力明显降低,出现姿势平衡障碍、冻结步态,容易跌倒。力求改善上述症状则需增加在用药物的剂量或添加尚未使用的不同作用机制的抗PD药物,可以根据临床症状学(震颤还是强直少动为突出),以及对在用多种药物中哪一药物剂量相对偏低或治疗反应相对更敏感的药物而增加剂量或添加药物。
冻结步态是PD患者摔跤的最常见原因,易在变换体位如起身、开步和转身时发生,目前尚缺乏有效的治疗措施,调整药物剂量或添加药物偶尔奏效,部分患者对增加复方左旋多巴剂量或添加MAO-BI和金刚烷胺可能奏效。此外,适应性运动康复、暗示治疗,例如:步态和平衡训练、主动调整身体重心、踏步走、大步走、视觉提示(地面线条,规则图案或激光束)、听口令、听音乐或拍拍子行走或跨越物体(真实的或假想的)等可能有益。必要时使用助行器甚至轮椅,做好防护。随着人工智能技术的发展,智能穿戴设备以及虚拟现实技术在改善姿势平衡障碍、冻结步态方面带来益处.
(二)运动并发症的治疗
运动并发症(症状波动和异动症)是PD中晚期阶段的常见症状,严重影响患者的生活质量,给临床治疗带来较棘手的难题。通过提供持续性多巴胺能刺激(CDS)的药物或手段可以对运动并发症起到延缓和治疗的作用,调整服药次数、剂量或添加药物可能改善症状,以及手术治疗如脑深部电刺激(DBS)亦有效。
症状波动的治疗(图2):症状波动主要有剂末恶化、开-关现象等。
(1)剂末恶化的处理方法有:
①避免饮食(含蛋白质)对左旋多巴吸收及通过血脑屏障的影响,需在餐前1 h或餐后1.5 h服用复方左旋多巴,调整蛋白饮食可能有效。
②不增加服用复方左旋多巴的每日总剂量,而适当增加每日服药次数,减少每次服药剂量(以仍能有效改善运动症状为前提)。
③复方左旋多巴由常释剂换用缓释片以延长作用时间,更适宜在早期出现的剂末恶化,尤其发生在夜间时为较佳选择,但剂量需增加20%~30%。新型的左旋多巴/卡比多巴缓释胶囊可以快速到达并较长维持血药多巴浓度,减少给药次数,缩短“关”期,减少症状波动,因此左旋多巴/卡比多巴缓释胶囊对症状波动的治疗被评估为有效、临床有用。
④加用对纹状体产生CDS的长半衰期DAs。若已用DAs中的一种而出现不良反应或疗效减退可试换用另一种。
⑤加用对纹状体产生CDS的COMTI。
⑥加用MAO-BI。
⑦腺苷A2受体拮抗剂伊曲茶碱对症状波动的治疗被评估为可能有效,临床可能有用。
⑧双侧丘脑底核-DBS和苍白球内侧部(GPi)-DBS对症状波动的治疗均被评估为有效。单侧苍白球损毁术相对于单侧丘脑和丘脑底核损毁术以及单侧丘脑刺激术,对改善症状波动的证据更充分。
(2)开-关现象的处理方法有:
①选用长半衰期的非麦角类DAs,其中普拉克索、罗匹尼罗、罗替高汀证据较为充分。每日1次的DAs缓释片较常释片的血药浓度更平稳,可能改善“开-关”现象的作用更满意,以及依从性更高。如罗匹尼罗缓释片相对于常释片能够带来更长“关”期时间的减少。
②对于口服药物无法改善的严重“关期”患者,可考虑采用持续皮下注射阿扑吗啡或左旋多巴肠凝胶灌注。
③手术治疗(丘脑底核-DBS或GPi-DBS)。
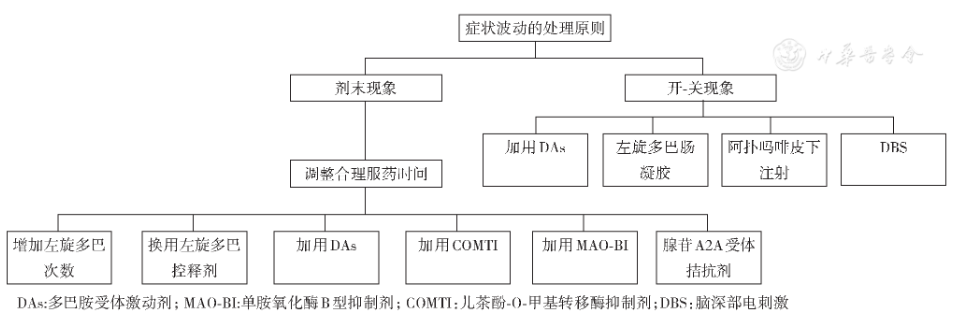
图2 帕金森病患者症状波动的处理原则
2.异动症的治疗(图3):异动症包括剂峰异动症、双相异动症和肌张力障碍。
(1)对剂峰异动症的处理方法为:
①减少每次复方左旋多巴的剂量,若伴有剂末现象可增加每日次数。
②若患者是单用复方左旋多巴,可适当减少剂量,同时加用DAs,或加用COMTI。
③加用金刚烷胺或金刚烷胺缓释片,后一剂型是目前唯一获批用于治疗左旋多巴相关的异动症口服药物。
④加用非经典型抗精神病药如氯氮平。
⑤若在使用复方左旋多巴缓释片,则应换用常释剂,避免缓释片的累积效应。
(2)对双相异动症(包括剂初异动症和剂末异动症)的处理方法为:a.若在使用复方左旋多巴缓释片应换用常释剂,最好换用水溶剂,可以有效缓解剂初异动症。b.加用长半衰期的DAs或加用延长左旋多巴血浆清除半衰期、增加曲线下面积(AUC)的COMTI,可以缓解剂末异动症,也可能有助于改善剂初异动症。
(3)肌张力障碍包括清晨肌张力障碍、关期肌张力障碍和开期肌张力障碍。
①对清晨肌张力障碍的处理方法为:a.睡前加用复方左旋多巴缓释片或DAs。b.也可在起床前服用复方左旋多巴水溶剂或常释剂。
②对“关”期肌张力障碍的处理方法为:a.增加复方左旋多巴的剂量或次数。b.加用DAs、COMTI或MAO-BI。
③对“开”期肌张力障碍的处理方法为:a.与剂峰异动症的处理方法基本相同。b.若调整药物治疗无效时,可在肌电图引导下行肉毒毒素注射治疗。
(4)药物难治性异动症的处理方法为:可以使用左旋多巴/卡比多巴肠凝胶制剂、丘脑底核-DBS和GPi-DBS手术治疗可获裨益,也可使用阿扑吗啡皮下注射。其他正在进行临床研究的治疗异动症的药物主要是作用于5-羟色胺能、谷氨酸能、γ-氨基丁酸能和去甲肾上腺素能等非多巴胺通路途径。

图3 帕金森病患者异动症的处理原则
四、非运动症状的治疗
PD的非运动症状涉及许多类型,主要包括睡眠障碍、感觉障碍、自主神经功能障碍和精神及认知障碍。非运动症状在整个PD的各个阶段都可能出现,某些非运动症状,如嗅觉减退、快速眼球运动期睡眠行为异常(RBD)、便秘和抑郁可以比运动症状出现得更早。非运动症状也可以随着运动波动而波动非运动症状严重影响患者的生活质量,因此在管理PD患者的运动症状的同时也需要管理患者的非运动症状。
(一)睡眠障碍的治疗
60%~90%的患者伴有睡眠障碍,睡眠障碍是最常见的非运动症状,也是常见PD夜间症状之一。
睡眠障碍主要包括失眠、RBD、白天过度嗜睡(EDS)和不宁腿综合征(RLS);约50%或以上的患者伴有RBD,伴RBD的处理首先是防护,发作频繁可在睡前给予氯硝西泮或褪黑素,氯硝西泮有增加跌倒风险,一般不作为首选。
失眠和睡眠片段化是最常见的睡眠障碍,首先要排除能影响夜间睡眠的抗PD药物,如司来吉兰和金刚烷胺都可能导致失眠,尤其在傍晚服用者,首先需纠正服药时间,司来吉兰需在早、中午服用,金刚烷胺需在下午4时前服用,若无改善,则需减量甚至停药。若与药物无关则多数与PD夜间运动症状有关,也可能是原发性疾病所致。
若与患者的夜间运动症状有关,主要是多巴胺能药物的夜间血药浓度过低,因此加用DAs(尤其是缓释片)、复方左旋多巴缓释片、COMTI能够改善患者的睡眠质量。若是EDS要考虑是否存在夜间的睡眠障碍,RBD、失眠患者常常合并EDS,此外也与抗帕金森病药物DAs或左旋多巴应用有关。
如果患者在每次服药后出现嗜睡,提示药物过量,适当减小剂量有助于改善EDS;如果不能改善,可以换用另一种DAs或者可将左旋多巴缓释片替代常释剂,可能得到改善;也可尝试使用司来吉兰。
对顽固性EDS患者可以使用精神兴奋剂莫达菲尼。帕金森病患者也常伴有RLS,治疗优先推荐DAs,在入睡前2 h内选用DAs如普拉克索、罗匹尼罗和罗替高汀治疗十分有效,或用复方左旋多巴也可奏效。
(二)感觉障碍的治疗
最常见的感觉障碍主要包括嗅觉减退、疼痛或麻木。90%以上的患者存在嗅觉减退,且多发生在运动症状之前多年,可是目前尚缺乏有效措施能够改善嗅觉障碍。
40%~85%的PD患者伴随疼痛,疼痛的临床表现和潜在病因各不相同,其中肌肉骨骼疼痛被认为是最常见的,疼痛可以是疾病本身引起,也可以是伴随骨关节病变所致。疼痛治疗的第一步是优化多巴胺能药物。特别是症状波动性的疼痛,如果抗PD药物治疗“开期”疼痛或麻木减轻或消失,“关”期复现,则提示由PD所致,可以调整多巴胺能药物治疗以延长“开”期,约30%患者经多巴胺能药物治疗后可缓解疼痛。反之则由其他共病或原因引起,可以予以相应的治疗,如非阿片类(多乙酰氨基酚和非甾体类抗炎药)和阿片类镇痛剂(羟考酮)、抗惊厥药(普瑞巴林和加巴喷丁)和抗抑郁药(度洛西汀)。
通常采用非阿片类和阿片类镇痛剂治疗肌肉骨骼疼痛,抗惊厥药和抗抑郁药治疗神经痛。
(三)自主神经功能障碍的治疗
最常见的自主神经功能障碍包括便秘、泌尿障碍和位置性低血压等。对于便秘,摄入足够的液体、水果、蔬菜、纤维素或其他温和的导泻药,如乳果糖、龙荟丸、大黄片等能改善便秘;也可加用胃蠕动药,如多潘立酮、莫沙必利等;增加运动。需停用抗胆碱能药。
对泌尿障碍中的尿频、尿急和急迫性尿失禁的治疗,可采用外周抗胆碱能药,如奥昔布宁、溴丙胺太林、托特罗定和莨菪碱等;
对逼尿肌无反射者则给予胆碱能制剂(但需慎用,因会加重PD的运动症状);若出现尿潴留,应采取间歇性清洁导尿,若由前列腺增生肥大引起,严重者必要时可行手术治疗。
位置性低血压患者应增加盐和水的摄入量;睡眠时抬高头位,不要平卧;可穿弹力裤;不要快速地从卧位或坐位起立;首选米多君治疗,且最有效;也可用屈昔多巴和多潘立酮。
(四)精神及认知障碍的治疗
最常见的精神及认知障碍包括抑郁和(或)焦虑、幻觉和妄想、冲动强迫行为和认知减退及痴呆。首先需要甄别可能是由抗PD药物诱发,还是由疾病本身导致。若是前者因素则需根据最易诱发的几率而依次逐减或停用如下抗PD药物:抗胆碱能药、金刚烷胺、MAO-BI、DAs;若仍有必要,最后减少复方左旋多巴剂量,但要警惕可能带来加重PD运动症状的后果。如果药物调整效果不理想,则提示可能是后者因素,就要考虑对症用药。
1. 抑郁、焦虑和淡漠:约35%的患者伴随抑郁,31%的患者伴随焦虑,其中抑郁伴焦虑的类型居多。抑郁可以表现为“关”期抑郁,也可与运动症状无明确相关性,治疗策略包括心理咨询、药物干预和重复经颅磁刺激(rTMS)。
当抑郁影响生活质量和日常生活时加用DAs、抗抑郁药物包括五羟色胺再摄取抑制剂(SSRIs)、五羟色胺去甲肾上腺素再摄取抑制剂(SNRIs)或三环类抗抑郁药(TCAs)。DAs类中的普拉克索和SNRIs药物文拉法辛证据较充分;TCAs药物中的去甲替林和地昔帕明改善抑郁症状证据其次,但存在胆碱能不良反应和心律失常的不良反应,不建议用于认知受损的老年患者。
需注意,SSRIs在某些患者中偶尔会加重运动症状;西酞普兰日剂量20 mg以上可能在老年人中引起长QT间歇,需慎用。
PD伴焦虑,常见的治疗方式包括抗抑郁药物、心理治疗等;
PD伴淡漠,DAs类药物吡贝地尔、胆碱酯酶抑制剂利伐斯的明可能有用。
2. 幻觉和妄想:PD的幻觉和妄想等发生率为13%~60%,其中视幻觉最常见。
首先要排除可能诱发精神症状的抗PD药物,尤其是抗胆碱能药、金刚烷胺和DAs。若排除药物诱发,可能是疾病本身导致,则给予对症治疗,推荐选用氯氮平或喹硫平,氯氮平会有1%~2%的几率导致粒细胞缺乏症,故需监测血细胞计数,因此临床常用喹硫平。
选择性5-羟色胺2A反向激动剂匹莫范色林,由于不加重运动症状,也用于治疗PD相关的精神症状。
其他抗精神病药由于可加重运动症状,不建议使用;
对于易激惹状态,劳拉西泮和地西泮很有效。
所有的精神类药物都不推荐用于伴随痴呆的PD患者。
3. 冲动强迫行为( ICBs):包括:冲动控制障碍(ICDs)、多巴胺失调综合征(DDS)和刻板行为。ICDs包括病理性赌博、强迫性购物、性欲亢进、强迫性进食等;DDS是一种与多巴胺能药物滥用或成隐有关的神经精神障碍,患者出现严重的但可耐受的异动症、“关”期的焦虑以及与多巴胺药物成瘾性相关的周期性情绪改变;刻板行为是一种重复、无目的、无意义的类似于强迫症的刻板运动行为,如漫无目的地开车或走路、反复打扫卫生或清理东西等,并且这种刻板行为通常与先前所从事的职业或爱好有关。
对ICDs的治疗可减少DAs的用量或停用,若DAs必须使用,则可尝试换用缓释剂型;托吡酯、唑尼沙胺、抗精神病药物(喹硫平、氯氮平),以及金刚烷胺治疗可能有效;阿片类拮抗剂(纳曲酮和纳美芬)治疗可能有用,但尚需进一步研究。认知行为疗法(CBT)也可以尝试。
对DDS的治疗可减少或停用多巴胺能药物可以改善症状,短期小剂量氯氮平和喹硫平可能对某些病例有帮助,持续的左旋多巴灌注和丘脑底核-DBS可以改善某些患者的症状。
严重的异动症和“关”期情绪问题,可通过皮下注射阿朴吗啡得到改善。
对刻板行为的治疗,减少或停用多巴胺能药物也许有效,但需平衡刻板行为的控制和运动症状的恶化;氯氮平和喹硫平、金刚烷胺及rTMS可改善症状,但需进一步验证。
以上3种ICBs的治疗尚缺乏有效的循证干预手段,临床处理比较棘手,因此重在预防。
4. 认知障碍和痴呆:25%~30%的PD患者伴有痴呆或认知障碍。临床上首先需排除可能影响认知的抗PD药物,如抗胆碱能药物苯海索。若排除了药物诱发因素后可应用胆碱酯酶抑制剂,利伐斯的明证据充分,临床有用;多奈哌齐和加兰他敏证据有限,临床可能有用。
*手术治疗
PD早期对药物治疗效果显著,但随着疾病的进展,药物疗效明显减退,或并发严重的症状波动或异动症时,可以考虑手术治疗。手术方法主要有神经核毁损术和DBS,DBS因其相对无创、安全和可调控性而成为目前的主要手术选择。
需强调的是,手术虽然可以明显改善运动症状,但并不能根治疾病;术后仍需应用药物治疗,但可减少剂量,同时需对患者进行优化程控,适时调整刺激参数。非原发性PD的帕金森叠加综合征患者对手术无效,是手术的禁忌证。
手术对肢体震颤和(或)肌强直有较好疗效,但对中轴症状如严重的语言吞咽障碍、步态平衡障碍疗效不显著,或无效,另外对一些非运动症状如认知障碍亦无明确疗效,甚至有可能恶化。
*康复与运动疗法
对PD运动和非运动症状改善乃至对延缓病程的进展都有帮助。PD患者多存在步态障碍、姿势平衡障碍、语言和(或)吞咽障碍等轴性症状,这些症状对于药物疗效甚微,但可以从康复和运动疗法中获益。因此,康复治疗建议应用于PD患者的全病程。
根据不同的行动障碍进行相应的康复或运动训练,如健走、太极拳、瑜伽、舞蹈、有氧运动、抗阻训练等。
有效的PD康复治疗包括:物理与运动治疗、作业治疗、言语和语言治疗以及吞咽治疗。需注意的是,在进行康复和运动治疗时,安全性是第一位。
需要针对不同的患者特点制定个体化和适应性康复和运动训练计划;同时需要确保长期依从性,若能每日坚持,则有助于提高患者的生活自理能力,改善运动功能,并能延长药物的有效期。
*心理干预
心理干预,特别是认知训练、CBT提供了一种可行的非药物治疗方案。对PD患者的神经-精神症状应予有效的心理干预治疗,与药物应用并重,以减轻身体症状,改善心理精神状态,达到更好的治疗效果。
*照料护理:科学护理对维持患者生活质量十分重要。
科学的护理能对有效控制病情和改善症状起到一定的辅助治疗作用;同时更能够有效地防止误吸或跌倒等可能意外事件的发生。
针对运动症状和非运动症状进行综合护理,包括药物护理、饮食护理、心理护理及康复训练。向患者普及药物的用法和注意事项等从而有利于规范药物使用,避免药物不良反应的发生;定制针对性饮食方案改善患者营养状况和便秘等症状;及时评估患者的心理状态,予以积极引导,调节患者的负面情绪,提高患者生活质量,与家属配合,督促患者进行康复训练,以维持患者良好的运动功能,提高患者的自理能力。
*人工智能及移动技术
一、远程医疗:就诊更方便,从而增加医患间的互动频率,有助于医生全面评估病情从而指导治疗。
二、可穿戴设备:一方面能够对症状进行客观评估与监测,有助于病情的准确评估和个体化方案的制定;另一方面可作为辅助治疗手段改善患者的生活质量,如防抖勺辅助进食,视/听觉提示改善冻结步态等。
三、智能手机应用:有利于患者信息的收集,病情评估以及患者教育。
四、虚拟现实技术,可用于康复训练。







 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国