活化-钝化腐蚀是一种阳极钝化过程,阳极钝化是作为阳极的金属或化合物在电流作用下,不同程度地失去转入溶液的能力。一般认为阳极钝化是阳极表面生成一层致密的氧化物(或其他化合物)薄膜,这层薄膜覆盖着金属,隔离了阳极与溶液,阻碍了金属的继续氧化溶解,但它仍具有导电作用。
阳极钝化简介在阳极溶解过程中,电极电位愈正,金属的溶解速率愈大。但电位增至一定值后,溶解速率减小,即电极电流密度超过某一临界值,便出现电极电位的突跃,这种现象称为阳极钝化。硬质合金废料电解过程,由于电流密度超过某一临界值,电流会消耗在进行某些新的电极过程,如O2、Cl2的析出,使硬质合金中的钴溶解过程减慢,甚至停止溶解,出现钝化。产生钝化原因可能在合金表面上有新的成相层,如氧化物薄膜或某些金属盐的固相薄膜,它使金属面与溶液机械隔开而使合金钝化;或在合金表面或部分表面上生成氧或含氧粒子的吸附层,大大降低电化学反应的速度。要使钝化的硬质合金活化,就要创造破坏钝化层的条件。加入某些活性离子、改变溶液的pH值、控制好电化学溶解工艺条件等,避免阳极析出O2和Cl2而使合金氧化。
在电解过程中,电解速度不仅与废硬质合金牌号有关,还与废硬质合金装料松紧程度、阳极接触面积及电解质导电性有关。为提高电解速度,在装料时,要细心的将其紧密接触,电解过程中还要经常用一塑料棒捣实,增加导电性,提高电流密度。为增大阳极接触面积,采用经常清筐,使电解过程中破裂下来的WC片及时去除,避免影响导电性1。
活化-钝化腐蚀过程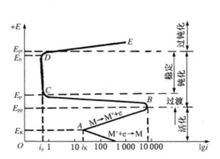
如图为活化一钝化金属如铁、铬、镍及其合金在一定介质中采用恒电位法测得的典型阳极极化曲线示意图。它标志了金属活化、钝化的各特性点和特性区。由图可知,从金属的腐蚀电位E起,随着电位增加,电流迅速增大,在B点达到最大值。电位继续升高,电流密度却开始大幅度下降,到达C点后电流密度保持一个很小的数值,已不再随电位变化而变化。起过D点,电位增大,电流密度又开始上升。
可将此典型阳极极化曲线划分为几个不同的区域:
AB段:金属的活性溶解区。在这个电位区间,金属进行正常的阳极溶解,溶解速度按塔菲尔规律增长,这一段极化曲线很平坦,表示阳极过程很少受阻碍。
BC段::金属的活化-饨化过渡区。当电位达到某一临界值(B点),可得致饨电流密度(ipp)和致钝电位(Epp)。在这个电位区间,金属表面状态发生急剧变化并处于不稳定状态,可能生成二价到三价的过渡氧化物。随着电位升高,阳极溶解电流密度显著下降。到达C点后,金属转入完全钝态,电流密度变得很小。
CD段:金属的钝化区。CD段的电流密度只有微小的变化或几乎不变,这一微小的电流密度称为维钝电流密度(ip)。C点的电位是维持金属钝态所必须的电位,称为维钝电位(Ep)。在这个电位区间金属处于钝化状态,金属表面已生成较高价的稳定氧化物膜。但是,钝化膜在介质作用下还是会在其薄弱地区发生轻微溶解而引起局部坏。维钝电流密度正是通过金属的少量溶解生成相应的氧化物来修补破坏了的钝化膜,维钝电流密度愈小,金属在钝态下的腐蚀速率也愈低。
CE段:金属的过钝化区。过D点以后,阳极极化电位继续增高,电流密度开始增大。D点的电位称为过钝化电位。在这个电位区间发生了某种新的阳极反应或者是原来的钝化膜进一步氧化后变得不耐腐蚀了,即金属阳极溶解生成了高价的可溶性离子2。
本词条内容贡献者为:
黎明 - 副教授 - 西南大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国