克劳修斯-克拉佩龙方程(英语:Clausius–Clapeyron relation)是用于描述单组分系统在相平衡时压强随温度的变化率的方法,以鲁道夫·克劳修斯和埃米尔·克拉佩龙命名。
简介克劳修斯-克拉佩龙方程(英语:Clausius–Clapeyron relation)是用于描述单组分系统在相平衡时压强随温度的变化率的方法,以鲁道夫·克劳修斯和埃米尔·克拉佩龙命名。
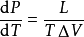 此处
此处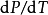 是压强随温度的变化率,L是相变焓(早年称为潜热),T是相平衡温度,
是压强随温度的变化率,L是相变焓(早年称为潜热),T是相平衡温度,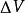 是相变过程中的比容变化。1
是相变过程中的比容变化。1
相变相变(英语:Phase Change)是指物质在外部参数(如:温度、压力、磁场等等)连续变化之下,从一种相(态)忽然变成另一种相,最常见的是冰变成水和水变成蒸气。然而,除了物体的三相变化(固态、液态、气态)自然界还存在许许多多的相变现象,例如日常生活中另一种较常见的相变是加热一块磁铁,磁铁的铁磁性忽然消失。其他在物理学中重要相变列举如下:
物质从金属变成超导体的超导相变
液态氦从正常液体变成超流体的λ相变
磁铁在居里温度从铁磁性变成顺磁性
金属-绝缘体相变
量子相变1
焓焓(英语:enthalpy,读音ㄏㄢˊ|hán)是一个热力学系统中的能量参数。规定由字母H表示(H来自于英语Heat Capacity(热容)一词),单位为焦耳(J)。此外在化学和技术文献中,摩尔焓Hm(单位:千焦/摩尔,kJ/mol)和质量焓(或比焓)h(单位:千焦/千克,kJ/kg)也非常重要,它们分别描述了焓在单位物质的量和单位质量上的定义。
焓是内能和体积的勒让德变换。它是SpN总合的热势能。1
参见范特霍夫方程
安托万方程
本词条内容贡献者为:
胡建平 - 副教授 - 西北工业大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国