具有多型性的金属,当温度变化(加热或冷却)时,它由一种晶体结构向另一种晶体结构的转变过程,叫作金属的多型性转变或同素异型转变。这个发生转变的温度,称为转变的临界点。金属及合金在固体状态下因发生相变而引起的组织变化称为重结晶。
简介多型性转变(allotropic transformation)又称同素异构转变、同素异晶转变或同位异构转变。指一种元素或化合物随温度和压力的不同而发生的结构类型转变。当发生多型性转变时,由于不同晶体结构的致密度和配位数等不同,将伴随有体积变化和电阻、热膨胀系数等物理参量的突变。多型性转变所对应的温度点称为临界点。与液体结晶相类似,新的结构类型的形成也是以形核和长大的方式进行。
固态中的多型性转变具有较大的过冷倾向。最常见的是铁的多型性转变。在912℃由α-Fe(bcc)转变为γ-Fe(fcc),而在1394℃则由γ-Fe转变为δ-Fe(bcc)。除铁外,如Mn、Ti、Sn、C、Ca、Ce、Pr等也具有多型性转变的特征。另外,一些化合物如SiO2、BN、TiO2、NaBa2Nb5O15(BNN)等也具有该特征。通常,具有同素异构特性的元素,在低温态大多具有密排结构(hcp或fcc),而在高温态则大多具有bcc结构,只有少数情况例外,如Sn等。固态下元素所表现的多型性,主要与该类原子的电子层结构的变化有关。即在不同温度或压力下,通过参与键合的外层电子分布状态的改变,而引起原子间结合能以致点阵形式发生改变。多型性转变是金属材料热处理的依据之一。1
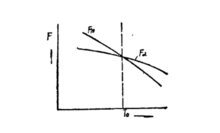
热力学条件及机理(一)多型性的金属或合金,若具有两种晶体结构,则它们在不同温度下的自由能曲线,如图所示。
从图中可以看出,当温度低于T0时,α相的自由能Fα低于β相的自由能Fβ,此时α相是稳定的。因此β相要向α相转变,即β→α。当温度高于T0时,β相的自由能Fβ小于Fα,β相是稳定的。因此α相有可能向β相转变,即α→β。当温度正好为T0时,Fα=Fβ,α和β两相处于平衡,即α←→β。T0是标志着一个相态转变为另一个相态的温度,因此称它为相变温度(或转变温度),又叫作临界点。
β→α或α→β的多型性转变,正如金属的结晶一样,也是通过形核和核长大的步骤来进行的。新相的核心主要产生在母相的晶界上。这是因为晶界层原子排列较乱,结构比较疏松,便于原子的重新排列。同时,晶界层的原子具有较高的自由能,为形成新的相界面提供了必须的条件。
不仅旧相晶界对新相的形核起很大作用,高熔点的杂质质点也能起相似的作用。
新相晶核形成后,其长大则根据过冷度的大小不同,可能沿两种途径进行。当过冷度较小时,长大是靠原子从旧相扩散转移来进行的。这种扩散转移所需的激活能很大,温度不高时,相界面上只有一部分原子能借热振动获得这种为转移所必须的能量起伏。因此靠这种情况来进行转变,速度是非常缓慢的,这就叫作扩散型的转变。当过冷度很大时,在某些金属和合金中,晶核是共格式的长大,原子的移位及其激活能都很小,因此晶格的改组或重新排列的过程,甚至可以在极低的温度下也能很快进行,因此称这种转变为共格型转变。2
(二)多型性金属具有三种或更多种晶体结构时,则转变较为复杂。下图表示金属或合金的三种不同晶体结构(α、β、γ)自由能与温度的关系曲线。
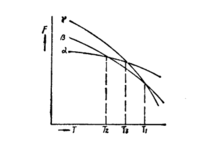
图的T1、T2各相当于β和γ、α和β的平衡温度或转变温度。在T1以上,γ相的自由能Fγ最低,因此γ相是热力学稳定的。若使温度过冷到T1与Ts的温度之间,在热力学上仅能生成β晶体,直至γ相完全转变为β相才结束。T2温度以下,α相的自由能Fα最低,最稳定,β相就要转变为α相。假若原γ相,过冷到Ts温度以下,则由于α和β相在此温度时均较γ相具有较低的自由能,因此α及β两个低温相都有可能析出。在Ts与T2温度之间,γ→β的转变,较之γ→α会引起自由能更大的降低。因此从热力学上看,γ→β的转变应该进行。但是,由于γ→α的转变可能在动力学上比较有利(α和γ的晶格类型有较大的相似性),因此α相形核的几率和生长速度可能要高于β相。在这样的过冷度情况下,α和β二相同时形核和长大也是可能的。
若快速冷却,γ相也能过冷到T2温度以下,此时在γ相中,α及β相都可能形核和长大。生成的α和β相的数量决定于它们形核,长大的动力学条件(成分起伏、结构起伏等)。
在所有这些情况下,转变可以通过原子的扩散来实现,也可以通过共格型或切变型来实现。生成的组织可以是单相的、两相的或三相的。而各相的状态可以是稳定的,或者是亚稳定的。2
同素异构和多型性转变很多材料在特定温度和压力下会发生晶体结构的转变,元素的这种行为称为同素异构转变。化合物的这种行为称为多型性转变。如纯铁在912℃以下是具有BCC结构的α-Fe,在912~1394℃之间则变为FCC结构的γ-Fe,而在1394℃~熔点(1540℃)之间又变为BCC结构的δ-Fe。α-Fe、γ-Fe、δ-Fe都是铁的同素异构体。
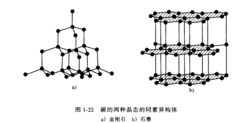
另一个同素异构体材料是碳。如下图所示,它可以以金刚石或石墨的晶态存在。金刚石具有配位数(CN)等于4的共价键四面体三维网络结构。三维共价网络中异常高的键合强度,使得金刚石的熔点和硬度比任何其他元素的都高。相反,碳在室温下热力学有利的形式是石墨,它具有六边形二维层状结构。在这种结构中层面上的碳原子仅有3个最近邻,其间构成共价键;但层与层之间是结合力比较弱的二次键,二次键比较容易断开使得石墨具有优越的润滑性。
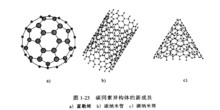
近年来,在碳的同素异构体中又不断出现新的成员。下图分别表示富勒烯、碳纳米管和碳纳米筒的结构。富勒烯是1985年发现的团簇状新材料(克劳托等人因这一发现,得到了1996年的诺贝尔化学奖)。被称为C60的富勒烯是由60个碳原子组成,其结构类似于一个足球的球状中空结构(直径约为0.7nm)。碳纳米管是与富勒烯结构非常相似、非球状且沿一个方向延伸的针状结晶。由于针状结晶是中空的,因此称为纳米管。对其中塞满微细针状结晶的称为纳米导线。纳米管和纳米导线直径约为1nm到数十纳米,长度为几微米大小。纳米筒的形状类似于盛冰淇淋的圆锥筒,其端部细而尖。此外,纳米片、纳米带是厚度在几纳米的微细薄膜状材料。
除Fe、C外,如Mn、Ti、Sn、Ca、Ce、Pr等也具有同素异构转变的特征。通常,具有同素异构特性的元素在低温态大多具有密排结构(HCP或FCC),而在高温态则大多具有BCC结构,只有少数情况例外,如Sn等。固态下元素所表现的同素异构性,主要与该类原子的电子层结构的变化有关。即在不同温度或压力下,通过参与键合的外层电子分布状态的改变,而引起原子间结合能以致点阵形式发生改变。3
当发生同素异构和多型性转变时,由于不同晶体结构的致密度和配位数等不同,将伴随有体积变化和电阻、热膨胀系数等物理参量的突变。同素异构和多型性转变所对应的温度点称为临界点。与液体结晶相类似,新的结构类型的形成也是以形核和长大的方式进行。固态中的多型性转变具有较大的过冷倾向。
很多陶瓷材料,如二氧化硅(SiO2)、氧化铝(Al2O3)和氧化钛(TiO2)随温度改变会发生几种晶体结构的改变,其性能伴随结构改变而变化。例如,体积变化而引起密度可能增加或减少。很多陶瓷材料不能经受这种体积变化所产生的内应力,这些材料在转变温度下失效,如氧化锆(ZrO2)就是一个例子。正方系的氧化锆(冷却)在约1000℃时多型性转变为单斜系氧化锆,伴随着体积变化可使材料断裂。
同素异构和多型性转变是金属材料热处理的依据之一,也是制备新材料、控制陶瓷材料性能必须要考虑的因素之一。3
铁的多型性转变在压力变化的条件下,固态铁可呈三种不同的晶体结构:
1.体心立方晶格的铁,α-Fe;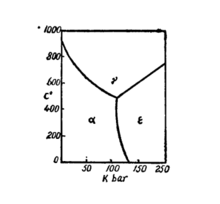
2.面心立方晶格的铁,γ-Fe,
3.密排六角晶格的铁,δ-Fe(如下图)。
在常压下,铁只呈现两种不同的晶体结构,即α-Fe和γ-Fe。
纯金属的多型性转变(又叫同素异型转变)只是一种有晶体结构的变化而无成分变化的相变。根据金属的纯度不同,旧相的晶粒大小以及冷却速度的不同,铁的多型性转变可能以下面三种方式进行。
1.形核,长大的方式进行
在常压和极缓慢的冷却速度条件下,γ-Fe→α-Fe的转变温度接近910℃。在这种条件下,α-Fe通过扩散型的转变方式(形核,长大都需要Fe原子作长距离的扩散)进行。
2.块形转变方式进行
若冷却速度在5000~30000℃/s之间时,则γ-Fe→α-Fe以块形转变的方式进行。块形转变形成的α-Fe,如下图所示。

块形转变时,γ-Fe与α-Fe的相界面不共格,但具有高的界面能,γ-Fe的原子仅跳动几次便转移到α-Fe,不需长距离的扩散,相界面的移动是非常迅速的。虽然如此,但仍然是通过形核、长大的步骤进行,只不过这两个步骤不太明显而已。
块形转变必须造成一定大的过冷度才能实现,铁发生这种转变是在750℃,过冷度约为170℃。因为只有在足够的过冷度条件下,才能提供不共格介面的能量,同时,也只有这样才能抑制住在此相变前不发生其它扩散型的相变。
3.马氏体型或切变型方式进行
若冷却速度再增加, 如达到40000~50000℃/s,γ-Fe以马氏体型相变生成α-Fe,α-Fe呈针状形态,表面发生了倾动或折绉。这种转变所需要的冷却速度与铁的纯度有关,纯度越高,所需的过冷度越大,纯度越低,则所需的过冷度越小。2
本词条内容贡献者为:
李航 - 副教授 - 西南大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国