Eschemoser亚甲基化反应,利用Eschenmoser盐引入亚甲基的方法。
作为一种典型的预制亲电试剂,Eschenmoser盐在有机合成中有着广泛的应用。自从1971年被研制出来,Eschenmoser盐已有了广泛的应用。
简介Eschenmoser 盐有着广泛的应用。更确切地说,该反应由价格低廉的原料出发,以一种较为经济的方式得到合成药物和天然产品所必需的结构单元。从收率和资源来看,该法是非常有效的。同时,由于Mannich 反应条件的兼容性,许多多步反应(Domino 反应)有可能以一锅法的方式完成,这也大大提高了该法的应用价值。除了经济价值以外,许多研究结果也证明,采用Eschenmoser盐进行Mannich 反应也能够满足现代化学选择性(化学、位置和空间)的要求。除了本文讨论的Eschenmoser盐,还有许多类似的胺甲基化或胺烷基化试剂被不断研制出来,这些试剂较强的亲电性质使得它们非常容易与几乎所有的亲核试剂起反应。这些新型的预制亲电胺烷基化试剂和Eschenmoser 盐一起必将大大拓展Mannich反应的在有机合成化学中的应用。123
Eschenmoser 盐和羰基化合物的反应Eschenmoser盐和含有α-碳原子的羰基化合物如醛和酮可在温和的条件下反应,生成相应的Mannich碱。所得到的Mannich 碱很容易脱去氨甲基得到亚甲基衍生物。实际上,这类反应是Eschenmoser 盐应用最为广泛的领域。
1、Eschenmoser 盐和醛的反应
为了通过合成确认 T. marginata(一种巴西肉食性昆虫)性信息素的三环倍半萜烯骨架结构,Kuwahara等采用Eschenmoser 盐合成了α, β-不饱和醛,进而合成了重要的碘化物合成片段,最终合成了该性信息素,确证了其结构。
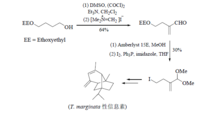
2、Eschenmoser盐和酮的反应
Kündig 等通过路易斯酸Cr(CO)3活化芳烃双键,结合闭环方法,方便地合成了二环[4.3.0]、[4.4.0]、[4.5.0]和[4.6.0]衍生物。Eschenmoser盐被用来增加一个亚甲基,合成二环[4.4.0]衍生物。
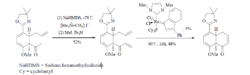
3、Eschenmoser 盐和酰胺的反应
α, β-二脱氢氨基酸(DDAAs)是一类构象限制的非蛋白质源氨基酸。它们能够被用来合成具有生物活性的环状氨基酸,如1-氨基环丙烷羧酸。Abellan从N-Boc(t-丁氧荃羰基)保护的吡嗪-2-酮(1)出发,合成了DDAA衍生物2,并由2经几步反应最终制得了二环α-氨基酸3。
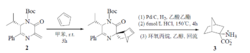
4、Eschenmoser 盐和酯的反应
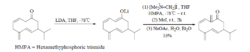
Marcos等利用Eschenmoser 盐在内酯的α位碳原子上引进一个亚甲基,最终得到了合成生长调节素(+)-Dihydroampullicin 的重要前体物质。32

Eschenmoser 盐和烯醇化合物的反应虽然烯醇化合物从本质上可以看作与羰基化合物相同,但是作为一种羰基化合物的活性变种,它能够对反应的位置和空间选择性的提高起到重要作用。实际上,目前大多数的此类反应都采用烯醇化合物的形式,所以在本文中将其另辟一节加以阐述。
1、Eschenmoser 盐和金属烯醇化合物的反应
Ivkovic利用预先制备的金属锂烯醇化合物与Eschenmoser 盐反应,完成了PeriplanetaAmericana 化学信息素Periplanone C的全合成。
2、Eschenmoser 盐和硅烷基烯醇醚化合物的反应
硅烷基烯醇醚类化合物比其相应的金属烯醇化合物具有更为出众的亲核性能,这使得它们能够在较为温和的反应条件下发生Mannich 反应。由于硅烷基化合物的种类较多,其体积大小也可较为容易的控制,这种方法在β-氨基羰基化合物的合成中能够有效提高产物的空间选择性。从另一方面来说,也可以选择性地将化合物的某个羰基转变为其相应的硅烷基烯醇醚,从而在Mannich反应的进行中控制反应进行的位置。基于以上的优点,目前很大一部分的Mannich反应都采用硅烷基烯醇醚这一活性中间体进行。
由于樟脑酮化合物的空间位阻原因,一般的Mannich反应条件下较易生成空间位阻小的内向型产物。McClure 等将樟脑酮化合物转变为三甲基硅烯醇醚,然后与Eschenmoser盐反应,以较高的空间选择性(86%)得到了外向型氨甲基化产物,其内向型产物含量不超过3%。4

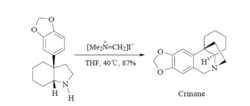
Eschenmoser 盐和芳香化合物的反应Eschenmoser盐也可以和富电子的芳香化合物如苯酚类、烷氧基苯类、吲哚类、吡咯类等化合物起反应。Padwa采用Eschenmoser盐和芳基六氢吲哚啉酮反应,六氢吲哚啉上氮原子迅速亲核取代所得Mannich碱的氨甲基,从而成环合成了优良的戒毒药物Crinane。从反应的实际结果来看,Eschenmoser 盐主要在烷氧基对位进行反应,位置选择性较好。4
本词条内容贡献者为:
王宁 - 副教授 - 西南大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国