丙二酸酯或乙酰乙酸酯的活性亚甲基,在比较弱的碱性条件下也容易被拔去氢。利用这个首先进行烷基化后再脱碳酸,前者可以得到取代的酮,后者可以得到取代的酯产物。
反应机理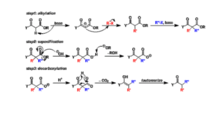
β-酮酯的亚甲基酸性比较大,优先和一个当量的碱反应,生成碳负离子。然后,碳负离子和烷基化试剂RX发生SN2反应,生成亚甲基上有取代基R的产物。如果重复这个过程,再加入一当量的碱和烷基化试剂R'X,可以得到亚甲基上有R和R'的产物。
β-酮酯可以在碱存在下发生水解反应,然后在酸环境并且加热的条件下可以脱掉羧基,而得到羰基化合物。如下所示:
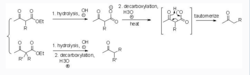
一般来说甲基上的氢酸性比亚甲基上的氢酸性强,但是对于β-酮酯的亚甲基上的氢来说酸性要比羰基的α-甲基上的氢的酸性大的多。所以,亚甲基优先和碱反应生成共轭的enolate,另一当量的碱会拔掉临近β-酮羰基的甲基上的氢,形成一个碳负离子。这碳负离子不稳定,活性强会迅速和烷基化试剂反应生成γ-取代的β-酮酯。1
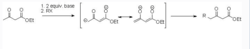
反应实例脱碳酸的时候不想用酸/碱条件的话,可以用甲基酯的Krapcho法。
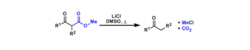
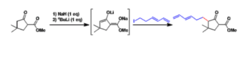
对于β-酮羰基化合物来说,用2当量以上的强碱作用的话,通常会引起不同位置的烷基化。这种带有两个阴离子的化合物,通常即使在反应性比较低的位置同样也能发生烷基化反应。1
本词条内容贡献者为:
陈红 - 副教授 - 西南大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国