二元系统相图是系统内二种组分之间相互作用的性质决定。三元系统内三种组分之间,相互作用的本质也与二元系统类似。但由于组分增加,情况更为复杂。
三元系统组成的表示方法三元凝聚系统:f=c-p+1=4-p,当 p=1 时,fmax=3(即组成x1、x2和温度的变化。
在三元系统中用等边三角形来表示组成。顶点:单元系统或纯组分;边: 二元系统;内部:三元系统。
应用:1、已知组成点确定各物质的含量;2、已知含量确定其组成点的物质。1
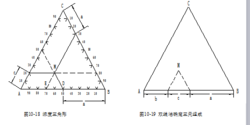
浓度三角形的几个重要定则1、截线规则:
以组分对边平行线在组分座标上的截距表示该组分的浓度(组分座标按逆时针增加法确定)
2、双线规则:
过组成点作任意两条平行于三角形两边的直线与第三边相交,并将第三边分为三段,此三段长度与组分对应含量成正比(中段为对角组分,边沿为不相邻组分)。组成点越靠近某角顶,该角顶组分含量越高。
3、等含量规则
在三角形中,平行于底边的直线上的所有的点都含有等量的对应顶点组元 。
4、定比例规则
在浓度三角形中,顶点与对应边上任意一点的联线上所有点,表明其余两个顶点组元的含量比例保持一定。
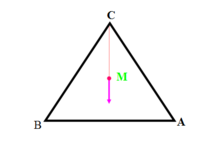
5、背向线规则
如果物质M中析出纯组元C,那么组成点M将沿MC连线并背离顶点C的方向移动。
6、杠杆规则
同样适用于三元系统相平衡(仅适用于两相平衡共存时)。
包括以下含义:
两相合成一新相时,新相组成点必在原来两相组成点连线上;
新相组成点与原来两相组成点的距离和两相的量成反比;
由一相分解为两相时,新两相的组成点必分布于原来相点的两侧,且三点必成一直线。
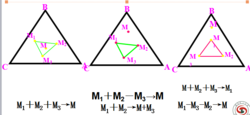
7、重心规则
在三元系统中,若有三种物质M1、M2、M3合成混合物M,则混合物M的组成点在连成的△M1M2M3之内,M点的位置称为重心位置。当一种物质分解成三种物质 ,则混合物组成点也在三物质组成点所围的三角形内。
8、交叉位置关系
新组成点与某一物质组成点联线若与另两物质组成点联线相交,则称新物质与与该物质成交叉位置关系。
9、交叉位置规则
三种旧物质合为一种新物质,且新物质组成点在三角形M1M2M3之外并与M3成交叉位置关系时,在M生成的同时必须从M1+M2中取出相当数量的M3,即M与M3同时生成 。
10、共轭位置关系
新组成点与某一物质组成点联线的延长线若与另两物质组成点联线相交,则称新物质与与该物质成共轭位置关系。
11、共轭位置规则
三种旧物质合为一种新物质,且新物质的组成点在三角形M1M2M3之外,并与M1成共轭位置关系时,在M生成的同时必须从M1中取出相当数量的M2+M3 。
三元系统中最大平衡相数为4,4个平衡相相点的相对位置可能有三种配置关系:1
简单三元系统的立体状态图和平面投影图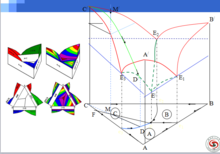
说明1、三棱边:A、B、C的三个一元系统;
2、三侧面:构成三个简单二元系统状态图,并具有相应的二元 低共熔点;
3、二元系统的液相线在三元系统中发展为液相面, 液相面代表了一种二相平衡状态,三个液相面以上的空间为熔体的单相 区;
4、液相面相交成界线,界线代表了系统的三相平衡状态,f=1;
5、三个液相面和三条界线在空间交于E/点,处于四相平衡状态,f=0;1
立体图与平面投影图的关系(1)冷却过程温度降低的方向
(2)等温线: 在空间结构图的液相面上,高度不同, 温度也不同,而液相面投影到ABC上是一个没有高低差别的平面,因而引入等温线。相图中一般注明等温线的温度。
结论:三角形顶点温度最高, 离顶点愈远其表示 温度愈低。等温线愈密,表示液相面越陡峭。
牢记:按杠杆规则,原始配料组成、液相组成和固相组成,这三点任何时刻必须处于一条直线上。并可计算某一温度下系统中的液相量和固相量。1
三元系统相图的基本类型1、具有一个低共熔点的三元系统相图
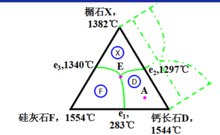
特点:三元组分各自在液态时完全互溶,而在固态时完全不互溶,不形成固溶体,也不形成化合物。只具有一个三元低共熔点。2
2、生成一个一致熔融二元化合物的三元系统相图
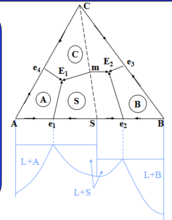
在相图上的特点:其组成点位于其初晶区范围内。
要求:
(1)确定温度的变化方向;
(2)各界线的性质;
(3)会划分各分三元系统;
(4)分析不同组成点的析晶路程,析 晶终点和析晶终产物;
(5)在E1E2界线上m点是温度最高点。(连线规则)
m点:
CS连线上的温度最低点,C-S系统的低共熔点;E1E2界线上的温度最高点。称:马鞍点。
重要的规则——副三角形的划分
副三角形——指与该无变量点液相平衡的三个晶相组成点连接成的三角形。
副三角形化的原则是要划分出具有可操作的副三角形,即画出的副三角形应有与其相对应的三元无变量点。
① 根据三元无变量点划分,因为除多晶转变和过渡点外,每个三元无变量点都有自己所对应的三角形,将与无变量点周围三个初晶区相应的晶相组成点连接起来即可。
② 把相邻两个初晶区所对应的相组成连起来,不相邻的不要连,这样就可划分出副三角形。
注意:与副三角形相对应的无变量点可以再该三角形内,亦可以在该三角形外,后者出现在不一致熔融化合物低的系统中。
3 具有不一致熔融二元化合物的三元系统
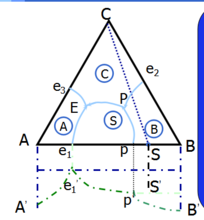
化合物组成点S不在其初晶区内。
S不稳定高温分解。连线CS不代表真正二元系统,不能将系统分为二个分三元系统。
P点与E点不同,是个转熔点:LP+B=C+S
分析:1点在S的初晶区内,开始析出晶相为S,组成点在△ASC内,析晶终点为E点,析出晶相为A、S、C;
2点在B的初晶区,开始析出的晶相为B,组成点在△BSC内,析晶终点为P点,析出晶相为B、S、C。
3点在C的初晶区内,开始析出的晶相为C,在△ASC内,析晶终点在E点,结晶终产物是A、S、C。途中经过P点,P点是转熔点,同时也是过渡点。2
4、生成一个固相分解的二元化合物的三元系统
1)形成高温分解低温稳定存在的二元化合物的三元相图
特点:三个无变量点,但只能划分两个副三角形,即可能的析晶终点是P点或E点。
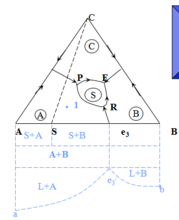
2)生成一个一致熔融三元化合物S
化合物组成点S在三元化合物初晶区内。
S:三元稳定化合物三个分三元系统2
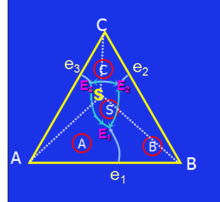
分析相图的主要步骤判读相图的步骤:
(1)判断有多少化合物生成,判断化合物的性质。
(2)用连线规则判断界线温度变化方向;
(3)用切线规则判断界线性质;
(4)根据无变量点划分相应的副三角形。
(5)确定无变量点的性质;
(6)分析析晶路程;
(7)判断相图上是否存在晶型转变、液相分层或形成固溶体等现象。2
复杂相图处理办法(1)判断化合物的性质——遇到一个复杂的三元相图,首先要了解系统中有那些化合物,其组成点和初晶区的位置,然后根据组成点是否在它的初晶区内,判断化合物的性质。
(2)划分副三角形——根据划分副三角形的原则和方法把三元相图划分为多个分三元系统,使复杂相图简化。
(3)判断界线的温度走向——根据连续规则判断各条界线的温降方向,并用箭头标出。
(4)判断界线性质——应用切线规则判断界线是共熔性质还是转熔性质,确定相平衡关系。共熔界线上用单箭头,转熔界线上用双箭头标出温降方向以表示界线性质不同
(5)确定三元无变量点——根据三元无变量点与对应的副三角形的位置关系或根据交汇于三元无变量点的三条界线的温度下降方向来判断无变量性质,确定无变量点上的相平衡关系。
(6)分析冷却析晶过程或加热熔融过程——按照冷却或加热过程的相比规律,选择一些系统点分析析晶或熔融过程。必要时用杠杆规则计算冷却或加热过程中平衡共存的各相含量。在分析冷却析晶过程时要主要一下情况:① 系统组成点正好位于界线上时如何判断初晶相?
首先判断界线的性质,若界线是共熔线,则熔体冷却时初晶相是界线两侧初晶区对应的两个晶体,可用切线规则球的初晶相的瞬间组成;若界线是转熔线,其熔体析晶时并不发生转熔?(因为没有任何晶体可转熔),而使析出单一固相,液相组成点直接进入单相区(即某一晶体的初晶区)并按背向线规则变化。
② 系统组成点正好位于无变量点上时的初晶相是什么?
若无变量点是三元低共熔点,则熔体析晶是共同析出该三组元的固相;若无变量点是单转熔点,则其熔体析晶时在无变量点并不发生四相无变量过程,也不发生转熔,而是液相组成点沿某一界线变化析晶,具体析晶性质由①点判断;若无变量点是双转熔点,则其熔体析晶时在无变量点并不发生四相无变量过程,不发生转熔,也不沿界线变化,而是析出单一固相,这时液相组成进入单相区并按照背向线规则变化。2
本词条内容贡献者为:
耿彩芳 - 副教授 - 中国矿业大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国