任何一个氧化还原反应都可以看成是两个半反应之和:一个是氧化剂(氧化型)在反应过程中氧化数降低,氧化型转化为还原型的半反应,另一个是还原剂(还原型)在反应过程中氧化数升高、还原型转化为氧化型的半反应。一对氧化型和还原型物质构成的共轭体系称为氧化还原电对,可用“氧化型/还原型”表示。1
氧化还原电对和原电池在氧化还原反应中,氧化剂获得电子由氧化型变为还原型,还原剂失去电子由还原型变为氧化型。由物质本身的氧化型和还原型组成的体系称为氧化还原电对。例如:
I2 + 2e- == 2I- 电对I2/I-
Zn2+ + 2e- == Zn 电对Zn2+/Zn
氧化型和还原型是相对而言的,例如电对MnO4/MnO2和电对MnO2/Mn2+ ,在前一个电对中MnO2是还原型,在后一个电对中MnO2是氧化型。要注意:电对都应写成“氧化型/还原型”。 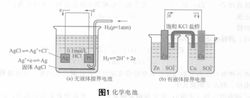
每一个电对对应的氧化还原反应,称为半反应。各电对对电子接受和给出的能力是不同的。因此,当把两个接受和给出电子能力不同的电对用导线连接起来时,就有电流流通,这就叫做原电池,见图1。2
氧化还原电对的作用氧化剂或还原剂的强弱,可用氧化还原电对的电极电位来衡量。对一个氧化还原反应来说,若Ox表示某一电对的氧化态,Red表示它的还原态,n为电子转移数,该电对的氧化还原半反应为 Ox + ne- == Red
用氧化还原电对的条件电极电位,能够准确衡量氧化剂或还原剂的强弱。正确地判断氧化还原反应的方向、次序和程度。3
氧化还原电对应用氧化-还原电对添加剂
氧化-还原电对添加剂的研究始于二次锂电池的限压保护,如今已经成为锂离子电池限压添加剂的主要组成部分,这类化合物包括芳香族化合物、金属茂化合物、聚吡啶配合物、锂的卤化物、噻蒽、茴香醚、联(二)茴香醚以及吩嗪等。
氧化-还原电对添加剂在电解液中的作用机理是:在正常充电条件下,氧化-还原电对[O]/[R]稳定存在于电解液中,不参加任何化学或电化学反应,对电池宏观电化学性能没有影响;当电池电压达到或超过电池截至电压时,还原态[R]在阴极表面被氧化,氧化产物[O]扩散到阳极表面被还原成为[R],还原产物[R]再扩散到阴极继续被氧化,整个过程沿“氧化—扩散—还原—扩散”循环进行。这样,阴极电位就被锁定在氧化-还原电对[O]/[R]的氧化电位附近,直到充电结束。在限压添加剂的工作过程中,法拉第电流仅仅是通过可逆的氧化-还原反应来承载,过充的电量既没有被储存在两电极,也没有用于电解液的不可逆氧化分解,只是伴随着添加剂的氧化一还原反应以热的形式释放出来,从这个意义上讲,限压添加剂的使用不会对电池造成根本性的破坏。4
本词条内容贡献者为:
郑国忠 - 副教授 - 华北电力大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国