定律定义
维里方程的一般表达式:
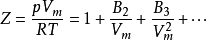
维里方程也可以用压力p的幂级数来表示
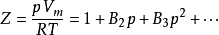
其中Vm是气体分子的摩尔体积,计算式:Vm=V/n;B2、B3分别称为第二、第三维理系数,它们与气体的种类有关,而且是温度的函数,在某一温度下,维理系数为0,实际气体行为就和理想气体近似。而且从以上两式可以看出摩尔体积越大,气压越低,则气体的行为越趋近于理想气体。当压力p→0,体积Vm→∞时,维里方程还原为理想气体状态方程。1
推导过程理想气体状态方程的表达式: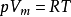 引入压缩因子Z,其大小反映出真实气体对理想气体的偏差程度,计算定义是Z等于Vm(真实)除以Vm(理想),Z是一个趋近于1的数字,在后面加入级数来进行修正即得到维里方程。
引入压缩因子Z,其大小反映出真实气体对理想气体的偏差程度,计算定义是Z等于Vm(真实)除以Vm(理想),Z是一个趋近于1的数字,在后面加入级数来进行修正即得到维里方程。
理论上, 任何气体的状态方程, 都可以用维里形式描述:
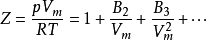
维里状态方程具有清楚的物理意义, 方程中第一项对应理想气体; 第二项描述了两个分子的相互作用; 第三项考虑了三个分子的作用, 余此类推. 对于处在高温、中高压状态下的气体, 多分子同时碰撞相互作用的情况已不可忽略,必须考虑高阶维里项. 但是, 随着维里系数阶数的提高, 计算的复杂性迅速增大, 甚至变得极其困难。2
适用范围维里方程有坚实的理论基础。用统计力学方法能导出维里系数,并赋予维里系数明确的物理意义:第二维里系数表示气体两个分子相互作用的效应,第三维里系数表示三个分子的相互作用,等等。原则上可以从理论上导出各个维里系数的计算式,但实际上高级维里系数的运算是十分困难的,目前除了简单的钢球模型外,还只能算到第三维里系数,通常维里系数由实验测定。
对于液相和汽相,维理状态方程描述一个 P-V等温过程更灵活,因为方程有较高次幂的体积、它们比三次状态方程更精确,普遍化主要是针对烃化合物。因此,对于这些化合物能够获得极好的结果,不推荐将它们用于极性化合物。
定律影响状态方程是实际气体热力计算的基础,当前常用的状态方程有B-W-R、M-H、R-K-S、P-R等方程。有的形式复杂,计算繁琐。有的由于有较强的针对性,在气体流体区内的计算精度欠佳,在热力工程应用中常受到一定限制。维里方程具有形式简明,且有明确的物理意义,但由于维里系数难于处理,在实际应用中,多限于第二维里系数以内。3维里方程在高密度区的精度不高,但由于具有理论基础,适应性广,很有发展前途。B-W-R方程、M-H方程都是在它的基础上改进得到的。




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国