NKK氨法
NKK氨法是日本钢管公司开发的工艺,该工艺流程主要分三部分,即SO2的吸收、 (NH4)2SO3氧化、(NH4)2SO4结晶。
NKK氨法应用塔型为填料塔,填料为聚丙稀格栅式。该塔有一定的特点,按其功能可 分三段。下段(从塔底开始) 是预洗涤段,主要作用是除尘和降温,在这阶段不加吸收剂 NH3; 中段是第一吸收段,加有吸收剂NH3; 上段为第二吸收段,没有NH3加入,仅用工 业水来洗涤。
NKK氨法对 (NH4)2SO3的氧化在单设一台氧化在反应器中进行。其氧化用氧由压缩 空气补充,氧化后的余气 (含有SO2和NH3) 排入系统中,。压缩空气压力为 0.5~1.0MPa。
GE公司氨法GE公司氨法的工艺流程如图所示,主要由预洗涤、SO2吸收、亚硫酸铵氧化和 结晶四个工序构成所需工艺系统。
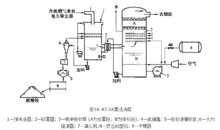
(1) 烟气系统。烟气经过静电除尘器除尘后,进入烟气预洗涤段,由于预洗涤段也具有 对SO2的吸收作用,所以该技术也可视为两段吸收或称双循环吸收。烟气在预洗涤器中能 起脱除SO2的作用,但其吸收量较小,这是由预洗涤器尚未通入氨气,其pH值小于2所 致。烟气经过预冷却器冷却饱和后进入吸收塔,经氨水洗涤脱硫,净化后烟气经除雾器除去水滴,由烟囱排出。
(2) SO2吸收系统。氨法SO2吸收反应在SO2吸收塔中进行。来自预洗涤器的已被冷 却饱和的烟气进入SO2吸收塔,烟气与喷淋的氨液逆向流动接触,SO2与稀硫酸铵液反应, 生成 (NH4)2SO3或硫化氢。稀硫酸液靠浆液循环泵进行循环。对于 (NH4)2SO3的氧化工 序,是在吸收塔底部进行的,生成(NH4)2SO4。液氨是通过减压蒸发后同空气同时送入塔 底,以维持吸收液的pH值。
根据GE公司提供的试验数据,吸收液中 (NH4)2SO4的浓度是热烟气温度和SO2含量 的函数,即使烟气中SO2浓度高达6 100mg SO2/kg烟气,吸收液中 (NH4)2SO4的浓度也 不会超过30% (质量)。为排出已产生的 (NH4)2SO4,从吸收塔底部排出适量的吸收液,但同时必需以自动补 水方式来维持恒定的液位。
(3) 硫酸铵回收系统。预洗涤段硫酸铵结晶液和吸收段硫酸铵结晶液先经旋流器浓缩, 经离心机脱水,使含水量小于2%,回收。
NADS脱硫净化技术NADS (Novel Ammonia De—Sulphurization,氨—肥法) 是由中国华东理工大学开发成功的一种新的脱硫方法,它是采用氨来吸收烟气中的SO2,可根据不同情况生成 NH4HSO3、(NH4)2SO3,结合化肥生产,将脱SO2产物生成硫氨、磷铵或硝铵等化肥,并 生产工业用高浓度硫酸。
相关化学反应:
SO2+xNH3+H2O⇌ (NH4)xH2-xSO3
上式中x值现有氨法中x=2,而NADS法的x=1.2~1.4。
NADS除能生产 (NH4)2SO4,同时也可与磷铵化肥厂或硝铵化肥厂联合生产 (NH4)3PO4、NH4NO3及工业高浓度硫酸,其反应如下
2(NH4)xH2-xSO3+xH2SO4⇌x(NH4)2SO4+2SO2↑+2H2O
(NH4)xH2-xSO3+xH3PO4⇌xNH4H2PO4+SO2↑+H2O
(NH4)xH2-xSO3+xHNO3⇌xNH4NO3+SO2↑+H2O
SO2+1/2O2+H2O⇌H2SO4+热量
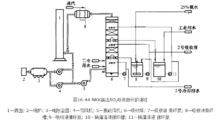
工艺流程以硫酸铵—硫酸为例, NADS的工艺流程如图16-46 所示。由静电除尘器来的烟先 经GGH,冷段降温 (由140~ 160℃) 冷却到小于80℃进入 SO2吸收塔,吸收塔内吸收温 度约45~60℃之间,SO2的吸 收率大于95%。

吸收塔内烟气中SO2与NH3和H2O的吸收结合生成含有 (NH4)2SO3,NH4HSO3和 少量Na2SO4的过程与其他氨法一样,在NADS技术中NH3和H2O是分别进入吸收塔,这 样做有三大好处:
(1) 吸收塔出口NH3含量低,氨损耗小。
(2) 吸收液循环量小,气液比大,能耗低。
(3) 生成 (NH4)2SO3浓度高,有利于硫铵化肥生产,节约成本。
混合液中,总盐含量约为30%~50%,具体值与烟气中的SO2浓度有关,净化后烟气 中含SO2量约为10~100mL/m。
NADS法中吸收系统阻力通常在1.96~2.9kPa之间,引风机富余压头难以满足,需装 增压风机。
吸收SO2后产生的亚硫酸铵浆液用其酸解装置,硫酸生产装置和硫酸铵生产装置来完 成后续工序。
(1) 亚硫酸铵溶液酸解装置。该装置是将 (NH4)2SO3(包括NH4HSO3) 与H2SO4 (或者H3PO4、HNO3) 反应,生成 (NH4)2SO4(或NH4H2PO4、NH4NO3) 溶液和SO2 气体,同时酸解过程送入空气,使得SO2在空气混合物中浓度达10%~20% (质量)。酸解 中硫酸原料的浓度为98% (质量),酸解是放热反应,温度可达70~80℃,所以SO2解析 不需外部热源。最后,用氨调节pH值,中和富余的硫酸。
(2) 硫酸生产装置。包括SO2催化氧化 (催化剂为V2O5/SiO2) 为SO2的转化器和换 热器,SO2气体干燥塔和SO2气体吸收塔及酸循环槽等设备。
(3) 硫酸铵生产装置。硫酸铵溶液经蒸发、分离、干燥,包装出厂。
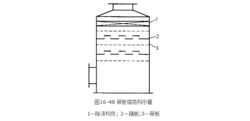
筛板塔NADS技术采用的是筛板塔。它用的是一种大孔径、高开孔率筛板做传质元件,具有 阻力小 (0.15~0.3kPa) 的特点,是传统板式塔的50%; 空塔气速可达4m/s,是传统板式 塔两倍。塔体可由耐热玻璃钢制造。
NADS技术气液接触方式是喷雾方式,且可一塔多级吸收,图16-48为二层隔板,三层 筛分段吸收。段层数视系统需要而增减。
氨—亚铵法氨—亚铵法是直接吸收SO2后的母液加工成产品——亚硫酸铵 (简称亚铵)。亚铵可替 代烧碱用于制浆造纸工业。该法工艺流程简单,它可用气氨、氨水及碳酸氢铵作氨源,取材灵活。
反应原理用碳酸氢铵溶液吸收SO2,主要反应为:
2NH4HCO3+SO2→ (NH4)2SO3+H2O+2CO2
(NH4)2SO3+SO2+H2O→2NH4HSO3
烟气中一般含一定量的氧,在溶液中还会发生副反应:
(NH4)2SO3+1/2O2→ (NH4)2SO4
对于硫酸尾气,含有少量SO3,会发生如下反应:
2 (NH4)2SO3+SO3+H2O→ (NH4)2SO4+2NH4HSO3
吸收SO2后,母液主要含NH4HSO3,加固体NH4HCO3中和,可析出亚铵晶体,反应如下:
NH4HSO3+NH4HCO3→ (NH4)2SO3+CO2+H2O
此反应为吸热反应,溶液不经 冷却即可降至0℃左右。
工艺流程氨—亚铵工艺 流程见图16-50,全部工艺可分为吸 收、中和、分离、氧化四个阶段。
1) 吸收。含SO2的气体依次进 入串连的吸收塔Ⅰ和Ⅱ,在塔内SO2 被循环喷淋的吸收液吸收后排放。 在第Ⅰ塔中吸收液尽量保持较高的 浓度,以便生成较多的NH4HCO3, 并不断抽取部分溶液送至中和工序, 以便制取固体 (NH4)2SO3产品。在 第Ⅱ塔中,吸收液浓度可降低些,保持高碱度,使(NH4)2SO3含量高些。为保持各塔循环液碱度和液位不变,要不断地补充 固体NH4HCO3。
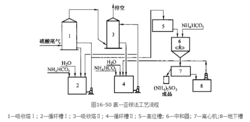
2) 中和。由于NH4HSO3比 (NH4)2SO3 在水中溶解度大,第Ⅰ塔引出高浓 度NH4HSO3溶液,在中和器内加入NH3HSO3 进行反应,反应后NH4HSO3转化成 (NH4)2SO3,而(NH4)2SO3的溶解度小,大量 晶体析出。
3) 分离。由中和器底部引出含有 NH4HSO3·H2O晶体的悬浮液通过离心机分 离,分离出白色固体NH4HSO3·H2O产品,滤 液送回第Ⅱ塔继续吸收。
4) 氧化。烟气中存在氧对NH4HSO3氧化率可达5%~14%,而晶体亚铵氧化成为硫 铵氧化率一般为0.3%~7%,最高可达50%。2




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国