高效液相色谱法原理
试样用稀酸经121℃~123℃高压釜处理,提取维生素B2(核黄素),过滤后,用高效液相色谱仪测定仪,保留时间定性,外标法定量。
试剂如无特别说明,所有世纪均为分析纯。
(1)水:符合GB/T 6682-2008规定的一级水。
(2)冰乙酸。
(3)甲醇:色谱纯huo经重蒸。
(4)盐酸溶液(0.1mol/L):吸取2.1mL盐酸(ρ20≈1.19g/mL),用水稀释至250mL,混匀。
(5)氢氧化钠溶液(1mol/L):称取10g氢氧化钠,溶于水中,用水稀释至250mL。
(6)乙酸溶液(0.02mol/L):吸取1.14mL冰乙酸,用水稀释至1L。
(7)乙酸钠溶液(0.05mol/L):称取3.4g三水乙酸钠,溶于水中,用水稀释至500mL,冰乙酸调pH为4.5。
(8)精密pH试纸:范围3.8-5.4。
(9)维生素B2标准溶液
标准储备液(100ug/mL):称取50.0mg维生素B2标准品,用乙酸溶液(0.02mol/L)溶解,并至500mL定容棕色容量瓶中(可在水浴上加热溶解,冷却后再定容)。
标准工作液(0.5ug/mL):吸取标准储备液(100ug/mL)1.00mL于100mL棕色容量瓶中,用乙酸溶液(0.02mol/L)定容,混匀,吸取此溶液5.00mL于100mL棕色容量瓶中,用水定容,混匀,临用时配置。
仪器和设备实验室常规仪器及下列仪器。
(1)机械设备:用于试样的均质化,包括高速旋转的切割机,或多孔板的孔径不超过4mm的绞肉机。
(2)高压釜:温度可控制在121℃~123℃。
(3)高效液相色谱仪:带紫外或荧光检测器。
取样实验室所收到的样品应具有代表性且在运输和储藏过程中无受损或发生变化。
取样方法参见GB∕T 9695.19。
取有代表性的样品200 g。
试样制备使用适当的机械设备将试样均质。注意避免试样的温度超过25℃。若使用绞肉机,试样至少通过该设备两次。
将试样装入密封的容器里,防止变质和成分变化。试样应在均质化后24 h内尽快分析。
分析步骤(1)试样处理
称取试样5 g(准确至0.001 g)于250 mL具塞锥形瓶中,加入盐酸溶液(4.4)10 mL,塞好瓶盖,用力振摇。用盐酸溶液冲洗瓶壁,总体积约为60 mL。将锥形瓶放人121℃~123℃高压釜中加热30 min,取出冷却至室温。用氢氧化钠溶液调pH为4.0~4.5,使蛋白质沉淀后,转移至500 mL棕色容量瓶中,用水定容,混匀,过滤,滤液避光备用。滤液经0.45 μm滤膜过滤后待测。
(2)测定
液相色谱参考条件
a)色谱柱:C18柱(150 mm×4.6 mm,5μm),或相当者;
b)流动相:甲醇+0.05 moI/L乙酸钠溶液(pH 4.5)=35+65(体积比);
c)流速:1.0 mL/min;
d)柱温:30℃;
e)检测波长:激发波长为440 nm,发射波长为565 nm;
f)进样量:20 μL。
根据试样溶液中的含量情况,选定峰面积相近的标准工作液。标准工作液和试样溶液中维生素B2的响应维生素B2值均应在仪器检测线性范围内。标准工作液和试样溶液等体积间隔进样测定。根据保留时间定性,外标法定量。标准色谱图参见附图。
(3)平行试验
按试样处理和分析步骤对同一试样进行测定。
(4)空白实验
除不加入试样外,均按试样处理和分析步骤进行测定。
计算 式中:
式中:
X:试样中维生素B2的含量(mg/100g);
c:标准工作液中维生素B2的浓度(ug/mL);
A:试样中维生素B2的峰面积;
V:试样溶液的最终定容体积(mL);
Ai:标准工作液中生素B2的峰面积;
m:试样质量(g)。
计算结果应扣除空白,结果准确至0.01mg/100g。
精密度同一分析者在同一实验室采用相同的方法和相同的仪器,在短时间间隔内对同一样品独立测定两次,两次测试结果的绝对差值不得超过算术平均值的20%。1
比色法原理试样用稀酸经121℃~123℃高压釜处理,提取维生素B2(核黄素),维生素B2在中性或酸性溶液中经照射产生蓝色荧光,荧光强度与维生素B2的浓度成正比,以此测定维生素B2的含量。
试剂如无特别说明,所有世纪均为分析纯。
(1)水:符合GB/T 6682规定的三级水。
(2)连二亚硫酸钠。
(3)高锰酸钾溶液(40g/L):称取4g高锰酸钾,溶于水中用水稀释至100mL。
(4)3%过氧化氢溶液:取10mL 30%过氧化氢,用水稀释至100m。
(5)冰乙酸
(6)盐酸溶液(0.1mol/L):吸取2.1mL盐酸(ρ20≈1.19g/mL),用水稀释至250mL,混匀。
(7)氢氧化钠溶液(1mol/L):称取10g氢氧化钠,溶于水中,用水稀释至250mL。
(8)乙酸溶液(0.02mol/L):吸取1.14mL冰乙酸,用水稀释至1L。
(9)精密pH试纸:范围3.8-5.4。
(10)维生素B2标准溶液
标准储备液(100ug/mL):称取50.0mg维生素B2标准品,用乙酸溶液(0.02mol/L)溶解,并至500mL定容棕色容量瓶中(可在水浴上加热溶解,冷却后再定容)。
标准工作液(0.5ug/mL):吸取标准储备液(100ug/mL)1.00mL于100mL棕色容量瓶中,用乙酸溶液(0.02mol/L)定容,混匀,吸取此溶液5.00mL于100mL棕色容量瓶中,用水定容,混匀,临用时配置。
仪器和设备实验室常规仪器及下列仪器。
(1)荧光分光光度计。
(2)机械设备:用于试样的均质化,包括高速旋转的切割机,或多孔板的孔径不超过4mm的绞肉机。
(3)高压釜:温度可控制在121℃~123℃。
取样实验室所收到的样品应具有代表性且在运输和储藏过程中无受损或发生变化。
取样方法参见GB∕T 9695.19。
取有代表性的样品200 g。
试样制备使用适当的机械设备将试样均质。注意避免试样的温度超过25℃。若使用绞肉机,试样至少通过该设备两次。
将试样装入密封的容器里,防止变质和成分变化。试样应在均质化后24 h内尽快分析。
分析步骤(1)试样处理
称取试样5 g(准确至0.001 g)于250 mL具塞锥形瓶中,加入盐酸溶液(4.4)10 mL,塞好瓶盖,用力振摇。用盐酸溶液冲洗瓶壁,总体积约为60 mL。将锥形瓶放人121℃~123℃高压釜中加热30 min,取出冷却至室温。用氢氧化钠溶液调pH为4.0~4.5,使蛋白质沉淀后,转移至500 mL棕色容量瓶中,用水定容,混匀,过滤,滤液避光备用。滤液经0.45 μm滤膜过滤后待测。
(2)测定
吸取备用滤液和维生素B2标准工作液(0.5ug/mL)各10.0mL,分别置于两支25mL棕色试管中,加入冰乙酸1.00mL。在不断摇动下加入高锰酸钾溶液(40g/L)4滴,使溶液显紫色,静置2min,滴加过氧化氢溶液两滴,摇匀,使紫色在10s内褪去。
于激发波长440nm,发射波长565nm处,用荧光分光光度计测定其荧光强度I和I`。
在各试管中分别加入二亚硫酸钠20mg,轻摇,10s内测其最小荧光强度Q和Q`。
计算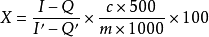
X:试样中维生素B2的含量(mg/100g);
I:试样溶液的荧光强度;
Q:试样溶液加连二亚硫酸钠后的荧光强度;
I`:维生素B2标准工作液的荧光强度;
Q':维生素B2标准工作液加连二亚硫酸钠后的荧光强度;
c:维生素B2标准工作液的浓度(ug/mL);
m:试样质量(g)。
计算结果准确至0.01mg/100g。
精密度同一分析者在同一实验室采用相同的方法和相同的仪器,在短时间间隔内对同一样品独立测定两次,两次测试结果的绝对差值不得超过算术平均值的20%。1




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国