自由电子碰撞是金属导体中的自由电荷。
碰撞“碰撞”在物理学中表现为两粒子或物体间极短的相互作用。 碰撞前后参与物发生速度,动量或能量改变。由能量转移的方式区分为弹性碰撞和非弹性碰撞。弹性碰撞是碰撞前后整个系统的动能不变的碰撞。弹性碰撞的必要条件是动能没有转成其他形式的能量(热能、转动能量),例如原子的碰撞。非弹性碰撞是碰撞后整个系统的部分动能转换成至少其中一碰撞物的内能,使整个系统的动能无法守恒。 下面示例的碰撞原理的数学表述是由克里斯蒂安·惠更斯在1651年到1655年间提出的。
碰撞过程的总述和分类通过作用在两个碰撞物接触点的切线称为“撞击线”。通过撞击线的接触点构成两个碰撞物的总切面,称作“接触面”。
设两个物体的质量为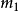 和
和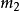 , 它们的初速度为
, 它们的初速度为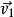 和
和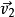 , 末速度为
, 末速度为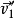 和
和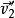 . 碰撞瞬时总速度为
. 碰撞瞬时总速度为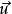 。
。
在“垂直碰撞”中,两个碰撞物的重心在同一撞击线上,在“斜碰撞”中则不然。当末速度向量随撞击线平行摆动,则称为“正面撞击”,否则称为“非正面撞击”。
碰撞后碰撞物能够恢复碰撞前的形态称为“弹性碰撞”,某些机械能没有转换为热能并产生变形的碰撞,称为“非弹性碰撞”,二者之间的情况则是“实际碰撞”。
在超弹性碰撞中内能转换超过最少中一个碰撞物的动能。其动能在此次碰撞后大于其碰撞前的动能。数学表达同总述的非弹性碰撞,为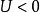 。
。
正面碰撞下面将只针对正面撞击进行阐述,预设碰撞物可以自由移动,两个碰撞物的速度因子较撞击线不变: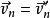 , 因此碰撞力只能沿着撞击线作用。碰撞物中心垂直于撞击线,物体碰撞后不会发生旋转运动。由此速度因子
, 因此碰撞力只能沿着撞击线作用。碰撞物中心垂直于撞击线,物体碰撞后不会发生旋转运动。由此速度因子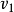 和
和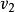 (标量) 平行于撞击线。
(标量) 平行于撞击线。
碰撞理论碰撞理论研究的是粒子间的一种相互作用。力学理论基础是动量守恒定律和能量守恒定律。粒子多种多样使碰撞理论分为:原子的碰撞、等离子体的碰撞等等。同属于粒子间的相互作用的还有:轻原子核的聚合、正负电子的湮没、荷电π介子的衰变、中子的beta衰变、核子N与π介子的相互作用、光子gamma与电子e-的散射等。
物理学和化学之中都涉及到粒子间的相互作用。每个物体的各自动能发生不连续变化的过程称作物理碰撞,简称碰撞。例如,电子枪发射的高速电子与原子核外电子之间的相互作用。其中,轫致辐射应该是没有发生碰撞的,所以动能变化是连续的。而,如果电子在原子核外电子电场力的作用下减速后,还具有充足的动能,就会把原子的内层电子碰撞出轨道。碰撞过程的每个电子的各自动能的变化是不连续的。有新物质生成的过程称为化学反应,简称反应。例如,轻原子核(含氢H的同位素)的聚合生成氦He、质子p和中子n。物理化学研究的是二者兼有的相互作用。粒子分裂利用动量守恒和能量守恒定律可以得到一系列关于各种力学过程特性的结论。特别重要的是,这些性质完全不依赖于粒子间具体的相互作用形式。
粒子分裂研究的是粒子自动、没有外力作用分裂成两个组成部分的问题,分裂后两个粒子独立运动。
在粒子分裂前静止的参考系中观察这个过程是最简单的。根据动量守恒定律,分裂后两个粒子动量之和仍为零,即两个粒子的动量大小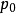 相等方向相反。动量的大小可以由能量守恒定律:
相等方向相反。动量的大小可以由能量守恒定律:
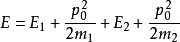
确定,其中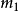 和
和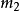 是两个粒子的质量,
是两个粒子的质量,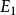 和
和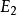 是两个粒子的内能,而
是两个粒子的内能,而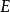 是原来粒子的初始内能。用
是原来粒子的初始内能。用 表示分裂能,即:
表示分裂能,即:
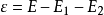
能量为正时反应才可能发生。由此可以确定动量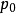 的大小,两个粒子的速度分别为:
的大小,两个粒子的速度分别为:
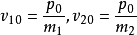
粒子是足够小的点,这样的点又称为质点。这样总动量为零的参考系称为质心参考系。如果反应前粒子以一定的速度相对此参考系运动,那么这个参考系称作实验室参考系。
基本信息自由电子碰撞: 金属导体中的自由电荷。金属原子的外层电子(价电子)脱离原子核束缚后而成为自由电子。各种金属的自由电子密度有相同的数量级。n型半导体中的多数载流子是自由电子发生碰撞
电子电子是一种基本粒子,目前无法再分解为更小的物质。其直径是质子的0.001倍,重量为质子的1/1836。电子围绕原子的核做高速运动。电子通常排列在各个能量层上。当原子互相结合成为分子时,在最外层的电子便会由一原子移至另一原子或成为彼此共享的电子。
这是由爱尔兰物理学家乔治·丁·斯通尼于1891年根据电的electric+-on“子”造的字
电子属于亚原子粒子中的轻子类。轻子被认为是构成物质的基本粒子之一,即其无法被分解为更小的粒子。它带有1/2自旋,即又是一种费米子(按照费米—狄拉克统计)。电子所带电荷为e=1.6×10的-19次方库仑,质量为9.10×10-31kg(0.51MeV/c2)。通常被表示为e-。电子的反粒子是正电子,它带有与电子相同的质量,自旋和等量的正电荷。
物质的基本构成单位——原子是由电子、中子和质子三者共同组成。相对于中子和质子组成的原子核,电子的质量极小。质子的质量大约是电子的1840倍。
特征1.电子是在原子核外距核由近及远、能量由低至高的不同电子层上分层排布; 2.每层最多容纳的电子数为n的平方的二倍个(n代表电子层数); 3.最外层电子数不超过8个(第一层不超过2个),次外层不超过18个,倒数第三层不超过32个。 4.电子一般总是尽先排在能量最低的电子层里,即先排第一层,当第一层排满后,再排第二层,第二层排满后,再排第三层。 电子在原子核外空间一定范围内出现,可以想象为一团带负电的云雾笼罩在原子核周围,所以,人们形象地把它叫做“电子云”。1
本词条内容贡献者为:
李雪梅 - 副教授 - 西南大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国