肠道菌群可以调节机体的情绪、认知、记忆等,并且与焦虑、抑郁、自闭症、多动症、阿尔茨海默病等神经疾病存在密切关联。
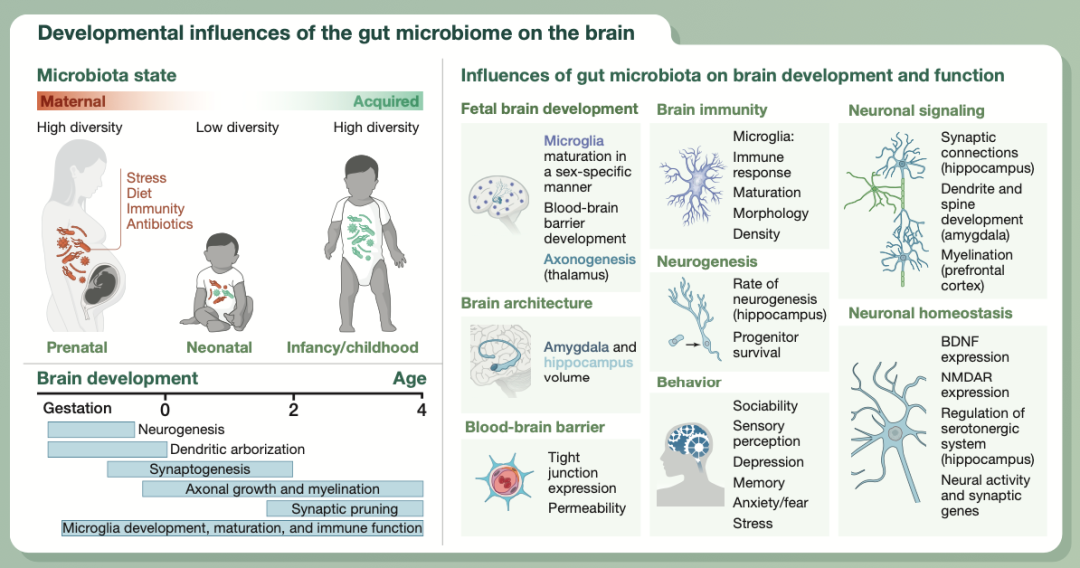 动物研究表明,肠道菌群还能影响后代大脑健康。无菌饲养、使用抗生素治疗或其他环境因素都能造成母体微生物组或出生后的早期微生物组改变,可能会导致子代的大脑免疫、血脑屏障通透性、大脑结构和神经回路在调节神经元的产生、特性和成熟方面出现异常。这些影响会持续到成年,并易导致长期的行为缺陷。
动物研究表明,肠道菌群还能影响后代大脑健康。无菌饲养、使用抗生素治疗或其他环境因素都能造成母体微生物组或出生后的早期微生物组改变,可能会导致子代的大脑免疫、血脑屏障通透性、大脑结构和神经回路在调节神经元的产生、特性和成熟方面出现异常。这些影响会持续到成年,并易导致长期的行为缺陷。
也就是说,在神经发育的关键窗口期4岁之前,维持微生物组平衡至关重要。
 【那么肠道菌群是如何影响肠道与大脑之间的交流呢?】
【那么肠道菌群是如何影响肠道与大脑之间的交流呢?】
【途径1:免疫系统】
肠道菌群与肠道免疫系统之间存在密切的互作。包括代谢产物(例如短链脂肪酸 SCFAs)和膜成分(例如多糖 A)在内的微生物组成分均可影响免疫稳态,形成促炎或抗炎的局部免疫反应。
肠道菌群还可以调节位于大脑的免疫细胞——小胶质细胞的发育、成熟和功能。
 在神经炎症的背景下,血脑屏障通透性的改变,可促进微生物组分通过这一屏障,以及外周免疫细胞对脑实质的侵袭。中风等疾病引起的大脑炎症会改变肠道菌群的组成,从而导致恶性循环——肠道菌群失调进一步加剧神经免疫反应,从而加重了大脑病理的严重程度。
在神经炎症的背景下,血脑屏障通透性的改变,可促进微生物组分通过这一屏障,以及外周免疫细胞对脑实质的侵袭。中风等疾病引起的大脑炎症会改变肠道菌群的组成,从而导致恶性循环——肠道菌群失调进一步加剧神经免疫反应,从而加重了大脑病理的严重程度。
【途径2:内分泌/循环系统】
微生物和代谢物,如次级胆汁酸、吲哚衍生物和 SCFAs,可以通过肠道内分泌细胞(EECs)和肠嗜铬细胞(ECCs)发出信号,从而调节神经肽的分泌,例如可调节食欲的激素胰高血糖素样肽-1(GLP1)和神经调节剂(如激素和神经递质血清素)。此外,某些肠道细菌可以直接合成和释放神经递质和神经调节剂。比如罗伊氏乳杆菌,长双歧杆菌等。
 【途径3:神经途径】
【途径3:神经途径】
微生物组分、微生物调节激素和微生物依赖性免疫介质,可直接与肠神经系统及其支配的迷走神经和脊髓传入神经相互作用。产生的局部信号可通过感觉神经回路传递到参与认知、情绪、恐惧/焦虑、躯体感觉和/或进食行为的大脑区域。
反过来,迷走神经和脊髓传出神经会传递信号至肠粘膜,并直接(如通过脊神经衍生信号调节寄生虫入侵)或间接(通过与肠神经系统的相互作用)影响胃肠稳态。
通过这种自上而下的信号或微生物相关分子调节肠道内神经元的活动,最终可影响胃肠道生理、局部免疫功能和肠道菌群的组成。
菌群-肠-脑轴其中的免疫、内分泌、系统和神经通路是高度复杂和相互关联的。
Benakis, C., Martin-Gallausiaux, C., Trezzi, J.P., Melton, P., Liesz, A., and Wilmes, P. (2020). The microbiome-gut-brain axis in acute and chronic brain diseases. Curr. Opin. Neurobiol. 61, 1–9.




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国